1.AM:纳米颗粒结合TLR7/8激发剂用于抗肿瘤的局部免疫疗法
局部治疗是指将肿瘤微环境从免疫抑制转变为促免疫原化来引起全身抗肿瘤免疫应答。在肿瘤微环境中,树突状细胞(DCs)的激活是产生T细胞抗肿瘤反应的关键。而使用激发剂去激发多种模式识别受体的治疗对于激活DCs非常有效,但同时也会产生严重的免疫相关不良反应。Nuhn等人报道了一种高效TLR7/8激发剂和纳米粒子结合,在不影响抗肿瘤治疗效果的前提下,二者相结合的局部治疗可以有效激活前哨淋巴结中的DCs,促进肿瘤抗原特异性CD8 T细胞的增殖。此外,结合了PDL1抗体检查点抑制和Flt3L(一种激活骨髓中的DCs的生长因子)的良好治疗效果也从实验中得到了证实。这一研究为提供空间性控制的免疫激活用于局部肿瘤治疗提供了新的思路。
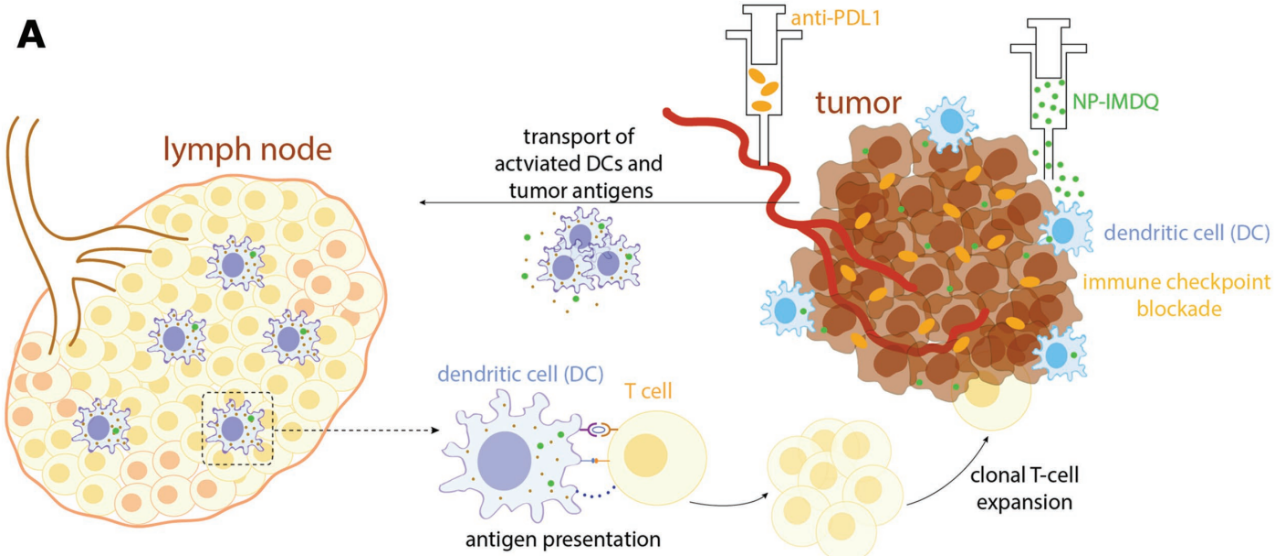
Nuhn L, Koker S D, et al.Nanoparticle-Conjugate TLR7/8 Agonist Localized Immunotherapy Provokes Safe Antitumoral Responses[J]. Advanced Materials, 2018.
DOI: 10.1002/adma.201803397
https://doi.org/10.1002/adma.201803397
2. Nat. Med.:CAR19治疗急性淋巴细胞白血病中的靶抗原丢失遗传机制
Orlando等人鉴定了CD19的基因突变和CD19在嵌合抗原受体(CAR)治疗复发时杂合性的丧失。这种突变通常存在于绝大多数耐药肿瘤细胞中,并被预测会导致一个不具有功能或无跨膜结构域的截断蛋白产生,从而导致表面抗原的丢失。CD19的这种不可逆转的丧失也说明今后应该采用另一种靶向性或组合性的CAR治疗方法来提高疗效。
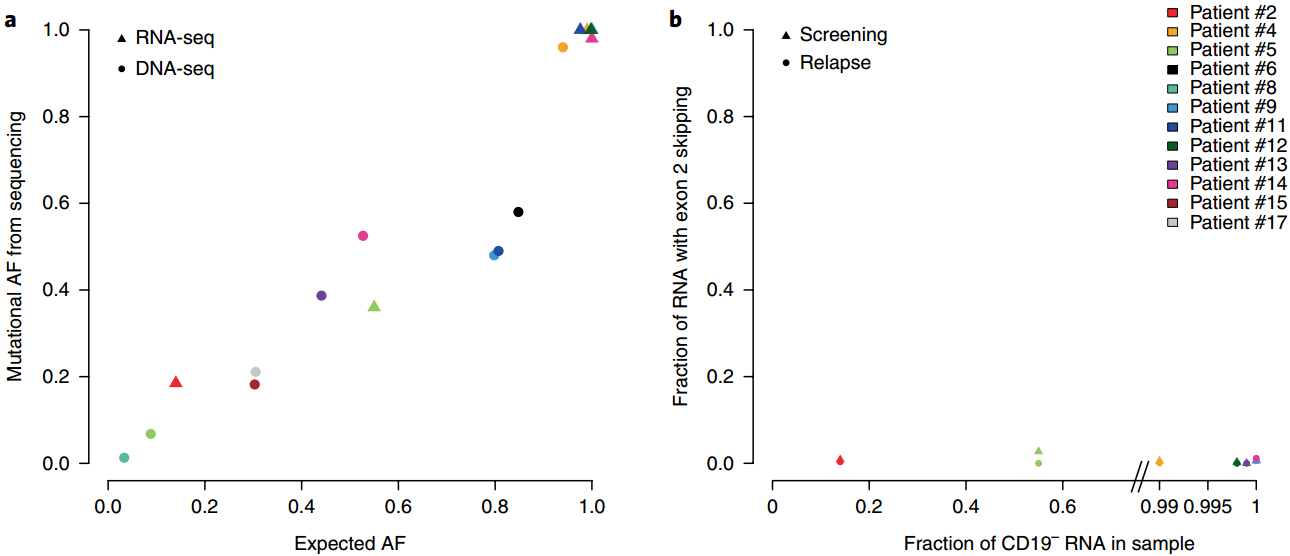
Orlando E J, Han X, et al.Genetic mechanisms of target antigen loss in CAR19 therapy of acutelymphoblastic leukemia[J]. Nature Medicine, 2018.
DOI:10.1038/s41591-018-0146-z
https://doi.org/10.1038/s41591-018-0146-z
3. AM:模拟T细胞的纳米颗粒用于治疗HIV的传染
为了改善对人类免疫缺陷病毒(HIV)的治疗和预防,开发有效的针对广谱病毒感染的治疗策略是非常重要的。在最近的细胞膜包覆技术的启发下,CD4+T细胞膜被收集并涂在聚合核表面。由此产生的T细胞膜涂层纳米颗粒(TNPs)具有对HIV结合至关重要的T细胞表面抗原。TNPs作为病毒攻击的诱饵,可以将病毒从它们预定的宿主目标中转移出来,从而中和HIV病毒。这个诱骗策略有助于克服HIV的遗传多样性。研究表明,TNPs会有选择性地与gp120结合,这是一种HIV病毒的重要包膜糖蛋白。因此TNPs可以有效地中和了单核血细胞和人类单核细胞衍生的巨噬细胞的病毒感染。这一研究证明利用天然T细胞的功能的TNPs作为一种新的治疗药物来对抗HIV感染具有巨大的潜力。
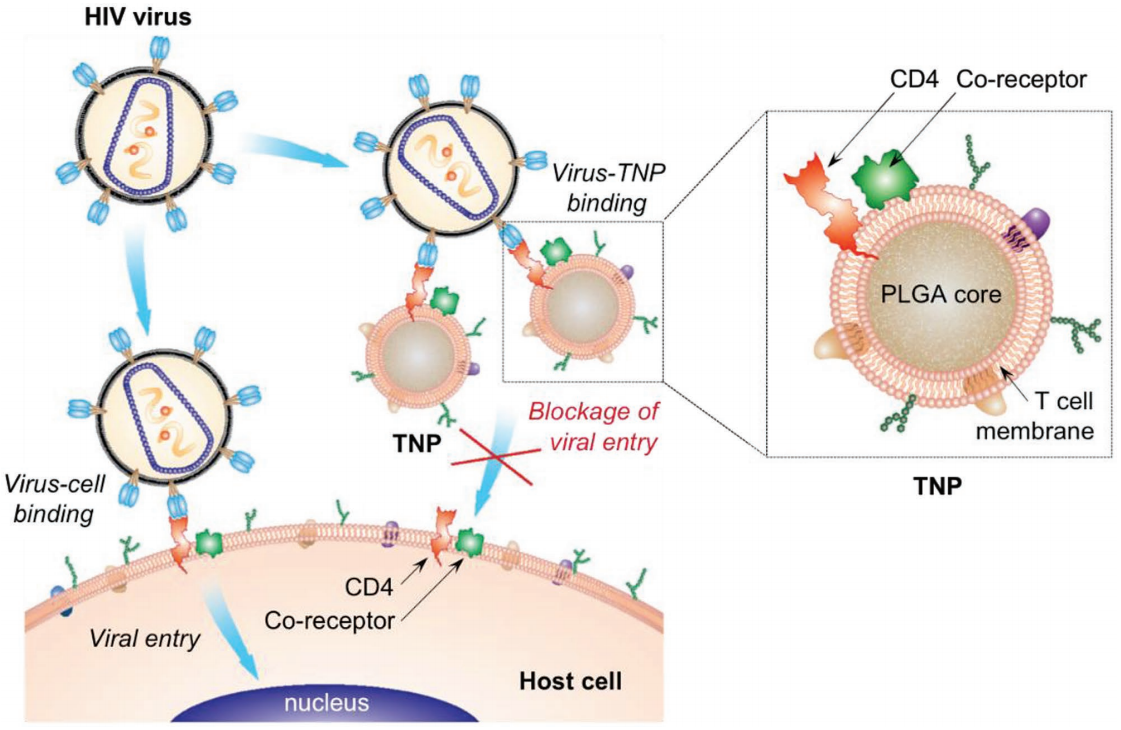
Wei X,Zhang G, et al. T-Cell-Mimicking Nanoparticles Can Neutralize HIV Infectivity[J]. Advanced Materials, 2018.
DOI:10.1002/adma.201802233
https://doi.org/10.1002/adma.201802233
4. Nat. Commun.:编辑RNA衍生表位作为癌症抗原发挥作用并引发免疫反应
除了基因组突变以外,在mRNA序列中引入核苷酸同样可以使得蛋白质的序列变化。这种对RNA的编辑有助于改善对不同类型的人类疾病包括癌症的治疗。Zhang等人报告了由RNA编辑产生的缩氨酸确实是由人类白细胞抗原(HLA)分子自然呈现的。实验的证据表明,在人类肿瘤中会产生特异性针对被编辑的肽的效应CD8+T细胞,并攻击正在呈现这些表位的肿瘤细胞。这些发现表明,对RNA的编辑扩展了HLA呈现的自我抗原的种类,并且这些抗原可以被免疫系统识别。
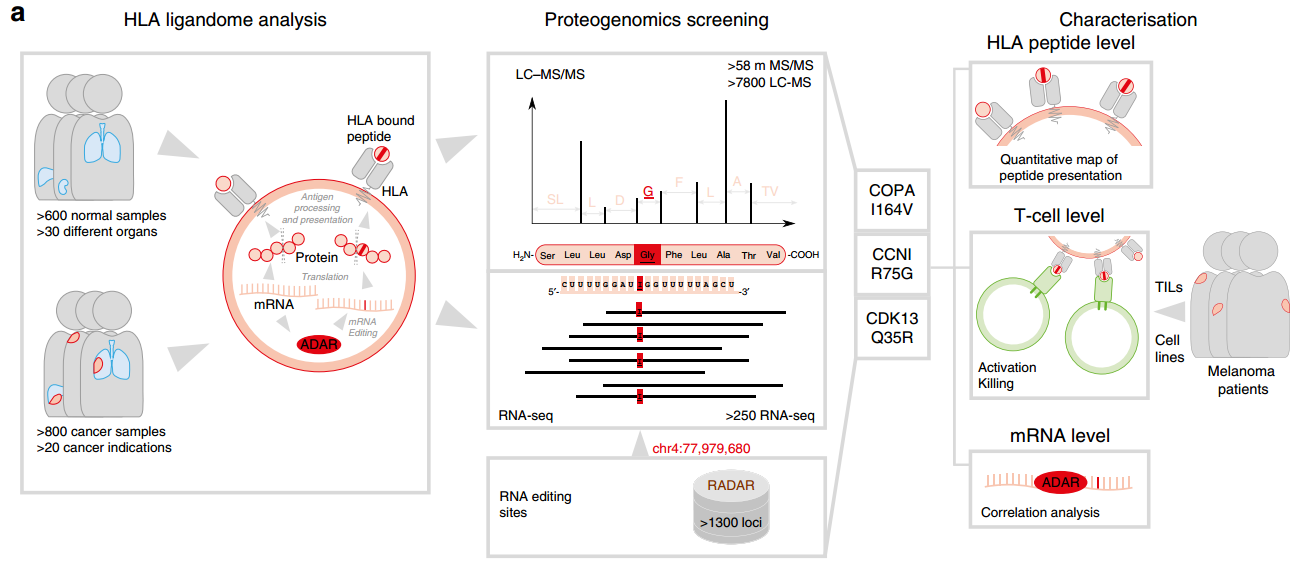
Zhang M, Fritsche J, et al. RNA editing derivedepitopes function as cancer antigens to elicit immune responses[J]. Nature Communications, 2018.
DOI: 10.1038/s41467-018-06405-9
https://www.nature.com/articles/s41467-018-06405-9
5. Nat. Med.:单个白血病B细胞转导对嵌合抗原受体T细胞疗法的抵抗力
Ruella等人报告了一例CD19-白血病患者在注射靶向CD19的嵌合抗原受体(CAR)T细胞(CTL019) 9个月后复发,该细胞会异常表达抗CD19的CAR。实验发现,这是由于在T细胞制造过程中,CAR 基因无意中被引入到单个白血病B细胞中,其产物在cis中与白血病细胞表面的CD19表位结合,掩盖了CTL019对其的识别病由此产生耐药性。
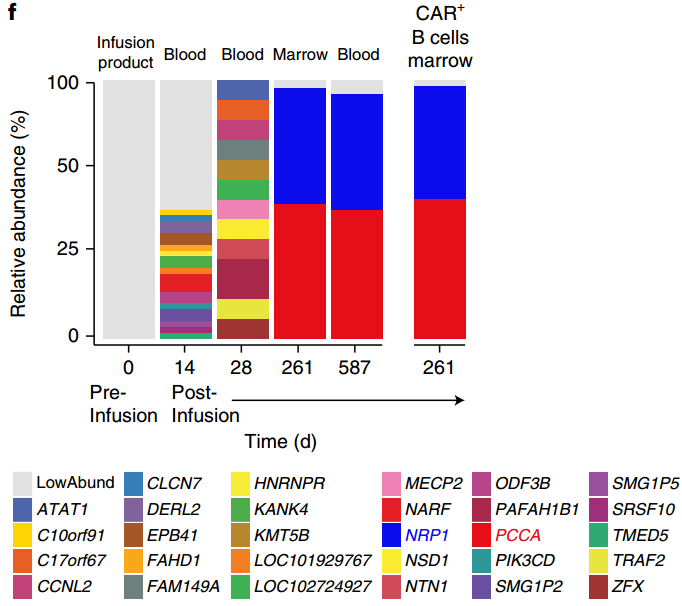
Ruella M, Xu J, et al.Induction of resistance to chimeric antigen receptor T cell therapy bytransduction of a single leukemic B cell[J]. Nature Medicine, 2018.
DOI:10.1038/s41591-018-0201-9
https://doi.org/10.1038/s41591-018-0201-9
6. Nat. Commun.:基因工程mRNA表达的抗体可预防呼吸道合胞病毒感染
肺是临床上重要的传染性病原体(呼吸道合胞体病毒RSV)的重要预防靶点。Tiwari开发了一种基于mRNA的方法,即通过气溶胶直接在肺部表达中和抗体以防止RSV感染。实验首先使用帕利珠单抗使RSV F数减少90.8%,并且发现膜锚定的帕利珠单抗可以防止转染细胞中的感染,分别减少了99.7%和89.6%的体外和体内的RSVF。最后实验表达一种锚定的高亲和力的RSV抗体(RSVaVHH和sVHH)证明了RSV aVHH而不是RSV sVHH可以在转染后7天内显著抑制RSV,并且证明了RSV aVHH在肺中可以至少存在28天。这一研究表明在肺部表达膜锚定的中和抗体是一种有前途的肺部预防病毒的方法。
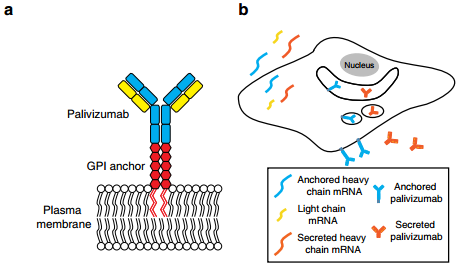
Tiwari P M,Vanover D, et al. Engineered mRNA-expressed antibodies prevent respiratory syncytial virus infection[J]. Nature Communications, 2018.
DOI:10.1038/s41467-018-06508-3
https://www.nature.com/articles/s41467-018-06508-3
7. JACS:细胞中酪氨酸磷酸酶和底物相互作用的蛋白质组学鉴定
蛋白质酪氨酸磷酸酶(PTPs)在细胞信号通路中扮演着重要的角色,但是在活细胞中识别未知的PTPs仍然是很大挑战。Tang等人合成了一系列以酪氨酸为基础的PTP抑制剂,其特点是可以在具有扩展遗传密码的细胞中对基质蛋白进行位点的特异性编码。实验通过对化学反应性的研究确定了最优活性氨基酸探针。以HER2为例,实验首次提供了在活的人类细胞中HER2y 1023和SHP2交联的直接证据。此外,利用蛋白质组学分析发现PTP1B是一种新型的HER2磷酸酶,这可能有助于解释PTP1B在治疗HER2阳性乳腺癌中所起的作用。
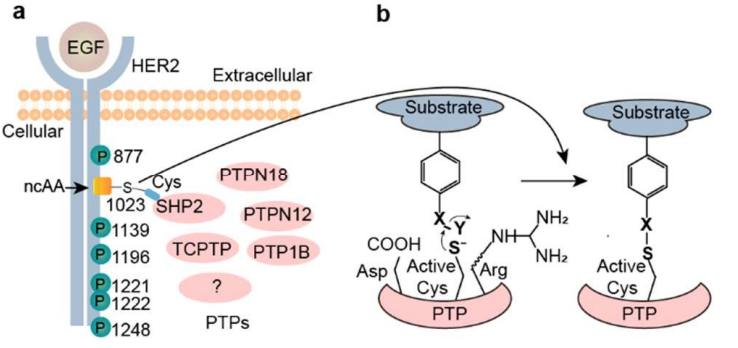
Tang H,Dai Z, et al. Proteomic identification of protein tyrosine phosphatase andsubstrate interactions in living mammalian cells by genetic encoding of irreversible enzyme inhibitors[J]. Journal of the American Chemical Society,2018.
DOI:10.1021/jacs.8b06922
https://pubs.acs.org/doi/10.1021/jacs.8b06922
8. JACS:一锅法合成介孔硅材料用于抗菌
Dubovoy等人合成了新型的介孔硅材料用于作为抗菌药物的输送系统(DDS)。该材料具有高的密度、宽的孔隙通道以及高的表面积。通过药物释放研究表明,在没有对材料进行额外的表面修饰的情况下,该材料可以对BAC实现控制释放。并且这种释放在酸性(pH 4.0、5.0、6.5)和中性(pH 7.4)溶液中的机制有着显著的差异。微生物化验结果表明,这一材料在合适的浓度下会使得金黄色葡萄球菌和沙门氏菌的活性明显下降。这一发现将有助于扩大BAC作为消毒杀菌剂的使用范围和潜力。
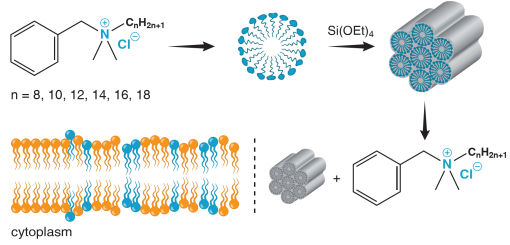
Dubovoy V,Ganti T, et al. One-Pot Hydrothermal Synthesis of Benzalkonium-Templated Mesostructured Silica Antibacterial Agents[J]. Journal ofthe American Chemical Society, 2018.
DOI:10.1021/jacs.8b04843
https://pubs.acs.org/doi/10.1021/jacs.8b04843
9.AM综述:DNA折纸纳米材料用于药物体内递送
近几十年来,为有效的药物输送而设计的新型纳米材料如雨后春笋。随着DNA纳米技术被逐渐开发出来,用于构建复杂的三维纳米结构和人工分子装置来在纳米尺度上操作,从而可以产生各种多样化的功能和多领域应用。特别是,DNA-折纸纳米材料具有合理设计的尺寸和精确的空间定位性以及显著的生物相容性,是一类很好的药物递送载体材料。Jiang总结了最近成功的利用自组装DNA-折纸纳米材料作为药物载体的工作,并且讨论了这一领域所面临的机遇和挑战。
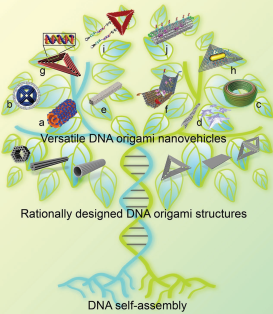
Jiang,Q., Liu, S.L. et al. Rationally Designed DNA-Origami Nanomaterials for Drug Delivery In Vivo. Advanced Materials, 2018.
DOI:10.1002/adma.201804785
https://doi.org/10.1002/adma.201804785











