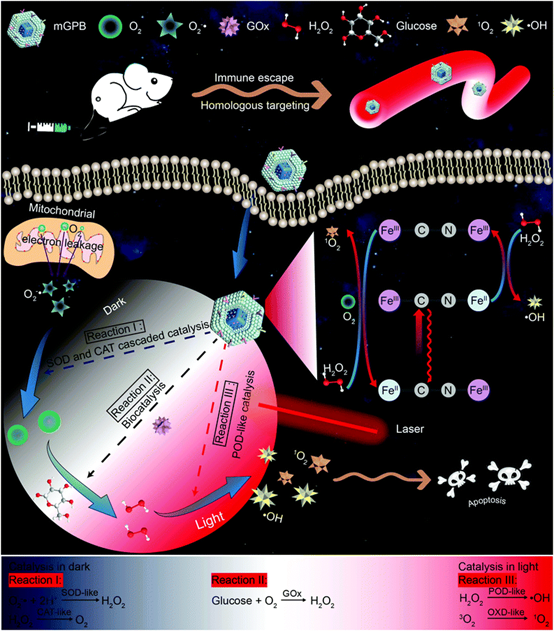
纳米酶已广泛用于生物医学,特别是在肿瘤治疗中。但是,肿瘤微环境(TME)中H2O2的供应不足以及体内纳米酶的不受控制的催化活性限制了它们的实际应用。因此,武汉大学张先正课题组提出了一种暗/光中继策略,以实现在暗反应阶段实现足够的H2O2供应,并通过远程光控制选择性地执行所需的催化活性,以产生有毒的活性氧(ROS)从而杀死肿瘤。肿瘤膜伪装和空心介孔普鲁士蓝(mGPB)装载葡萄糖氧化酶(GOx)纳米系统旨在利用膜的同源聚集靶向肿瘤组织。从空心介孔普鲁士蓝(HMPB)产生的超氧化物歧化酶(SOD)和类过氧化氢酶(CAT)活性的级联催化有效地将内源性O2−˙催化为O2,这有助于葡萄糖氧化分解,从而通过负载的GOx产生H2O2。此外,发现mGPB纳米粒子在其他光依赖的双重催化特性的作用下,在近红外光照射下利用过氧化氢生成˙OH 和1O2,起着过氧化物酶(POD)和氧化酶(OXD)的作用。通过暗/光中继催化,成功地克服了TME中有限的H2O2供应,并实现了精确的ROS生成,在小鼠异种移植模型中显示出显着的肿瘤抑制作用。
Chen, Y.; Li, Z.-H.; Hu, J.-J.; Peng, S.-Y.; Rong, L.; Sun, Y.; Zhang, X.-Z., Remote-controlled multi-enzyme system for enhanced tumor therapy via dark/light relay catalysis. Nanoscale Horizons 2019.
DOI: 10.1039/c9nh00583h
https://pubs.rsc.org/en/content/articlelanding/2019/nh/c9nh00583h#!divAbstract


















