膜蛋白和脂质协同发展并产生共调节作用,内向整流钾离子通道Kir(Inward rectifier potassium channels)通常被离子性脂质中K+传导通路中特有的膜激活,并且需要水的帮助。为了更好的理解Kir通道的活化过程,德州理工大学Benjamin J. Wylie等报道了通过ss NMR,钾外排试验,Förster共振能量转移(FRET)等方法对KirBac 1.1中的突变进行研究。
本文要点:
作者发现,在I131C稳定性突变体中,当加入双磷脂酰甘油CL(cardiolipin),存在阴离子脂质的通道展现出更高活性。当向Q中引入三个R会使使蛋白质失活,在ss NMR实验中发现,脂质和蛋白质之间的相互作用导致TQ突变并产生通道活性的大幅度降低。Water-edited ss NMR实验中进一步发现TQ突变体具有更好的整体暴露现象,但是离子通道对水的反应性降低,这和通道的闭合状态情况类似。
以上实验展示了水在KirBac1.1通道激活状态中起到选择性过滤作用。以上结果展现了脂质通过协同胞质结构域微单元的旋转进行结合,并通过内部多重盐桥亚组分稳定。本文中的发现展现了膜蛋白的广谱变化过程,包括脂类-蛋白相互作用、域重排、水辅助扩散等过程。

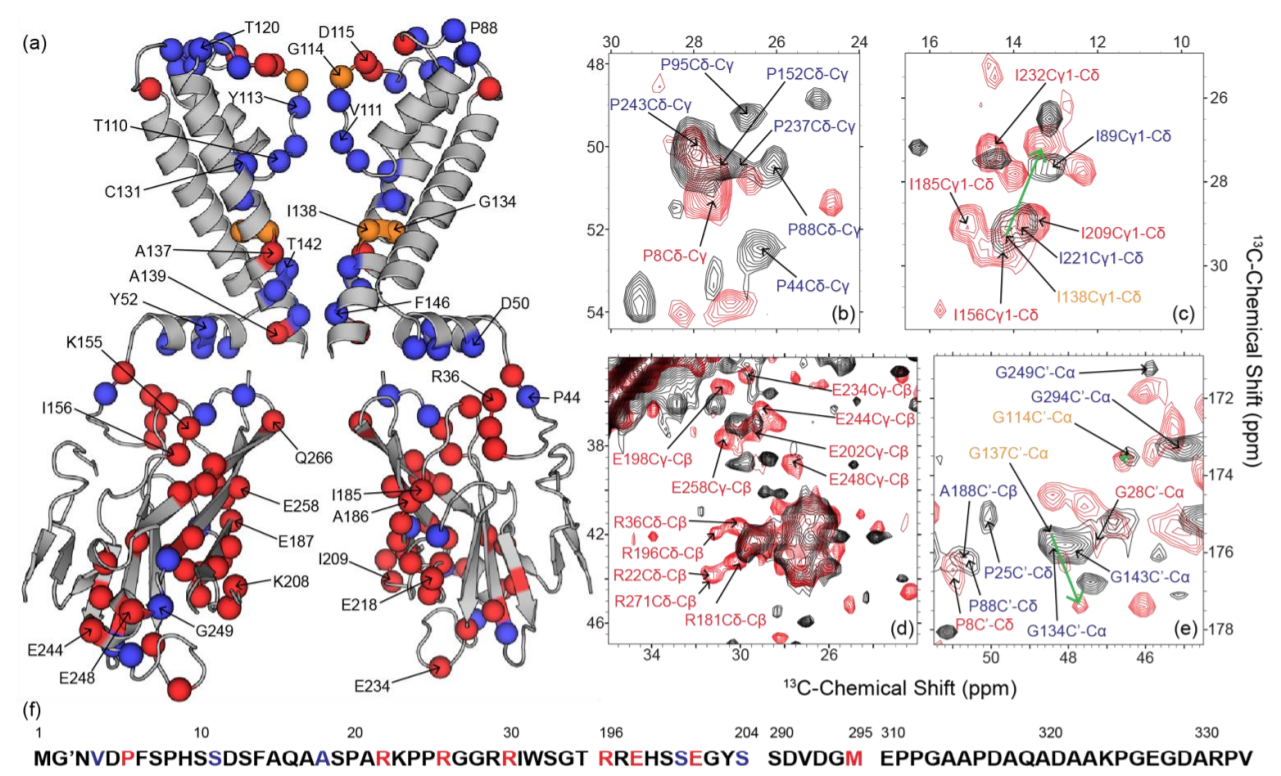
参考文献
Collin G. Borcik, Derek B. Versteeg, reza amani, Maryam Yekefallah, Nazmul H. Khan, and Benjamin J. Wylie*
The Lipid Activation Mechanism of a Transmembrane Potassium Channel, J. Am. Chem. Soc. 2020
DOI:10.1021/jacs.0c01991
https://pubs.acs.org/doi/10.1021/jacs.0c01991


















