细胞外囊泡(EVs)在疾病治疗和药物递送方面具有广阔的应用潜力。然而,如何实现EVs的准确药物释放以及EVs与药物在靶组织中的协同治疗效果仍具有相当的挑战性。北京理工大学谢海燕教授报道了一种工程化自激活的光-EVs,并将其用于协同三模态抗癌治疗。
本文要点:
(1)M1巨噬细胞来源的EVs (M1 EVs)可同时负载双[2,4,5-三氯-6-(戊氧羰基)苯基]草酸酯(CPPO)、Ce6和前药Dox-EMCH。给药后,由于M1 EVs具有肿瘤归巢能力,因此该M1 EVs系统能够主动靶向肿瘤细胞,并且可将M2重极化为M1巨噬细胞,因此其不仅表现出了免疫治疗作用,还能够产生H2O2。
(2)H2O2和CPPO之间的反应能够产生激活Ce6的化学能,随后既可以产生用于成像的化学发光,也能够产生用于光动力治疗(PDT)的单线态氧(1O2)。同时,1O2诱导膜破裂可以实现Dox-EMCH的释放,其在被激活后可以穿透至肿瘤深部的乏氧区。实验结果表明,免疫治疗、PDT和化疗产生的协同作用可以产生强大的抗癌效果,在对抗癌症方面具有很好的应用前景。
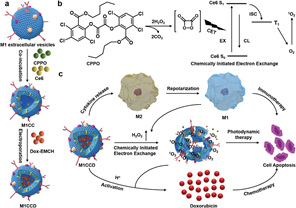
Jingjing Ding. et al. Self-Activatable Photo-Extracellular Vesicle for Synergistic Trimodal Anticancer Therapy. Advanced Materials. 2021
DOI: 10.1002/adma.202005562
https://onlinelibrary.wiley.com/doi/10.1002/adma.202005562



















