在T细胞反应有限的实体瘤中克服对免疫检查点抑制剂治疗的先天性或适应性抵抗仍然是一个挑战。越来越多的证据表明,表观遗传改变,特别是DNA甲基转移酶和免疫抑制腺苷的过表达,是T细胞激活的主要障碍。在此,武汉大学Zhi‐Jun Sun、西南大学Zhigang Xu等人合理设计了一种肿瘤微环境(TME)激发的前药纳米胶束(AOZN),它由表观遗传调节剂γ-谷维素(Orz)、腺苷抑制剂α、β -亚甲基腺苷5 '二磷酸(AMPCP)和GSH可激活交联剂组成。
本文要点:
1)高谷胱甘肽氧化还原触发Orz和AMPCP在TME中的释放。释放的Orz作为DNA甲基转移酶抑制剂,上调gasdermin D (GSDMD)的表达,AMPCP通过增加ATP水平将procaspase‐1转化为活性caspase‐1。在肿瘤细胞中,活性caspase‐1可诱导GSDMD分裂并诱导细胞焦亡。
2)研究还证明Orz和AMPCP在对抗免疫抑制TME时可能具有协同作用。
3)此外,Orz增强了程序性死亡配体1 (PD-L1)的表达,并使肿瘤对抗PD-L1治疗敏感。
综上所述,AOZNs纳米制剂极大地改善了Orz的疏水性,具有安全、经济、易获得和有效抑制肿瘤生长、提高PD‐L1反应率和延长B16F10黑色素瘤荷瘤小鼠模型生存期的优点。因此,AOZNs为增强癌症免疫治疗提供了一个有前景的策略。
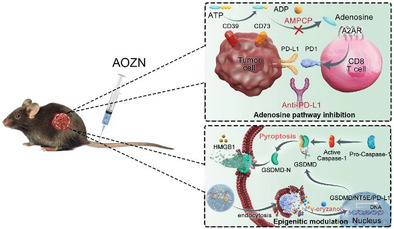
Honggang Xiong, et al. Inspired Epigenetic Modulation Synergy with Adenosine Inhibition Elicits Pyroptosis and Potentiates Cancer Immunotherapy, Adv. Funct. Mater., 2021.
DOI: 10.1002/adfm.202100007
https://doi.org/10.1002/adfm.202100007


















