临床上,抑制细菌感染和过度炎症是改善伤口治疗的关键步骤。西北工业大学戴亮亮副教授、重庆大学蔡开勇教授和刘鹏副教授设计了一种可被近红外(NIR)光激活的脱氧核糖核酸酶(DNase)-一氧化碳(CO)@介孔聚多巴胺纳米颗粒(MPDA NPs),它可以有效地消除耐甲氧西林金黄色葡萄球菌(MRSA)的生物膜和实现抗炎应用。
本文要点:
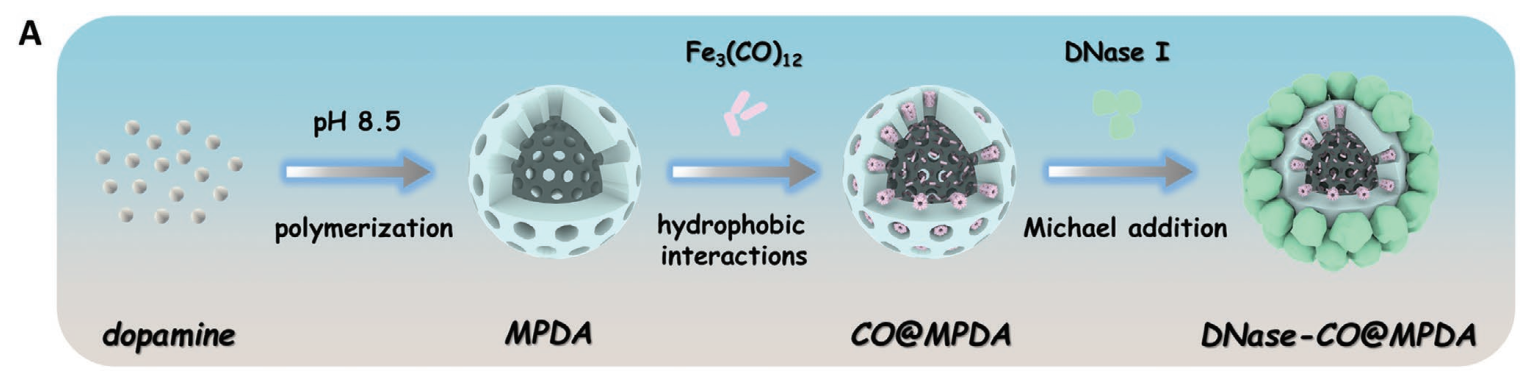
(1)实验首先将热敏释放CO的供体FeCO封装到MPDA NPs中,然后将脱氧核糖核酸酶I(DNase I)共价固定在MPDA NPs表面。DNA酶I可以降解生物膜中的细胞外DNA,破坏生物膜的致密性。在近红外照射下,DNase CO@MPDA NPs具有强大的光热能力,同时可进一步触发杀菌的CO气体的按需递送,并使其充分渗透到受损的生物膜中。最终,在DNase I和CO气体增强光热治疗的协同作用下,MPDA NPs可以实现有效的MRSA生物膜消除。
(2)与此同时,由于释放的CO具有抗炎性能,DNase-CO@MPDA NPs在NIR光刺激下治疗伤口时所产生的炎症反应也同时得到了缓解。研究结果表明,可被NIR光激活的DNase-CO@MPDA NPs能够有效加速耐MRSA生物膜感染的皮肤伤口的愈合过程。综上所述,这种光学治疗策略在治疗MRSA生物膜和随之而来的炎症所引起的临床问题方面具有巨大的治疗潜力。
Zhang Yuan. et al. Near-Infrared Light-Activatable Dual-Action Nanoparticle Combats the Established Biofilms of Methicillin-Resistant Staphylococcus aureus and Its Accompanying Inflammation. Small. 2021
DOI: 10.1002/smll.202007522
https://onlinelibrary.wiley.com/doi/10.1002/smll.202007522



















