饥饿治疗是一种通过调节葡萄糖代谢来抑制肿瘤生长的治疗策略。然而,肿瘤细胞的快速增殖会诱导产生乏氧的肿瘤微环境(TME),引起血管异构化而限制饥饿的效果。有鉴于此,澳门大学王瑞兵教授将葡萄糖氧化酶(GOx)诱导的饥饿治疗和乏氧激活的基因治疗相结合,开发了一种“双锁型”超分子纳米药物系统以用于实现癌症的协同治疗。
本文要点:
(1)实验将主-客体相互作用(可介导纳米组装形成)和乏氧激活的启动子作为两个锁,并将葡萄糖氧化酶(GOx)和治疗性质粒(RTP801::p53)负载于超分子金纳米囊泡(Au NVs)内。
(2)当Au NVs被癌症特异性活性氧(ROS)解离后,GOx会被释放以消耗葡萄糖和氧气,同时产生H2O2和诱导乏氧的TME,这也是触发有效载荷释放和启动子激活的两个关键。实验结果表明,这种实验超分子纳米药物在体内外具有很好的肿瘤抑制作用。
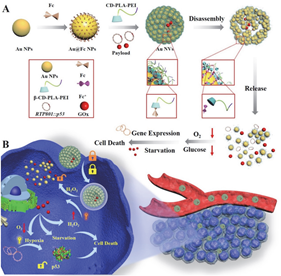
Ludan Yue. et al. Supramolecular nanovesicles for synergistic glucose starvation and hypoxia-activated gene therapy of cancer. Nanoscale. 2021
DOI: 10.1039/d1nr02159a
https://pubs.rsc.org/en/content/articlelanding/2021/nr/d1nr02159a#!divAbstract



















