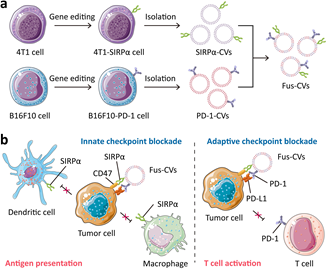
有效激活宿主免疫以对抗癌症已经发展成为一种有效的肿瘤治疗策略。然而,癌细胞会通过先天免疫效应和适应性免疫效应来抵抗宿主所产生的免疫反应。其中,肿瘤细胞上的CD47会通过与SIRPα发生相互作用而保护其免受巨噬细胞的吞噬,而PD-L1也会与其受体PD-1发生相互作用,进而抑制T细胞介导的肿瘤杀伤。深圳湾实验室饶浪研究员、南方医科大学Guang-Tao Yu和新加坡国立大学陈小元教授构建了对SIRPα变体和PD-1具有高亲和性的可编程基因型融合细胞囊泡(Fus-CVs)以解决上述两种机制。
本文要点:
(1)研究表明,利用Fus-CVs对CD47和PD-L1进行双重阻断能够显著增强巨噬细胞对于癌细胞的吞噬效果,促进抗原提呈,激活抗肿瘤T细胞免疫。此外,Fus-CVs的双特异性靶向设计也使其对肿瘤细胞具有更好的靶向性,而对其他细胞的靶向性更低,因此能够在减少全身副作用的同时提高治疗效果。
(2)在恶性黑色素瘤和乳腺癌模型中,实验证明了Fus-CVs可通过抑制术后肿瘤的复发和转移以显著提高模型动物的总体生存率。此外,Fus-CVs也能够通过基因工程以用于蛋白展示。综上所述,这一研究所开发的Fus-CVs是一种具有广阔发展前景的多靶点免疫检查点封锁治疗平台。
Qian-Fang Meng. et al. Genetically Programmable Fusion Cellular Vesicles for Cancer Immunotherapy. Angewandte Chemie International Edition. 2021
DOI: 10.1002/anie.202108342
https://onlinelibrary.wiley.com/doi/10.1002/anie.202108342



















