人α -1抗胰蛋白酶(A1AT)是一种天然的丝氨酸蛋白酶抑制剂,可以保护过度蛋白酶活化造成的组织损伤,可作为一种治疗A1AT缺陷患者的补充疗法。但A1AT容易氧化失活,且循环半衰期短。此前,还没有一种方法可以有效地保护治疗性蛋白在体内免受氧化损伤。有鉴于此,中国科学院生物物理研究所的Feng Wang、北京大学的吕华等研究人员,发现硒多肽与α-1抗胰蛋白酶(A1AT)的位点特异性偶联可增强抗氧化性和药理学特性。
本文要点
1)研究人员开发了一种新的生物相容性硒多肽,并将其与A1AT位点特异性偶联。
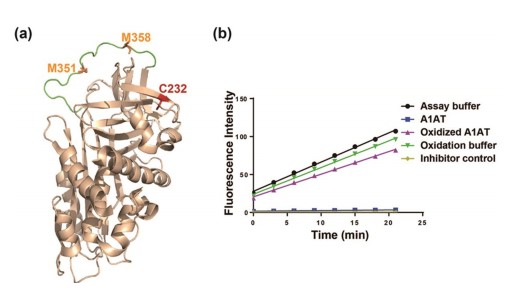
2)偶联后的A1AT完全保留了对中性粒细胞弹性蛋白酶的抑制活性,并增强了抗氧化能力,延长了血清半衰期,对急性肺损伤小鼠模型具有持久的保护作用。
本文研究结果表明,将A1AT与人工设计的硒多肽偶联是改善其药理特性的一种可行策略,这可能进一步应用于多种氧化敏感的生物治疗药物中。
参考文献:
Chao Dong, et al. Site-specific Conjugation of a Selenopolypeptide to Alpha-1-antitrypsin Enhances Oxidation Resistance and Pharmacological Properties. Angewandte Chemie, 2020.
DOI:10.1002/anie.202115241
https://onlinelibrary.wiley.com/doi/10.1002/anie.202115241


















