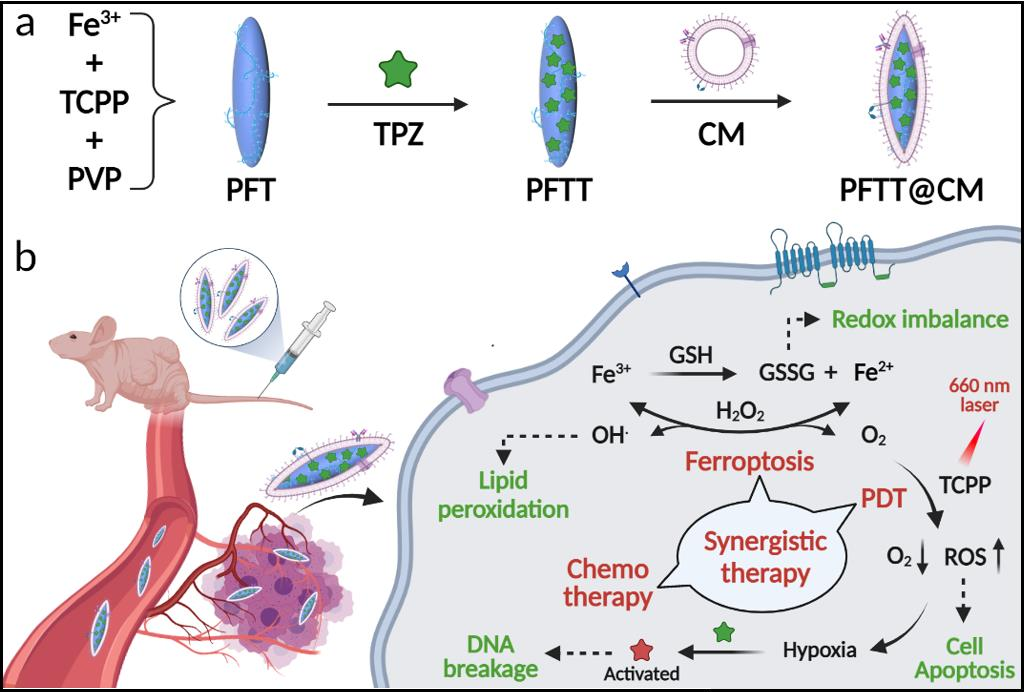
设计和开发基于肿瘤微环境(TME)的纳米药物以有效地治疗癌症具有重要的应用价值。南方医科大学陈金香教授和孙斌副教授构建了Fe-TCPP(TCPP=四(4-羧苯基)卟啉)的纳米金属有机骨架(NMOF),利用其负载乏氧激活的前药tirapazamine(TPZ),并在其表面包被癌细胞膜(CM)以形成纳米复合材料PFTT@CM。
本文要点:
(1)由于被同源癌细胞膜功能化,因此PFTT@CM能够躲避免疫清除,并优先聚集在肿瘤部位。被癌细胞内化后,PFTT@CM可通过Fe3+与内源性谷胱甘肽(GSH)和过氧化氢(H2O2)发生氧化还原反应和类芬顿反应,进而被TME激活,以促进GSH的消耗和•OH、O2的产生,引发铁死亡的同时显著提高光动力治疗(PDT)的效果。
(2)研究表明,TCPP介导的PDT过程会消耗氧气,从而加重肿瘤乏氧,进一步激活肿瘤化疗前药TPZ。因此,被TME为驱动的PFTT@CM纳米平台不仅具有调节TME的能力,而且也能实现级联协同治疗,有效地抑制癌细胞增殖。综上所述,该多模态纳米平台能够为设计对TME响应的治疗策略以增强协同治疗效果和促进癌症纳米药物的开发提供新的借鉴。
Wei-Lun Pan. Microenvironment-driven sequential ferroptosis, photodynamic therapy, and chemotherapy for targeted breast cancer therapy by a cancer-cell-membrane-coated nanoscale metal-organic framework. Biomaterials. 2022
https://www.sciencedirect.com/science/article/pii/S0142961222000886



















