乏氧是大多数实体瘤的典型和显著特征之一,其会加重肿瘤的侵袭和转移性。,复旦大学附属中山医院黄备建、上海大学陈雨教授和向慧静副教授合成了乏氧激活、含偶氮键的喜树碱(CPT)前药(CPT2-Azo),然后将其固定在集成声敏剂的金属有机骨架(MOF NPs)的介孔中,从而设计了一种超声(US)/乏氧敏感的声化疗纳米前药。
本文要点:
(1)进入乏氧肿瘤微环境(TME)后,固定有CPT2-Azo的MOFs(MCA)结构会破裂,其负载的CPT2-Azo前药会从MOF NPs中释放出来。在US驱动下,这种声化疗纳米前药不仅通过将氧转化为细胞毒性活性氧(ROS)以实现声动力治疗(SDT),而且通过增加氧消耗以加重TME乏氧。加重的乏氧能起到正放大器的作用,促进CPT2-Azo的激活和毒性化疗药物(CPT)的可控释放,以弥补SDT治疗效果的不足。
(2)体内外实验结果证实,连续SDT和肿瘤乏氧激活的超声化疗能够增强抗肿瘤疗效,导致显著的细胞死亡,有效抑制体内肿瘤生长。综上所述,该研究工作能够为开发乏氧激活的声化疗纳米前药提供新的见解。该药物能够利用SDT的副作用,即TME的乏氧状态来启动化疗,从而可以实现与常规SDT相比的更好的治疗结果。
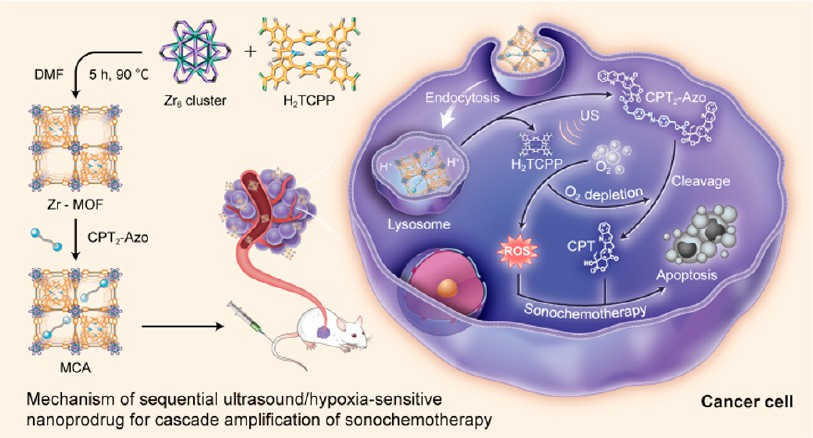
Fan Zhuang. et al. Sequential Ultrasound-Triggered and Hypoxia-Sensitive Nanoprodrug for Cascade Amplification of Sonochemotherapy. ACS Nano. 2022
DOI: 10.1021/acsnano.1c09505
https://pubs.acs.org/doi/10.1021/acsnano.1c09505



















