肿瘤源性外泌体介导的系统性免疫抑制是免疫检查点封锁(ICB)治疗耐药性产生的重要原因。有鉴于此,苏州大学殷黎晨教授利用自适应血小板(PLT)药物细胞来介导实现对于外泌体抑制siRNA和抗PD-L1(aPDL1)的级联递送,从而协同增强抗肿瘤免疫。
本文要点:
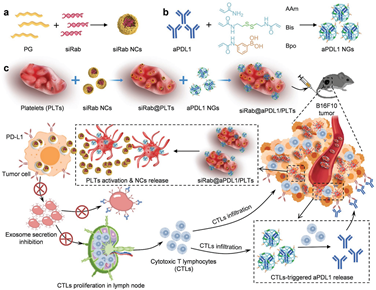
(1)在药物细胞中,由Rab27 siRNA(siRab)和膜穿透多肽组装而成的聚阳离子纳米复合物(NCs)被包裹在PLT的开放管状系统中,对细胞毒性T淋巴细胞(CTLs)响应的aPDL1纳米凝胶(NGs)则被共价连接在PLT表面。全身给药后,该药物细胞具有延长的血液循环周期,并能够主动地聚集到肿瘤中。随后,PLT会被激活以释放siRab NCs,从而有效地转染肿瘤细胞,使得Rab27a沉默,抑制外泌体的分泌。
(2)随后,免疫抑制会被解除,从而导致细胞毒性T细胞的激活、增殖和肿瘤浸润,并触发aPDL1释放。因此,表达PD-L1的外泌体竞争消耗aPDL1的能力会被最小化,从而实现对ICB的增敏。研究表明,siRab和aPDL1能够诱导强大的抗肿瘤免疫反应和免疫记忆以对抗同基因小鼠黑色素瘤。综上所述,该研究设计了一种仿生机制,有效解决了聚阳离子siRNA递送系统血液循环和细胞内化之间的矛盾,并为时空增强抗肿瘤免疫提供了一种新的方法。
Jing Yan. et al. Platelet Pharmacytes for the Hierarchical Amplification of Antitumor Immunity in Response to Self-Generated Immune Signals. Advance Materials. 2022
DOI: 10.1002/adma.202109517
https://onlinelibrary.wiley.com/doi/10.1002/adma.202109517



















