以细胞内装置为靶点的蛋白质药物具有广阔的治疗潜力,但由于缺乏有效的胞质递送技术,其临床应用仍受到很大阻碍。现有的策略主要依赖于纳米载体或结合细胞穿透肽(CPPs),因此往往存在材料复杂性/毒性、缺乏细胞特异性和内溶酶体截留等缺点。有鉴于此,苏州大学殷黎晨教授设计了一种独特的无载体方法来介导实现不依赖于内吞且具有癌症选择性的蛋白胞质递送。
本文要点:
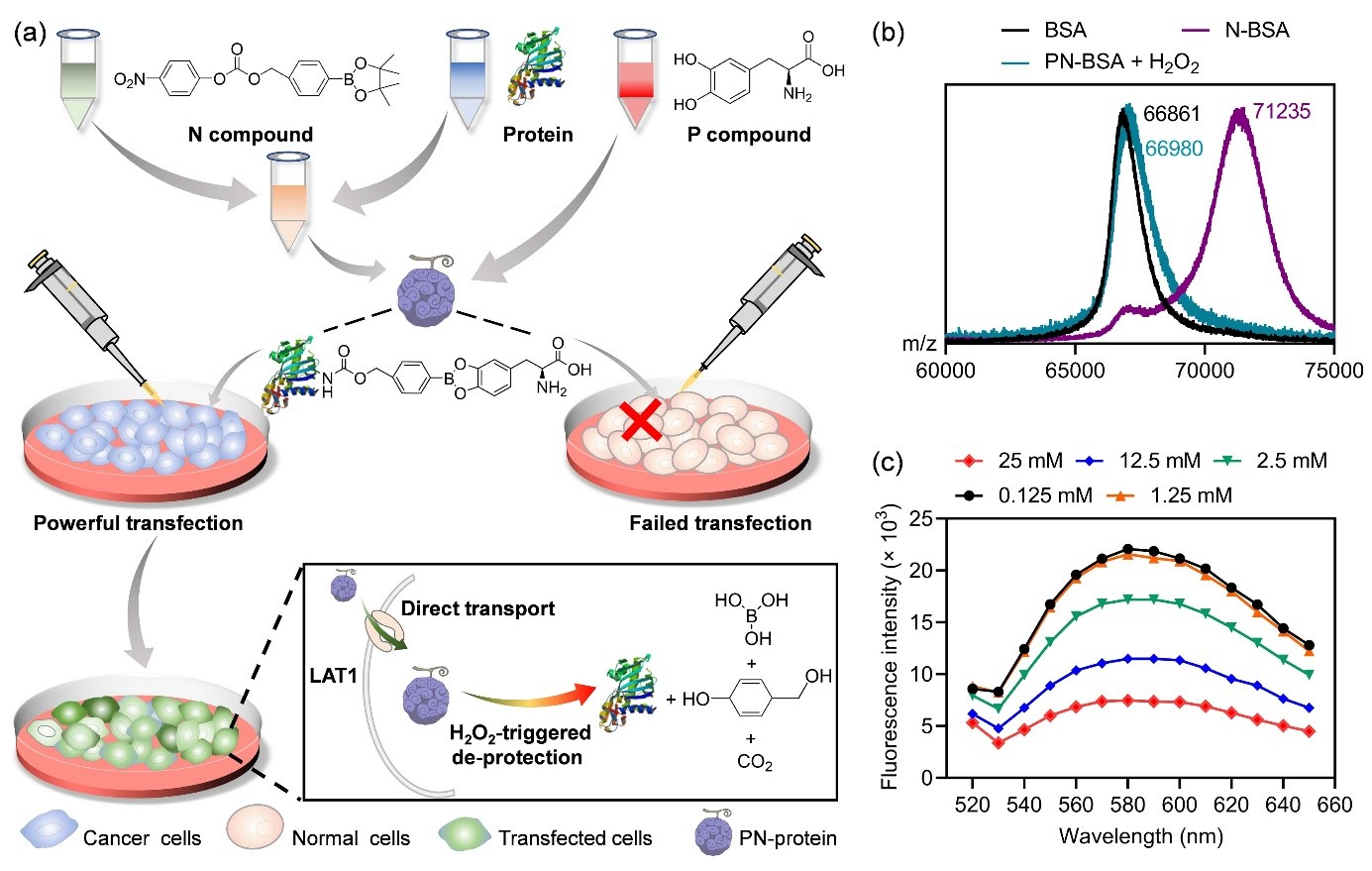
(1)实验以4-硝基苯- 4-(4,4,5,5-四甲基-1,3,2-二氧硼砂-2-基)碳酸苄酯为H2O2响应结构域,以3,4-二羟基- L-苯丙氨酸为L型氨基酸转运体1 (LAT1)的底物,依次对蛋白质进行修饰。因此,该前蛋白可以通过细胞膜上过表达的LAT1而被直接转运到肿瘤细胞中,进而绕过内吞作用和避免内溶酶体的截留。
(2)在细胞质中,过量产生的H2O2能够恢复蛋白质的结构和活性。基于这项技术,多种蛋白质能够以高效地进入肿瘤细胞,包括毒素、酶、CRISPR-Cas9核糖核蛋白和抗体等。研究表明,静脉注射皂草素前蛋白后能够在4T1荷瘤小鼠体内产生较强的抗癌作用,并且不会引发全身毒性。综上所述,该研究开发了一种简单、多功能的蛋白质前平台,有利于进一步推动蛋白质药物的发展。
Ziyin Zhao. et al. Endocytosis-independent and Cancer-selective Cytosolic Protein Delivery via Reversible Tagging with LAT1 substrate. Advanced Materials. 2022
DOI: 10.1002/adma.202110560
https://onlinelibrary.wiley.com/doi/abs/10.1002/adma.202110560



















