具有多重模拟酶活性的氧化还原纳米酶能够与免疫疗法产生协同作用,进而在实现安全高效的癌症治疗方面表现出广阔的应用前景。然而,这种时空精确的免疫反应也面临着脱靶不良反应和治疗反应不足等挑战。有鉴于此,南洋理工大学赵彦利教授开发了一种肿瘤细胞膜包覆的氧化还原纳米酶(CMOR@4T1),并将其用于近红外二区(NIR-II)光热免疫治疗。
本文要点:
(1)CMO-R@4T1以铜掺杂的MoOx(CMO)纳米酶为内核,其表面包覆了肿瘤细胞衍生的融合膜,膜壳内固定有免疫刺激物。除了具有增强的肿瘤积累性能以外,该纳米酶还可以通过产生活性氧和削弱抗氧化机制以对肿瘤细胞造成氧化损伤。在NIR-II光照射下,CMO-R@4T1也能够通过产生光热效应以实现肿瘤根除和触发免疫原性细胞死亡,并释放激动剂引发免疫激活。
(2)实验结果表明,这种可控的治疗模式能够加强对全身原发肿瘤的消融,抑制肿瘤的远处转移,并诱导产生长期的免疫记忆。综上所述,该研究利用缺陷工程的优势构建了一种细胞膜伪装的纳米酶,能够用于癌症的靶向光学免疫治疗。
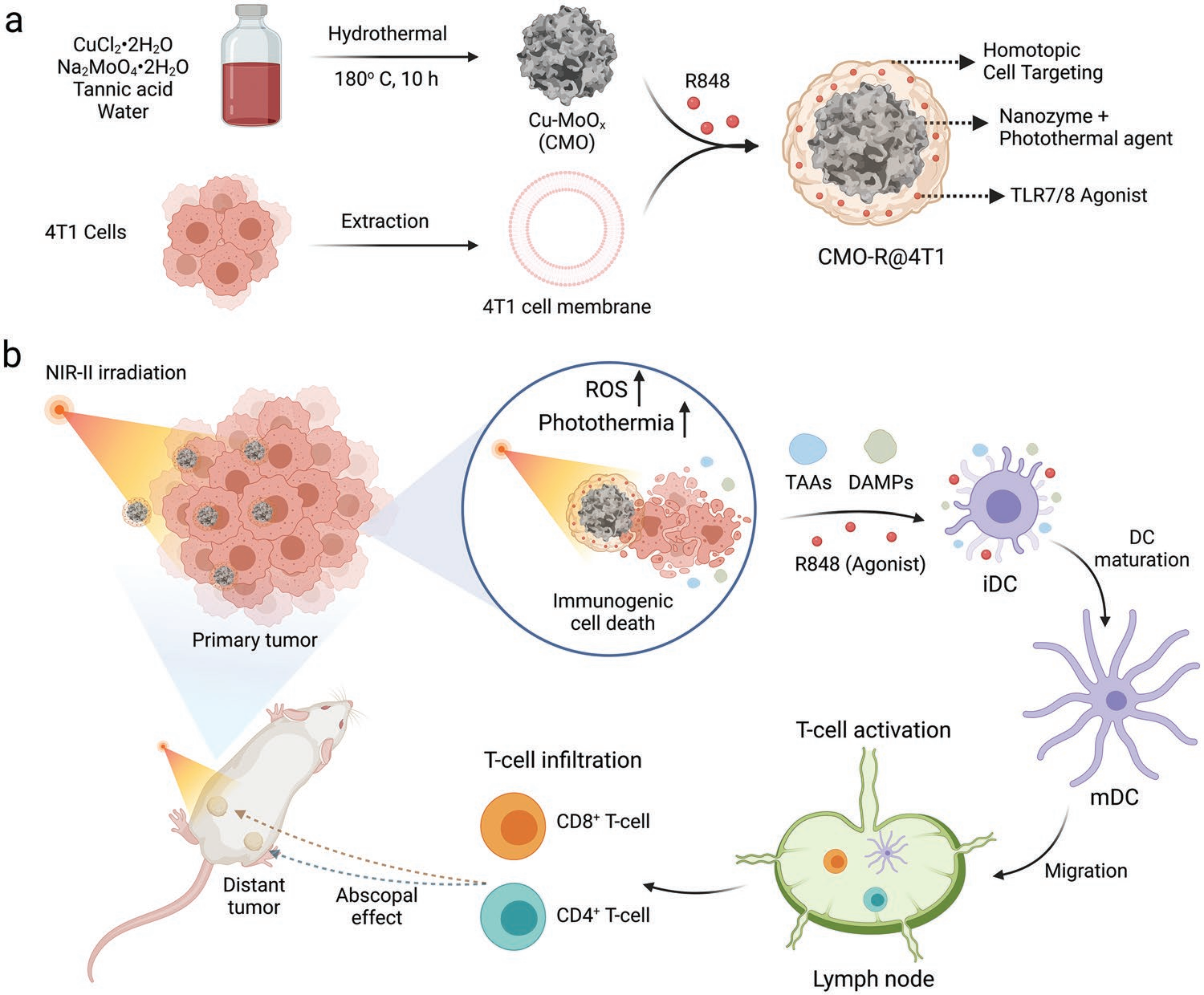
Deblin Jana. et al. A Defect-Engineered Nanozyme for Targeted NIR-II Photothermal Immunotherapy of Cancer. Advanced Materials. 2022
DOI: 10.1002/adma.202206401
https://onlinelibrary.wiley.com/doi/10.1002/adma.202206401



















