人工酶已被证明具有多种治疗多种恶性肿瘤的作用,但其抗肿瘤性能仍会受到非选择性催化、原子利用效率低和脱靶毒性等问题的严重影响。苏州大学陈华兵教授、邓益斌教授、缪丽燕教授和Jing Tao在单个白蛋白纳米笼中构建了类过氧化物酶生物矿化碱式碳酸铜(II)纳米晶体(CuCH-NCs),并将其作为pH激活的前酶以实现对侵袭性三阴性乳腺癌(TNBCs)的肿瘤选择性协同化学动力学/化学-免疫治疗。
本文要点:
(1)CuCH-NCs能够实现对pH敏感的Cu2+释放。Cu2+可在谷胱甘肽(GSH)的作用下还原为Cu+物种,进而催化H2O2产生羟基自由基(·OH),引起细胞的化学动力学损伤,并同时激活无毒的双硫仑转化为细胞毒性复合物,以通过阻断细胞增殖和放大细胞凋亡等方式产生选择性化疗损伤。研究发现,CuCH-NCs具有较强的肿瘤靶向能力,且穿透深度较深,可通过协同的化学动力学/化学治疗对乳腺原位肿瘤产生较好的疗效,且具有良好的体内安全性。
(2)此外,CuCH-NCs在与双硫仑联合作用时会引起显著的免疫原性细胞死亡效应,上调PD-L1的表达,从而与抗PD-L1抗体相协同以激活适应性免疫和先天免疫,缓解免疫抑制,最终对原发性和转移性TNBC产生较强的抗肿瘤作用。综上所述,该研究能够为开发智能型、具有高性能的前酶协同治疗策略以对抗侵袭性癌症提供新的见解。
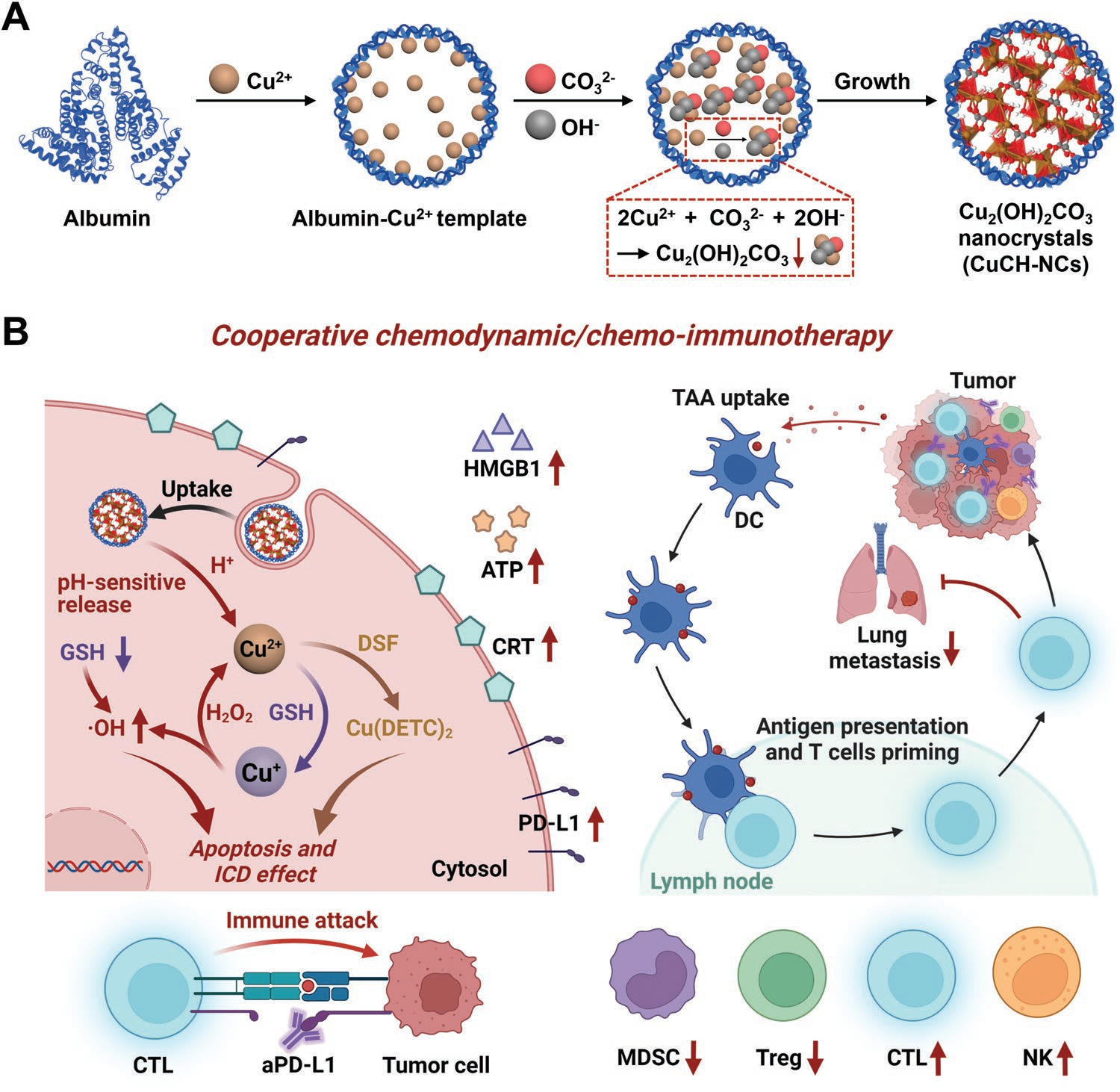
Ting Li. et al. A pH-Activatable Copper-Biomineralized Proenzyme for Synergistic Chemodynamic/Chemo-Immunotherapy against Aggressive Cancers. Advanced Materials. 2023
DOI: 10.1002/adma.202210201
https://onlinelibrary.wiley.com/doi/10.1002/adma.202210201



















