焦亡是程序性细胞死亡的一种促炎形式,会导致细胞内容物的释放和免疫反应的激活。然而,GSDME(一种焦亡执行蛋白)会在许多癌症中受到抑制。有鉴于此,中山大学帅心涛教授、肖泽聪研究员和Bo Li构建了一种新型纳米脂质体(GM@LR),并利用其将表达GSDME的质粒和羰基锰(MnCO)共递送到TNBC细胞中。
本文要点:
(1)在有H2O2存在的情况下,MnCO会生成Mn2+和CO。CO激活的caspase-3会裂解表达的GSDME,从而将4T1细胞的凋亡转化为焦亡。与此同时,Mn2+能够通过激活STING信号通路以促进树突状细胞(DCs)成熟。瘤内成熟DCs比例的增加会导致细胞毒性淋巴细胞的大量浸润,进而产生强大的免疫反应。
(2)此外,Mn2+也可用于实现磁共振成像(MRI)指导下的转移检测。综上所述,该研究开发的GM@LR纳米药物可通过焦亡和STING激活联合的免疫治疗实现对肿瘤生长的有效抑制。
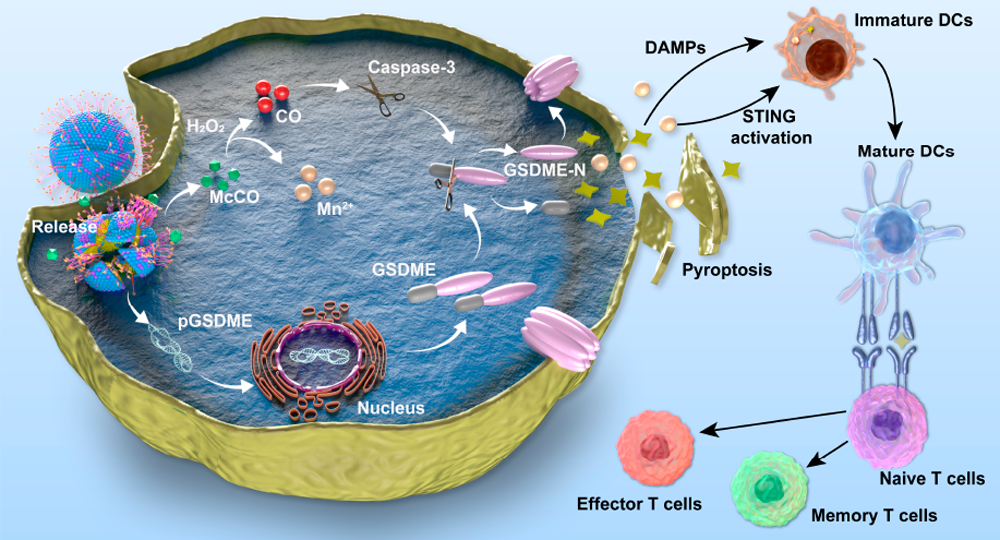
Huihai Zhong. et al. Nanodrug Augmenting Antitumor Immunity for Enhanced TNBC Therapy via Pyroptosis and cGAS-STING Activation. Nano Letters. 2023
DOI: 10.1021/acs.nanolett.3c01008
https://pubs.acs.org/doi/10.1021/acs.nanolett.3c01008



















