免疫检查点抑制剂(ICI)是一种治疗三阴性乳腺癌(TNBC)的潜在方法。然而,糖酵解高(TNBC细胞的标志)会驱动肿瘤固有的PD-L1糖基化,并增强调节性T细胞功能,从而影响ICI的疗效。有鉴于此,重庆大学胡燕教授、罗忠教授和李孟桓教授构建了一种基于自组装的适配体-聚合物偶联物、可由肿瘤微环境激活的纳米组装体,并将其用于靶向递送葡萄糖转运蛋白1抑制剂BAY-876(DNA-PAE@BAY-876)以重塑免疫抑制性TME,从而增强ICI的治疗响应。
本文要点:
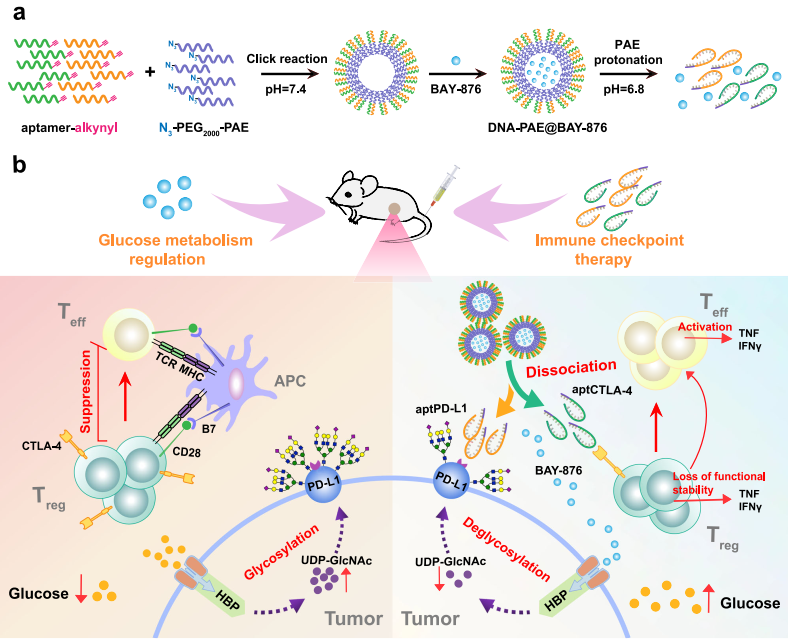
(1)实验合成了聚β-氨基酯(PAE)修饰的PDL1和CTLA-4拮抗适配体(aptPD-L1和aptCTLA-4),并将它们共组装成可负载BAY-876的超分子纳米组装体。研究发现,酸性肿瘤微环境会导致PAE发生质子化,并触发纳米组装体的解离,从而释放BAY-876和适配体。BAY-876能够选择性地抑制TNBC糖酵解,以剥夺尿苷二磷酸N-乙酰葡糖胺,并下调PD-L1糖基化,从而促进PD-L1识别aptPD-L1,以增强抗PD-L1治疗。
(2)与此同时,BAY-876治疗还可以提高对肿瘤内调节性T细胞(Tregs)的葡萄糖供应,使其重新到达免疫刺激状态,从而能够与aptCTLA-4介导的免疫检查点抑制相协同以有效消除Treg介导的免疫抑制。综上所述,该研究开发的DNA-PAE@BAY-876能够在TNBC临床前模型中有效地实现对免疫抑制性肿瘤微环境的重编程,为TNBC的临床免疫治疗提供了一种独特的新方法。
Xijiao Ren. et al. Inhibition of glycolysis-driven immunosuppression with a nano-assembly enhances response to immune checkpoint blockade therapy in triple negative breast cancer. Nature Communications. 2023
https://www.nature.com/articles/s41467-023-42883-2



















