gasdermin蛋白介导的细胞焦亡在肿瘤免疫治疗领域中具有巨大的应用潜力。然而,gasdermin蛋白低表达以及由非特异性细胞焦亡导致的全身毒性等问题仍会严重限制该策略的临床应用。有鉴于此,郑州大学陈真真教授和王永超研究员设计了一种合成生物学策略,将焦亡诱导质粒(pPHS)负载到锰(Mn)掺杂的碳酸钙纳米颗粒上,并包裹肿瘤源性细胞膜,构建了一种能够诱导肿瘤特异性焦亡的纳米平台M-CNP/Mn@pPHS。
本文要点:
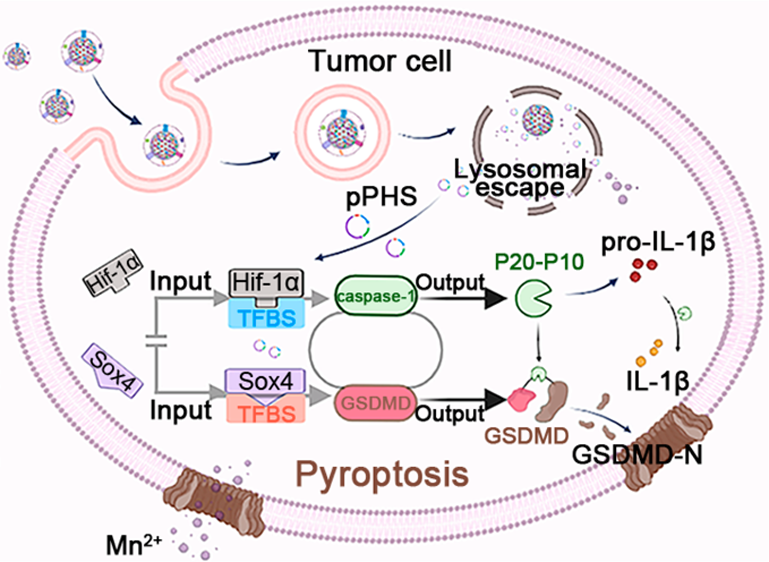
(1)M-CNP/Mn@pPHS具有良好的肿瘤靶向性。被肿瘤细胞内化后,MCNP/Mn@pPHS会在酸性内体环境中降解,使得质粒pPHS能够有效地逃逸内体。研究发现,以Hif-1α和Sox4为两个输入信号、以gasdermin D诱导的细胞焦亡为输出信号、根据“AND门电路”逻辑策略设计的pPHS能够触发肿瘤特异性细胞焦亡。只有在同时高表达Hif-1α和Sox4的细胞中,输出信号gasdermin D才会被表达。
(2)由于Hif-1α和Sox4均在肿瘤细胞中特异性表达,因此M-CNP/Mn@pPHS能够实现具有肿瘤特异性的gasdermin D表达,从而可引起细胞焦亡,触发有效的免疫反应,并且不会产生显著的全身毒性。实验结果表明,该纳米平台释放的Mn2+可通过刺激cGAS-STING通路进一步增强抗肿瘤免疫反应。因此,M-CNP/Mn@pPHS能够有效地抑制肿瘤生长,实现体内肿瘤消退(79.8%)。综上所述,该研究构建的基于逻辑“AND门电路”的gasdermin纳米平台能够诱导肿瘤特异性细胞焦亡,并且具有极低的全身毒性。
Xiaoxi Wang. et al. Logic “AND Gate Circuit”-Based Gasdermin Protein Expressing Nanoplatform Induces Tumor-Specific Pyroptosis to Enhance Cancer Immunotherapy. ACS Nano. 2024
DOI: 10.1021/acsnano.3c09405
https://pubs.acs.org/doi/10.1021/acsnano.3c09405



















