活性氧(ROS)介导的肿瘤细胞死亡是一种有效的抗癌策略。铜死亡是一种依赖于铜、由ROS介导的新型肿瘤治疗策略。然而,复杂的肿瘤微环境(TME)、较低的肿瘤特异性、较差的治疗效率以及缺乏成像能力等问题仍会限制现有铜死亡药物的治疗效果。有鉴于此,河南大学白锋教授和钟永教授以Au(III)四-(4-吡啶基)卟啉(AuTPyP)为配体,以铜离子(Cu2+)为节点,通过配位自组装策略设计了一种具有双响应性的二维金属有机框架(2D MOF)纳米诊疗药物。
本文要点:
(1)在酸性TME中,AuTPyP中的吡啶基质子化能够联合双重刺激和深穿透性超声(US)一起触发实现可控释放。此外,纳米药物的超薄结构(3.0 nm)也能够促进其释放过程。研究发现,释放出的Cu2+可通过消耗肿瘤中过表达的谷胱甘肽(GSH)而被还原为Cu+,从而不仅能够激活铁氧化还原蛋白1(FDX1)介导的铜死亡,也可以通过类芬顿反应催化肿瘤中过表达的过氧化氢(H2O2)转化为活性氧。
(2)与此同时,释放的AuTPyP能够与硫氧还蛋白还原酶发生特异性结合,以激活肿瘤细胞的氧化还原失衡。实验结果表明,这些治疗作用能够共同选择性地诱导线粒体空泡和肿瘤细胞死亡,并且不会损害正常细胞。荧光和磁共振成像(MRI)结果显示,该纳米诊疗药物能够靶向HeLa肿瘤,并且可以显著地增强化疗/铜死亡的自增强效应以及对肿瘤的抑制效率。综上所述,该研究工作阐明了多响应性纳米诊疗体系的可控自组装过程及其高特异性ROS调节功能在抗癌治疗领域中的应用潜力。
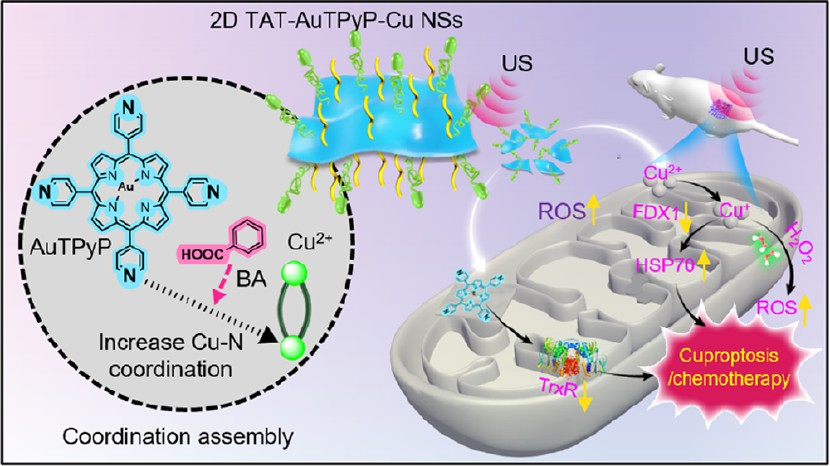
Jianshuai Bao. et al. Coordination Self-Assembled AuTPyP-Cu Metal−Organic Framework Nanosheets with pH/Ultrasound Dual-Responsiveness for Synergistically Triggering Cuproptosis-Augmented Chemotherapy. ACS Nano. 2024
DOI: 10.1021/acsnano.3c13225
https://pubs.acs.org/doi/10.1021/acsnano.3c13225



















