治疗性核酸,例如反义寡核苷酸、siRNA和mRNA,已被用于治疗和预防多种疾病。例如,已显示基于核酸的治疗可改善遗传性转甲状腺素介导的淀粉样变性和纯合子家族性高胆固醇血症患者的临床结果。此外,最近还开发了针对癌症和寨卡病毒的实验性核酸疫苗,并且针对 COVID-19 的核酸疫苗已获准用于临床。由于 mRNA 疫苗的开发速度比其他疫苗类型更快,因此基于核酸的疗法可以在控制大流行性疾病方面发挥重要作用。
尽管患者更喜欢口服剂型而不是注射剂,但核酸通常通过静脉内、肌肉内或皮下给药,因为胃肠道 (GI) 自然会阻止生物大分子的摄取。当口服给药时,核酸在摄入后迅速降解,从而限制细胞渗透并降低生物利用度。肠胃外给药方法能够快速全身吸收,并确保治疗到达接受大量血流的器官,例如肝脏、肺和肾脏。口服给药方法可以成为一种优选的全身摄取方法,并且还可以在胃肠道中进行靶向递送。
为了增强 GI 摄取、靶向特定器官、促进转染和或防止脱靶效应,基于核酸和其他大分子的药物通常转向渗透增强剂和专门设计的纳米颗粒。尽管如此,基于核酸的疗法仍然具有较低的口服生物利用度。之前的研究已经证明,口服给药的机器人注射药丸能够自动将药物注射到胃肠道内壁,能够以与皮下注射相当的剂量水平全身递送大分子蛋白质药物。然而,核酸的口服递送提出了额外的挑战,并且尚未使用这种方法进行证明。
鉴于此,麻省理工学院Giovanni Traverso、Robert Langer院士等人展示了通过口服胶囊将封装在支化聚合物纳米颗粒中的 mRNA 直接注射到胃粘膜下层的能力,绕过胃肠道中存在的天然屏障。并且使用猪和小鼠模型中蛋白质翻译的证据来确认给药 mRNA 的有效转染。成果发表在Matter上,Nicholas A. Peppas院士和陶伟对其进行评述。


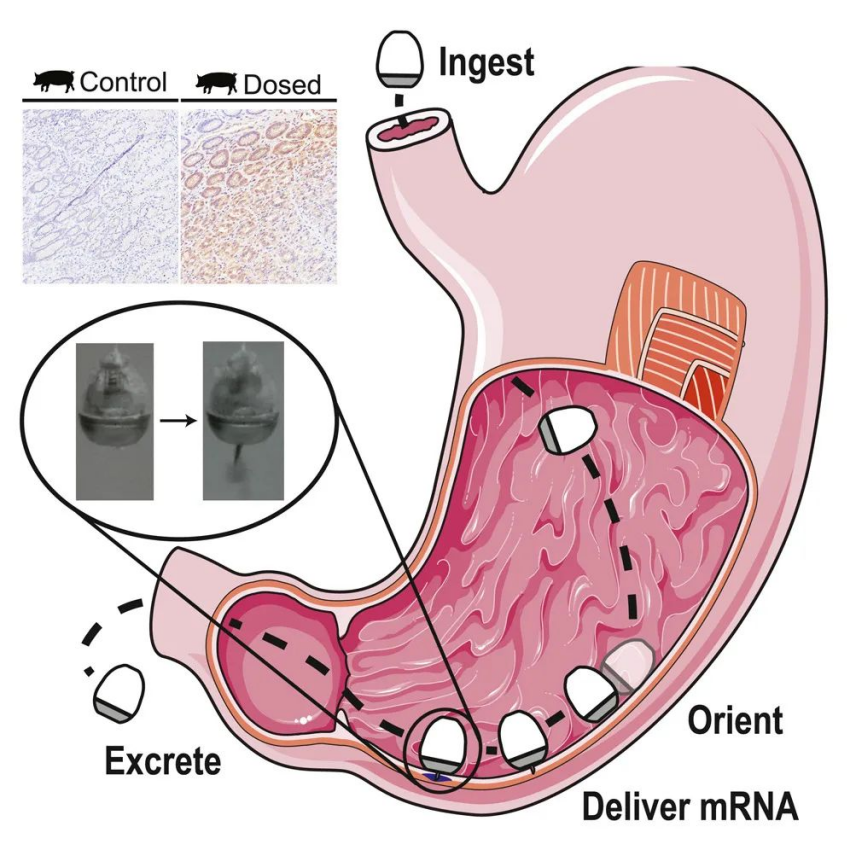
示意图
本文使用的药丸,称之为自定向毫米级施药器 (SOMA),能够通过组织注射将药物制剂直接输送到胃组织的血管层中,从而绕过胃肠道中的降解酶。为确保注射剂进入组织,而不是进入胃腔,该药丸利用独特的形状和密度分布来自主定向并可预测地面向胃壁。然后水合触发的致动器就会释放一个基于弹簧的注射机制,该机制将针头推入组织并将一团药物输送到胃粘膜下层,进而实现药物的胃部输送。本文的重点是优化 SOMA 系统,以解决核酸递送带来的独特挑战,例如剂量效力、转染效率和翻译率。
研究人员开发了一种用于核酸递送的强效纳米颗粒,并设计了一种适合冻干、上浓缩和填充到 SOMA 装置中的配方。研究人员合成并筛选了一个支链杂化聚β-氨基酯(PBAE) mRNA纳米颗粒文库,以提高转染效率。然后,将性能最高的配方与能够将配方直接输送到胃组织中的可摄入毫注射胶囊相结合。
研究人员比较了使用支链和支链混合 PBAE 纳米颗粒与使用线性 PBAE 纳米颗粒传递的 mRNA 的转染效率。多种细胞类型的体外研究表明,与线性 PBAE 纳米粒子相比,顶部分支或分支的杂化 PBAE 纳米粒子转染的细胞百分比更高。分支的混合 PBAE 也有效地将编码 eGFP 的mRNA 传递到 Caco2 细胞中。事实上,其中一个热门(846) 的转染效率大大高于支链聚乙烯亚胺。
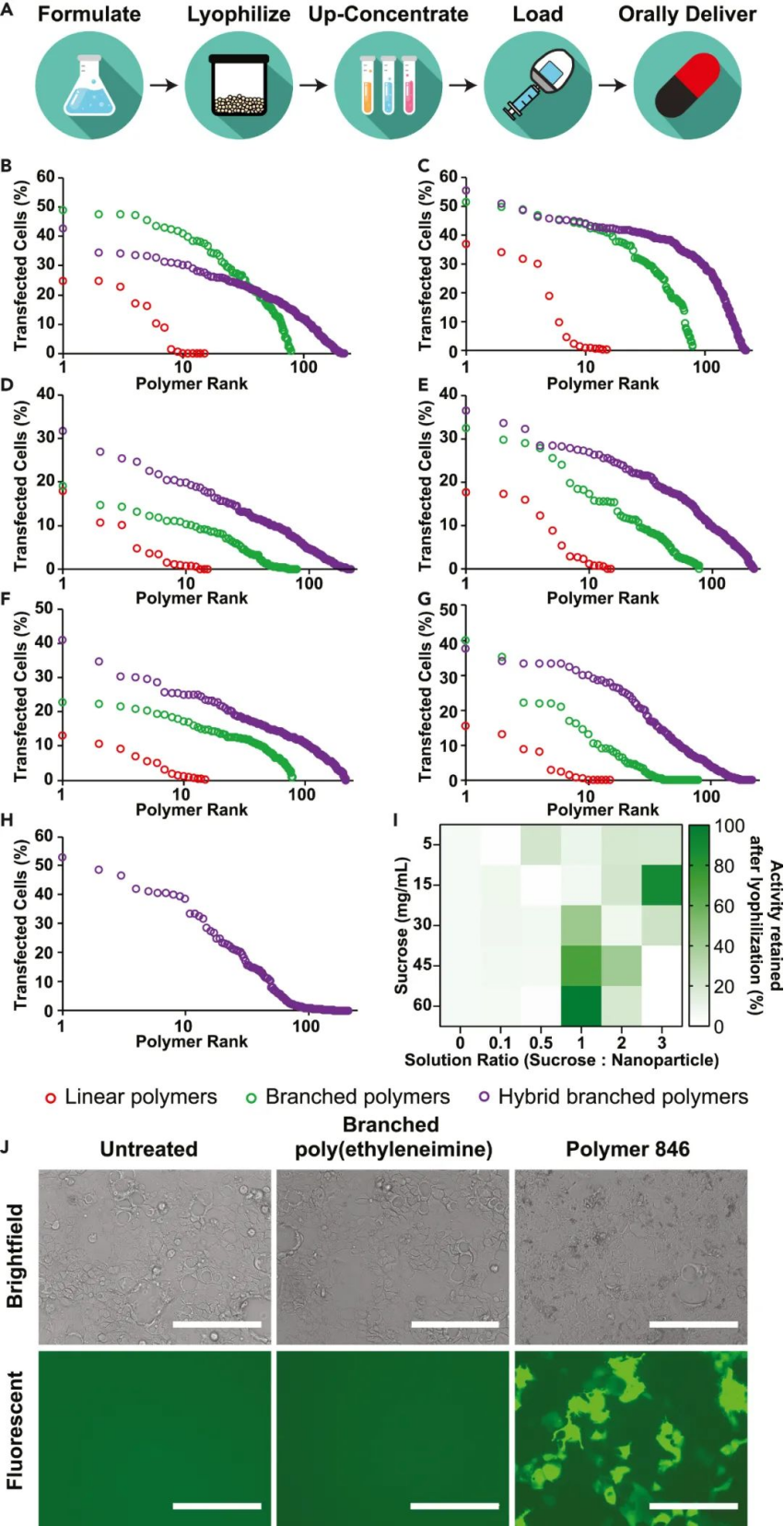
图|支链杂化聚合物纳米粒子的转染效率
为了增加可以装载到口服胶囊中的 mRNA 剂量,研究人员将纳米颗粒冻干并以更高的浓度重组它们。在没有保护剂的情况下冻干导致转染效率完全丧失。然而,以选择的浓度添加蔗糖导致转染效率的完全保留,并使能够将纳米粒子的浓度提高 > 100 倍。应该注意的是,在冻干过程中使用大量蔗糖来稳定纳米颗粒(纳米颗粒重量的 15-60 倍),这与文献报道的核酸递送系统值相当或更低。
随后,研究人员验证了配方和装置在啮齿动物和猪中的性能,证明了蛋白质在胃粘膜的三角洲、胃和壁细胞中的翻译,以及全身吸收。
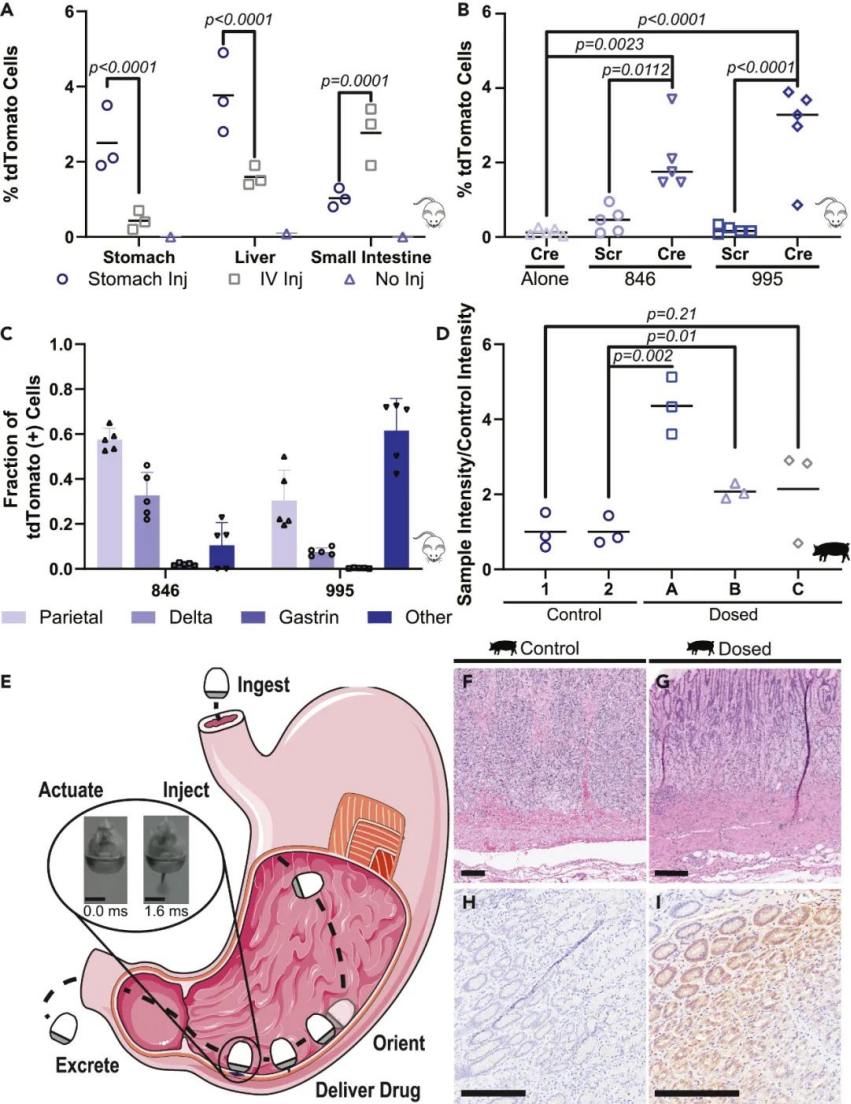
图|在小鼠和猪体内将 mRNA 递送到胃部
总结与展望
这些发现表明,通过口服装置将 mRNA 以及其他核酸直接注射到肠道内壁可能是将这些治疗分子递送到 GI 组织的可行方法。未来通过 B 细胞和 T 细胞反应评估粘膜免疫的工作可能有助于确定免疫反应是集中在胃中还是通过胃肠道和身体其他部位传播。
目前,仍然需要在其他大型动物模型和人体中进行验证,以评估该设备的临床安全性和有效性。在实验中使用了支链混合 PBAE 纳米颗粒,但其他聚合物和脂质纳米颗粒也可能与我们的系统兼容。重要的是,没有进行纳米颗粒优化,它可以减少组织注射后体内核酸降解的影响。有必要进行进一步的研究以进一步优化这些纳米颗粒制剂的给药效率。为了充分发挥该系统的潜力,应进行使用治疗性核酸(例如 mRNA 疫苗)而不是本研究中使用的模型核酸的研究。尽管如此,这种药丸对于口服核酸递送技术来说是一个有前途的发展,可能会提高患者群体的生活质量,并最终改善健康状况。
参考文献:
OralmRNA delivery using capsule-mediated gastrointestinal tissue injections. Matter2022.
https://doi.org/10.1016/j.matt.2021.12.022











