
第一作者:Benxiang Zhang, Yang Gao
通讯作者:Phil S. Baran
通讯单位:Scripps研究所
通过相似或相同官能团的交叉偶联构建C-C化学键是从简单结构快速合成复杂有机分子的有力方法,比如烯烃的复分解、交叉亲电偶联反应。Kolbe电催化反应是一种烷基羧酸电催化氧化脱羧,随后生成的烷基自由基进行C-C偶联的反应。Kolbe电催化反应历史悠久,对于有机合成非常重要,但是实际上Kolbe电催化反应基本上没有应用。从反应的设计角度看,Kolbe电催化能够实现两种羧酸分子之间偶联,而且不必考虑羧酸分子的极性或羧酸基团相邻的官能团。但是,实际上这种反应由于中间体容易受到强氧化性的电催化环境破坏,难以得到实际应用。
有鉴于此,Scripps研究所Phil S. Baran等报道通过还原性温和的Ni-电催化反应体系,能够将羧酸进行原位转化为氧化还原活性酯RAE,随后两种反应物进行脱羧交叉偶联继续反应,这种反应过程可以称之为双重脱羧交叉偶联dDCC(doubly decarboxylative cross-coupling)。
这种反应操作简单,对一级、二级、少数三级羧酸的氧化还原活性酯都兼容。对比发现,发展的电催化反应实现了化学计量比金属还原剂或者光催化反应都无法达到的效果。电催化反应能够放大合成,与现有主流合成方法相比更加简单有效,在合成32种已知化合物的过程中,与现有方法相比,合成步骤总体减少了73 %。
背景
Kolbe电催化反应历史悠久,首次出现在19世纪中叶。经典的Kolbe电催化反应是对脂肪羧酸进行氧化脱羧生成瞬态烷基自由基,随后自由基进行Csp3-Csp3偶联。这种反应很难应用于复杂结构有机分子,比较少见的例子是用于Corey经典合成五环角鲨烯和单环角鲨烯。Kolbe电催化在工业领域被应用于润滑油行业,近期Kolbe电催化被发现可能在生物质转化。Kolbe电催化虽然具有悠久历史,但是并没有在主流有机合成中得到应用。这是因为Kolbe电催化反应通常需要严苛的电催化环境,需要使用Pt电极、特别高的电流密度(>250 mA/cm2)、非常高的过电势,这导致反应过程难以产生较好的选择性、反应的官能团兼容性较差。
反应设计和发展
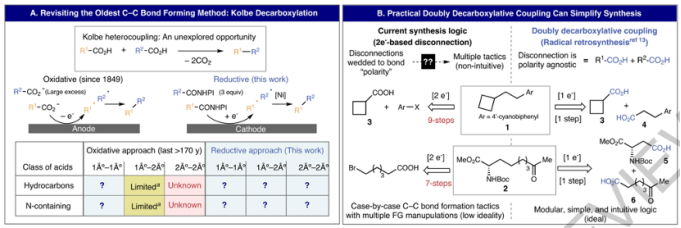
图1. Kolbe电催化偶联反应的性质和潜在优势
由于Kolbe氧化偶联反应具有底物兼容性较少的缺点,作者认为通过在反应过程中原位将羧酸转化为氧化还原活性的酯RAE,能够使用合适的过渡金属催化剂在比较温和的电催化反应条件以操作性更好的方式进行Kolbe电催化偶联。之前的工作中,Negishi, Suzuki, Kumada偶联反应能够通过Ni催化使用RAE用于构建C-C化学键,而且这种反应能够大大降低全合成所需的步骤。
在实验中发现,与文献方法相比,通过Ni催化剂进行电催化双重脱羧偶联,对32种分子的合成总共能降低>160步,步骤的缩减量达到73 %。
反应情况
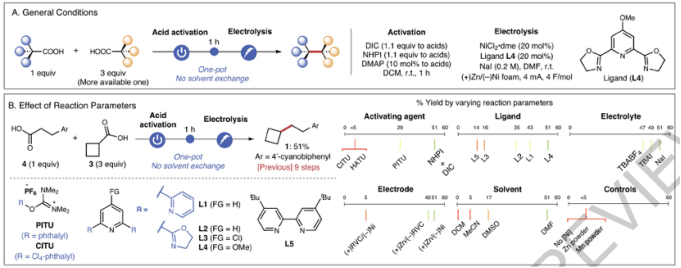
图2. 优化后的反应条件、反应参数对反应情况的影响
将两种不同羧酸反应物(反应物比例为1:3)溶解于CH2Cl2溶剂,随后加入DIC和NHPI和催化量DMAP,室温搅拌1 h后羧酸转化为氧化还原活性酯REA。随后加入DMF稀释,加入NiCl2和配体作为Ni催化剂,加入NaI后进行电催化。以Zn作为阳极、泡沫Ni作为阴极,经过2.5 h电催化反应得到目标偶联反应产物。
反应兼容性
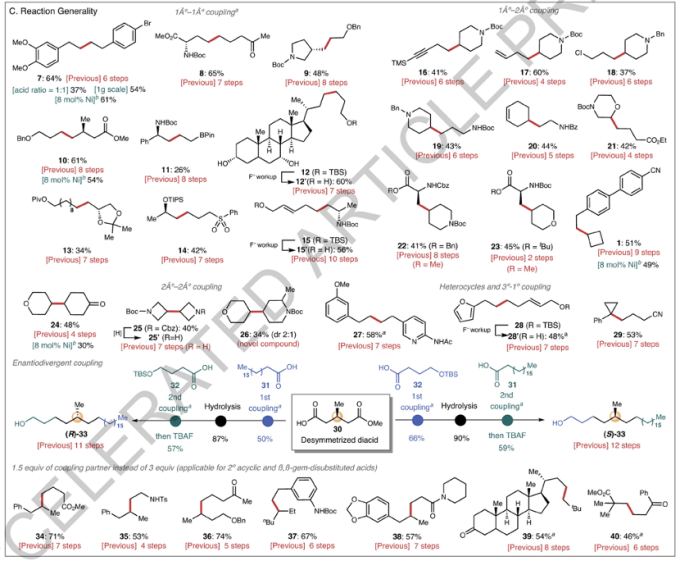
图3. 反应兼容性
Ni电催化双重脱羧偶联反应展示了广泛的底物兼容性,能够进行1°-1°、1°-2°甚至一些1°-3°偶联。该反应对芳基卤化物(7)、酯(8, 10, 13, 21-23, 34, 40)、氨基甲酸酯(8, 9, 11, 15-17, 19, 21-23, 25, 26, 37)、酰胺(20, 27, 35, 38)、三级胺(18, 19)、醚(7, 9, 10,12, 11, 14, 21, 23, 24, 26, 27, 36)、缩酮(13)、烷基卤化物(18)、炔烃(16)、烯烃(15, 17, 20, 28)、醇(12, 40)、砜(14)、酮(8, 24, 36, 39, 40)、烷基硼酸酯(11)、氮杂环丁烷(25)等结构分子都兼容。此外,该反应还对芳香/脂肪醛、重氮甲烷结构分子兼容。这些例子中,大量官能团无法兼容经典Kolbe电催化的强氧化性环境。
优势和不足
这种直接构建C-C化学键的方法有效的降低合成反应的步骤。比如通过之前的工作合成环丁烷结构是通过2e-反应进行,其中需要经历多个步骤,包括增加一个碳同系物、F-C酰基化/Wolff-Kishner反应多个步骤,合成总共需要9步,总收率仅仅11 %;通过这种电催化反应方法,有效的降低复杂反应过程。
反应方法学对于构建远端立体结构中心特别有效,因为含有手性中心的羧酸分子非常容易购买,因此能够免于复杂和代价较高的不对称催化合成,能够缩减3步或者更多步骤。
局限性。该反应的局限性在于难以对芳环/磷酸酯/酯相邻的脂肪羧酸进行脱羧偶联。
参考文献及原文链接
Zhang, B., Gao, Y., Hioki, Y. et al. Ni-Electrocatalytic C(sp3)–C(sp3) Doubly Decarboxylative Coupling. Nature (2022)
DOI: 10.1038/s41586-022-04691-4
https://www.nature.com/articles/s41586-022-04691-4











