大多数癌症疫苗以肽抗原为靶点,由于将肽呈递给 T 细胞的主要组织相容性复合物 (MHC) 分子存在巨大的个体差异,因此需要进行个性化。此外,肿瘤经常通过干扰肽呈递的机制逃避 T 细胞介导的免疫,例如,MICA 和MICB 蛋白可以在肿瘤上表达,并向免疫系统发出“杀死我”的信号,但是肿瘤通常会通过脱落这些蛋白质来伪装自己,这会阻止专门的自然杀伤 (NK) 细胞识别和破坏癌症。在2018年,美国丹娜法伯癌症研究院Kai W. Wucherpfennig等人在Science上报道了一种抗体的设计,这些抗体可防止人类癌细胞对细胞表面 MICA 和 MICB 的损失,进而使得免疫细胞可以对其进行杀伤作用。
近日,美国丹娜法伯癌症研究院Kai W. Wucherpfennig等人对于该靶点再次进行进一步的研究,开发了一种针对肿瘤免疫逃逸机制的概念性全新癌症疫苗,该疫苗可诱导多种 T 细胞和自然杀伤 (NK) 细胞群的协同攻击。成果发表在Nature上。

该疫苗以MICA和MICB(MICA/B)应激蛋白为靶点,这些蛋白在许多类型的人类癌症中因 DNA 损伤而被上调,但健康细胞的表达水平很低或无法检测到。MICA/B作为配体,激活T细胞和NK细胞上的NKG2D受体,然而,许多人类肿瘤通过从细胞表面蛋白水解脱落MICA/B 来逃避这一重要的免疫识别途径。据报道,去除MICA/B 蛋白可诱导 NKG2D 受体内化并抑制 NK 细胞功能。因此,该疫苗诱导的抗体旨在通过抑制蛋白水解裂解,来增加肿瘤细胞表面MICA/B蛋白的密度,增强树突状细胞向 T 细胞呈递肿瘤抗原并增强 NK 细胞的细胞毒性功能。该疫苗以蛋白水解脱落位点MICA/B中高度保守的α3结构域为靶点,旨在通过T细胞和NK细胞诱导肿瘤免疫。研究人员有意省略α1–α2结构域,以避免诱导可能阻断NKG2D受体结合的抗体。疫苗抗原的多价展示极大地增强了免疫原性,因此研究人员将MICB或MICA的α3结构域融合到幽门螺杆菌铁蛋白的N端,形成由24个亚单位组成的颗粒。所有实验均以铁蛋白作为对照抗原。并且,利用最近开发的一种由粒细胞-巨噬细胞集落刺激因子 (GM-CSF) 和 CpG ODN 1826(佐剂)配制而成的中孔二氧化硅棒 (MSR) 可生物降解支架,用于疫苗递送。
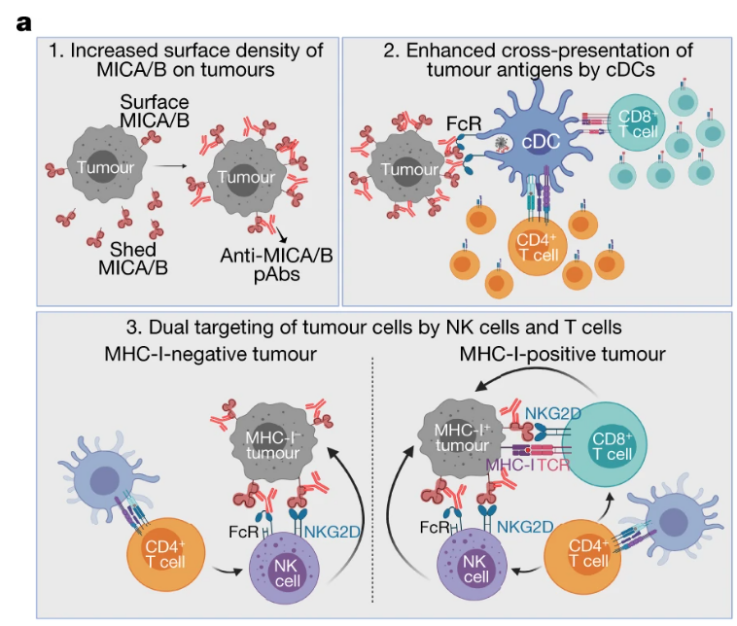
图|疫苗设计
首先,研究人员通过小鼠和恒河猴验证了该疫苗的有效性。在给恒河猴接种后,动物均产生了抗 MICA 和抗 MICB 抗体,并且恒河猴随着随后的加强免疫,滴度增加了 100 到1,000 倍。且接种后没有临床副作用或血液化学变化,这提供了疫苗安全性的初步证据。
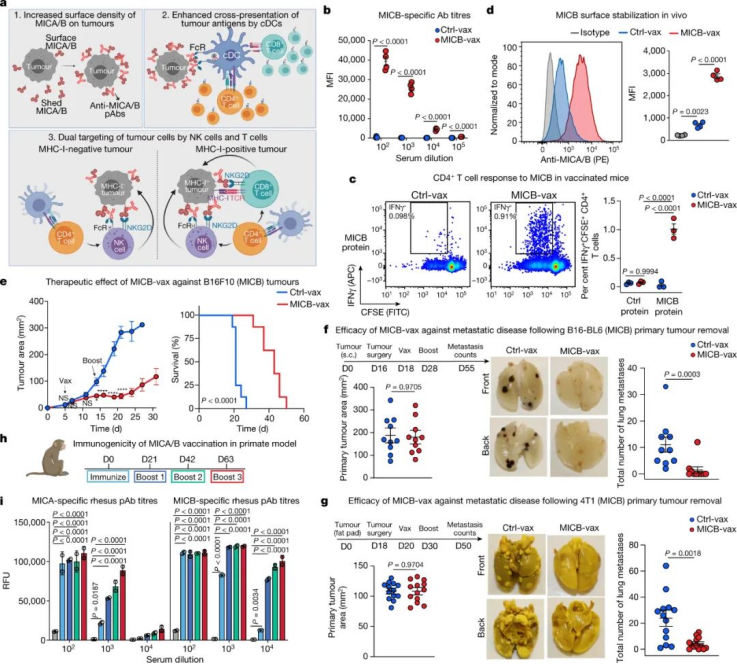
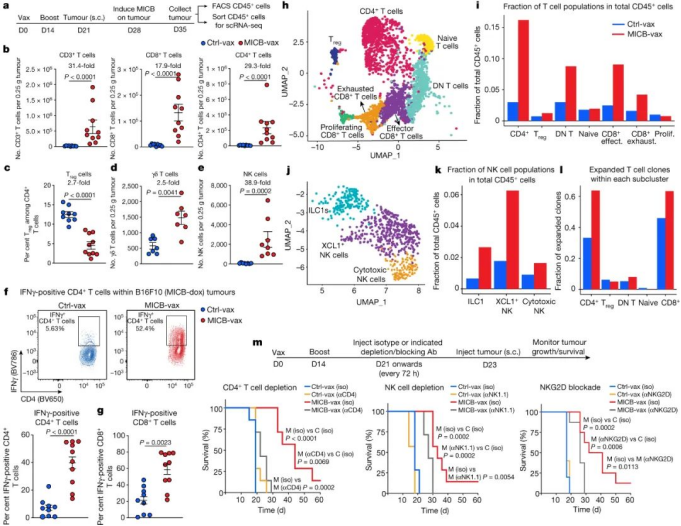
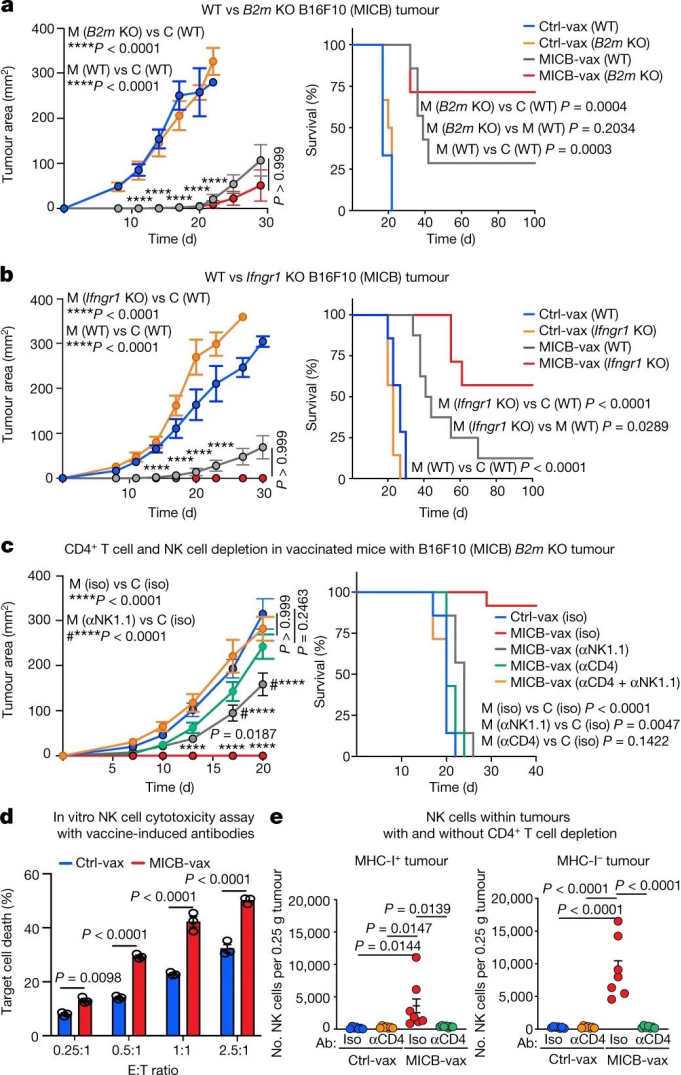
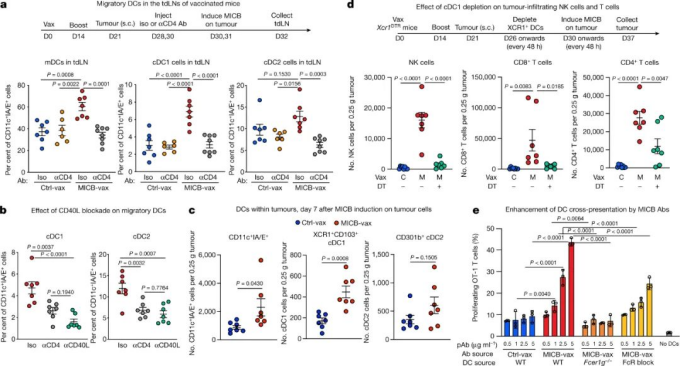
随后,研究人员对肿瘤中的免疫环境进行分析,与接受Ctrl-vax的小鼠相比,用MICB-vax免疫的小鼠肿瘤中的多效应淋巴细胞群高度富集,CD4+ T细胞富集29.3倍,CD8+ T细胞富集17.9倍,NK细胞富集38.9倍。此外,其相关基因和趋化因子显着上调和表达增加。因此,这些数据表明,MICB-vax可以诱导多效应 T 细胞和 NK 细胞群有效募集到处于高度激活状态的肿瘤中。对当前免疫疗法耐受的通常由 MHC-I 抗原呈递或 IFNγ 信号通路中基因的失活突变(或下调)介导,这会极大地损害 CD8+ T 细胞介导的肿瘤免疫。在对免疫耐受的肿瘤(B2m–/–和 Ifngr1–/–)实验中,50-75% 的小鼠在 100 天后仍保持无肿瘤状态,且其功效是由 NK 细胞和 CD4+T 细胞介导的,并且 CD4+ T 细胞在 NK 细胞募集到肿瘤中起重要作用。最后,研究人员研究了为什么NK细胞会被募集的机制。先前研究表明,cDCs(cDC1和cDC2)在将肿瘤抗原转运到肿瘤引流淋巴结(tdLNs)中发挥重要作用,它们在此处引发抗肿瘤T细胞。通过实验验证,与接受 Ctrl-vax 的小鼠相比,用 MICB-vax接种的小鼠的 tdLNs 中迁移的 cDC1 和cDC2 细胞数量显着增加。因此,MICB-vax 通过 CD4+ T 细胞依赖性机制诱导 cDC1 迁移到 tdLNs,并且在用MICB-vax 免疫的小鼠的肿瘤中,NK 细胞和 CD8+T 细胞的积累需要 cDC1 细胞。此外,还表明了MICB-vax接种处理的小鼠增强了 DCs对黑色素瘤抗原的体内摄取。图|CD4+ T 细胞和 cDC1 细胞在 NK 细胞募集到肿瘤中的作用综上所诉,所提出的疫苗设计通过多种效应细胞群(包括不同的 T 细胞和 NK 细胞群)实现了肿瘤免疫。疫苗诱导的抗体抑制了肿瘤细胞的蛋白水解MICA/B 脱落,增强了NK细胞的细胞毒性功能,并增加了cDC1介导的肿瘤抗原向 CD8+ T 细胞的交叉呈递。但是,这项工作的一个限制是人类 MICA/B 蛋白必须在小鼠肿瘤细胞中表达,因为小鼠 NKG2D 配体与 MICA/B 的同源性有限。因此,这种方法还需要在癌症患者的临床试验中进行评估,并且正在计划进行首次人体临床试验。此外,这种疫苗也可能与局部放射治疗结合使用,因为 DNA 损伤会增强癌细胞的 MICA/B 表达。1.Badrinath, S., Dellacherie, M.O., Li, A. et al. A vaccine targeting resistanttumours by dual T cell plus NK cell attack. Nature (2022).https://doi.org/10.1038/s41586-022-04772-42.Ferrari de Andrade, L. et al. Antibody-mediated inhibition of MICA and MICBshedding promotes NK cell-driven tumor immunity. Science 359, 1537–1542 (2018).https://www.science.org/doi/10.1126/science.aao0505