特别说明:本文由学研汇技术中心原创撰写,旨在分享相关科研知识。因学识有限,难免有所疏漏和错误,请读者批判性阅读,也恳请大方之家批评指正。
原创丨彤心未泯(学研汇 技术中心)
编辑丨风云
碳烯:
在化学领域,获取瞬态和反应中间体的新策略对进一步的研究和合成应用很有帮助。在有机化学中,碳烯就是这样一种中间体,是一种具有两个未共用价电子的中性碳分子。碳烯是一种高度有效的反应性中间体,可促进各种其他难以实现的化学反应,包括小环的形成和强δ键的插入。为了获得这种有价值的反应性,通常使用具有高熵或焓驱动力的试剂,包括爆炸性(重氮)或不稳定(宝石-二卤)化合物。重氮烷烃是一种活性碳基分子,在碳烯形成时释放氮。当与金属催化剂配对时,会发生各种不同的反应。重氮烷烃可以被受电子/给电子基团取代以调节生成的碳烯的电子特性以及随后的反应特性。然而,在处理这些热不稳定分子时,反应过程中释放的氮气会导致严重的安全问题(如爆炸、窒息等)。另一种常用方法是金属(例如锌)与二卤代烷烃的反应。虽然这种方法更安全,但所得锌类化合物的反应性仅限于环丙烷的形成(即环丙烷化)。如果原料是烷基取代的二卤代烷,则锌类碳烯的制备也可能会出现有害的副反应,这进一步限制了它们的应用。
虽然碳烯在有机化学中具有广泛的应用,但获取这种有价值的中间体仍存在以下关键问题:1. 安全问题亟需解决:重氮烷烃是一种不稳定的前体分子,在使用过程中会释放大量氮气,有可能会引起爆炸、不受控的连锁反应以及操作者的窒息等安全问题。2. 存在有害副反应:金属与二卤代烷烃的反应可以产生碳烯,但由于锌羰基化合物的1,2-H迁移,质子很少被耐受,使用锌类碳烯的制备可能会出现有害的副反应。3. 缺少合成活性碳烯的通用方法:虽然通过硼酸锂碳烯、Mo介导的酮脱氧和金催化的炔烃环化可以解决Matteson重排,但仍然没有一种通用的方法来获取非稳定的烷基碳烯,或者将它们用于稳定重氮试剂的广泛的碳烯反应。有鉴于此,美国俄亥俄州立大学David A. Nagib等人受经典的 Clemmensen中用Zn(Hg)和HCl还原羰基化合物的启发,开发了一种以安全的方式从稳定的前体制备碳烯的方法。利用稳定且可扩展的含乙酸盐的有机卤化物前体,证明了芳基和烷基取代的碳烯的形成,其本身可以衍生自简单的醛。通过将这些碳烯与适当的金属催化剂配对,可以控制它们的反应性以进行各种合成转化。这种通用方法避免了重氮烷烃的安全问题以及二卤代烷烃的稳定性和选择性限制。

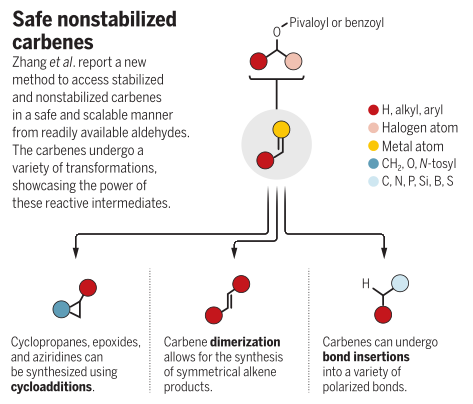
1、设计了羰基化合物转化为电子多样化碳烯的通用催化策略作者提出碱金属催化剂控制的α-酰基化消除可以形成活泼的金属羰基。与简单的锌羰基相比,催化可以赋予碳烯不同的反应性。此外,利用该方法可以实现大规模的生产且无安全隐患。作者探索了碳烯的安全性和反应性,对醛衍生的碳烯前体进行了不同类别反应性的验证,包括环丙烷化和X-H插入。发现一系列烷基胺和芳基胺有效地进行了N-H插入。更亲核的H供体(例如,膦、硅烷、硼烷)非常适合这种碳烯反应性,已证实应用于数10种反应类别。作者通过一系列中间体表征、反应性比较和动力学数据对碳烯反应解析了碳烯反应机理。发现了催化碳烯中间体的亲电性,在引入硫化物助催化剂后,瞬态过硫酸盐能够与此类亲电试剂发生反向反应,无需重氮中间体。利用原位红外光谱和可变时间归一化分析表明二聚反应在催化剂中是二级反应。
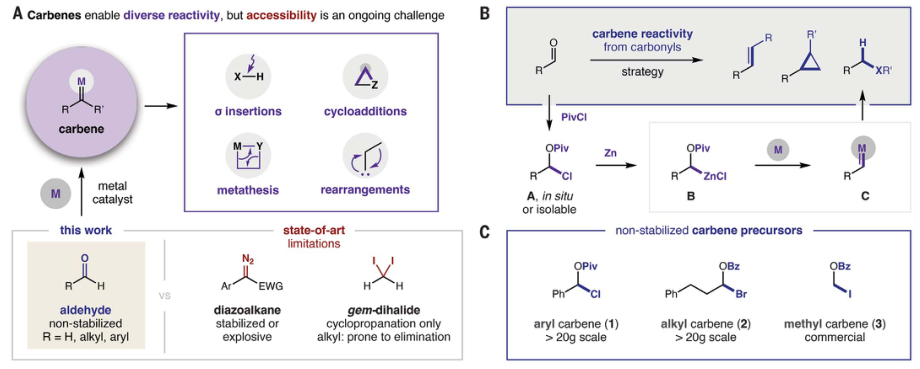
重氮烷烃可以在100°C分解,其分解产生的能量超过200 kJ/mol。这种热不稳定性使得这些试剂的放大反应非常危险。本工作中对于醛衍生的碳烯前体,在>300°C下分解时产生的能量小于30 kJ/mol,且避免了氮的输出。因此,该反应可以放大1000倍而不会发生安全事故。本工作中碳烯前体被证实在10多种不同类型的反应中具有通用性的。利用廉价的非贵金属催化剂,通过二聚反应选择性地生成烯烃产品。通过调控催化剂,可以实现碳烯反应性的调节。由这些前体生成的稳定的芳基碳烯和不稳定的烷基碳烯也成功地进行了键插入反应。作者提出碱金属催化剂控制的α-酰基化消除可以形成活泼的金属羰基。与简单的锌羰基相比,催化剂影响也可以赋予不同的反应性。作者发现亲电性较低的羰基化合物最好与亲电性更强的酰卤配对,以提供反应性越来越强的卡宾前体。然而,亲电性较低的脂肪醛最好与苯甲酰溴 (BzBr)结合形成不稳定的烷基类似物。两种反应都可以在>20 g的规模下进行,且不会出现类似重氮类似物固有的安全问题。苯甲酰碘 (BzI)很容易与反应性最低的醛、甲醛结合,从而获得甲基碳烯前体,这是一种常见的保护基团,可以以千克为单位购买,成为重氮甲烷的安全替代品。
通过将苯甲醛纳入所提出的策略来研究碳烯二聚反应,这是一个需要PivCl添加、插入Zn和金属催化的三阶段序列。结果表明几种基本金属盐能够有效地二聚生成二苯乙烯,并观察到CoCl2具有显著的催化剂立体控制。除了作为碳烯反应性概念的证明,还表明了电子上不同的取代基在芳基碳烯组分中具有很好的耐受。
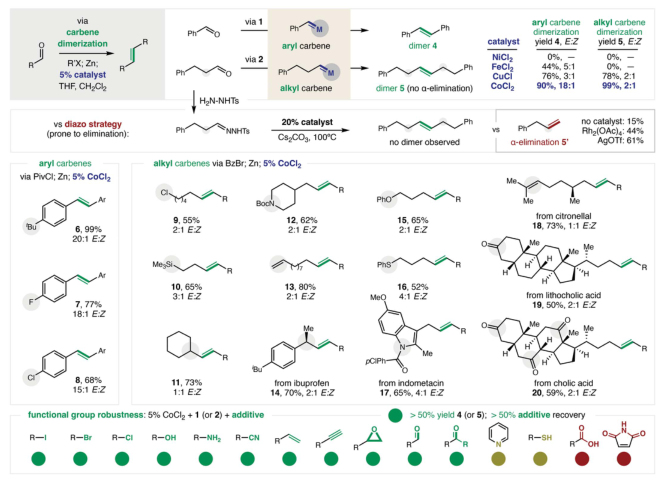
作者测试了烷基卡宾反应性可以通过催化方法以比重氮烷烃或二卤化物更安全和更有选择性的方式利用。可以转化为碳烯的脂肪族醛的独特广泛范围是这项初步研究的亮点。为此,发现CoCl2有效地催化氢化肉桂醛的碳烯二聚化。与未催化的甲硅烷氧基变体相比,没有观察到α-消除。为了进一步的比较,通过将腙置于各种催化剂和碱中以获得其碳烯,研究了重氮化策略。此外,进行了稳健性研究以进一步评估该策略的广泛官能团耐受性,将化学多样化的添加剂与催化剂和碳烯前体结合,证实了它们在二聚化步骤中的可行性。
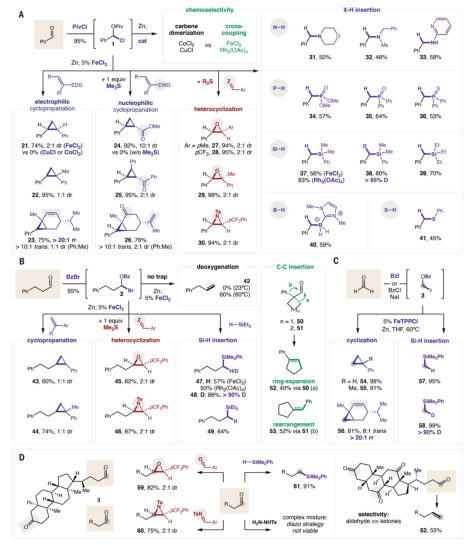
为了证明在更复杂的环境中的可行性,利用两种胆汁酸的醛经历了四种不同类别的碳烯反应,证实了本工作策略的可行性。作者基于一系列中间体表征、反应性比较和动力学数据解析了碳烯反应机理。作者探索发现了催化碳烯中间体的亲电性,在引入硫化物助催化剂后,瞬态过硫酸盐能够与此类亲电试剂发生反向反应,而无需重氮中间体。金属催化剂决定了反应的化学选择性。碳烯二聚反应的原位红外光谱和可变时间归一化分析表明二聚反应在催化剂中是二级反应。
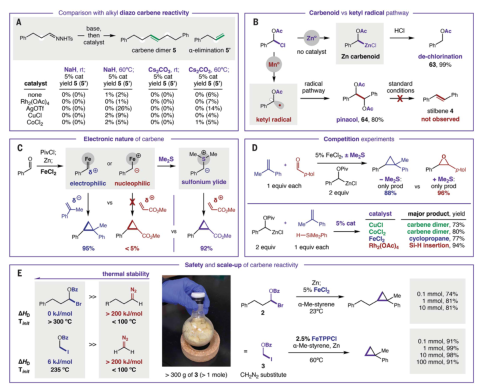
本文报道的碳烯前体的直接合成、稳定性、可扩展性和选择性,将为化学家提供更好的方法来实现有价值的碳烯合成应用。作者提供了一种直接的方法,克服了长期存在的安全性和反应性挑战,从醛中生成这些有价值的稳定和非稳定的反应性中间体。预计该方法将对碳烯反应的进一步发展产生三重影响,包括使用非贵金属催化剂、使用安全可扩展的试剂以及改进不稳定碳烯的合成途径,这将助力对碳烯化学的学术及工业化探索。MICHAEL S. WEST, et al. Safe, selective, and scalable carbenes. Science, 2022, 377: 580-581.DOI: 10.1126/science.abq8253.https://www.science.org/doi/10.1126/science.abq8253LUMIN ZHANG, et al. Carbene reactivity from alkyl and aryl aldehydes. Science, 2022, 377: 649-654.DOI: 10.1126/science.abo6443https://www.science.org/doi/10.1126/science.abo6443














