与传统药物疗法相比,机械组织刺激对于促进组织再生和康复具有吸引力,因为它可以提供局部活性,可以避免多效性效应,还可以简化监管审批程序。细胞和组织可以通过称为机械转导的过程对微环境生物物理线索和外部机械刺激作出反应,该过程将物理信号转化为细胞功能的变化。调查机械刺激对细胞和工程组织结构影响的研究发现,机械刺激(例如,拉伸)可以调节细胞增殖、力产生和细胞分化。此外,机械装置通常用于临床手术,如牵引成骨、组织扩张和正畸。最近的临床前研究证明了压缩负荷(例如,机械疗法)对肌肉再生和康复的治疗效果。然而,外部施加的拉伸或收缩是否也能产生这种有益效果,这在很大程度上仍然是未知的。
通过拉伸或收缩来机械刺激体内组织有两个主要的技术挑战:
1)一是开发能够沿着组织表面产生力或应变的机械系统,
2)二是形成坚固的组织界面,可以有效地将这些刺激传递到组织。
尽管软机器人领域已经发展出了各种产生机械驱动的机制,但许多机制既不具有生物相容性,也不适用于身体,这限制了它们在生物医学应用中的应用。形状记忆合金(SMA)是一种很有前途的候选材料,由于其坚固的机械性能、高弹性和生物相容性,已广泛应用于医疗器械中。由SMA制成的弹簧可以使用相对低的电压以受控的方式产生机械力和致动,这表明它们适合于生物相容的软机器人致动器。同时,一类基于坚韧水凝胶的组织粘合剂可以实现对多种组织类型的强粘合。这些水凝胶还被证明与工程材料如弹性体结合。将这两种类型的材料组合可以提供生物医学装置,其能够实现目标组织的机械拉伸或收缩。
机械刺激装置的一个潜在治疗目标是肌肉萎缩。肌肉萎缩是由身体缺乏活动或去神经支配引起的,也是对禁食和各种疾病(包括癌症相关恶病质和糖尿病)的系统反应。在萎缩的进展过程中,由于肌原纤维和可溶性蛋白质的加速降解以及新蛋白质的合成减少,导致肌肉质量下降,导致肌肉无力和残疾增加。虽然可以通过运动来预防或减缓肌肉萎缩,但这通常是不可行的(例如,对于卧床休息的患者)。因此,肌肉萎缩的有效对策通常仍代表着未满足的临床需求,而机械刺激的递送可能是替代或补充治疗。虽然已经提出机械疗法(例如,按摩疗法)来缓解肌肉萎缩,但尚未探索机械拉伸或收缩的影响。
成果简介
鉴于此,哈佛大学David J. Mooney院士等人开发了一种具有机械活性的凝胶-弹性体-镍钛诺组织粘合剂 (mechanically active gel–elastomer–nitinol tissue adhesive, MAGENTA),它可以牢固地附着在骨骼肌上,并以所需的强度和频率提供模拟肌肉收缩的刺激。

整体设计
MAGENTA的机械驱动由SMA(即镍钛诺)弹簧和弹性体制成的软机器人致动器实现。通过结合坚韧的水凝胶基粘合剂实现组织粘附,该粘合剂与下层组织接触并传递致动,以局部和受控的方式提供机械刺激。
虽然弹簧能够实现用于组织刺激的机械致动,但弹性体形成致动器的主体,提供结构和机械支撑。为了制造致动器,将镍钛合金弹簧连接到电线并嵌入弹性体中。当施加电压时,致动器快速收缩,直到弹簧收缩和弹性体阻力之间的力平衡。驱动应变(定义为弹簧长度变化与初始长度之比)以电压相关方式控制,直到达到最大值。当电流中断时,收缩的致动器在弹性体的恢复力的驱动下迅速松弛到其初始状态,从而允许连续驱动。致动的频率和持续时间可以通过微处理器简单地编程。考虑到制造工艺的简单性,致动器的设计和尺寸可以很容易地从毫米缩放到几厘米。研究结果表明弹性体-水凝胶和水凝胶-组织界面的界面韧性分别测得高于 800 J m -2和 600 J m -2。该方法建立了一种简单而简便的方法,用于构建可按需提供编程驱动的软机器人致动器。
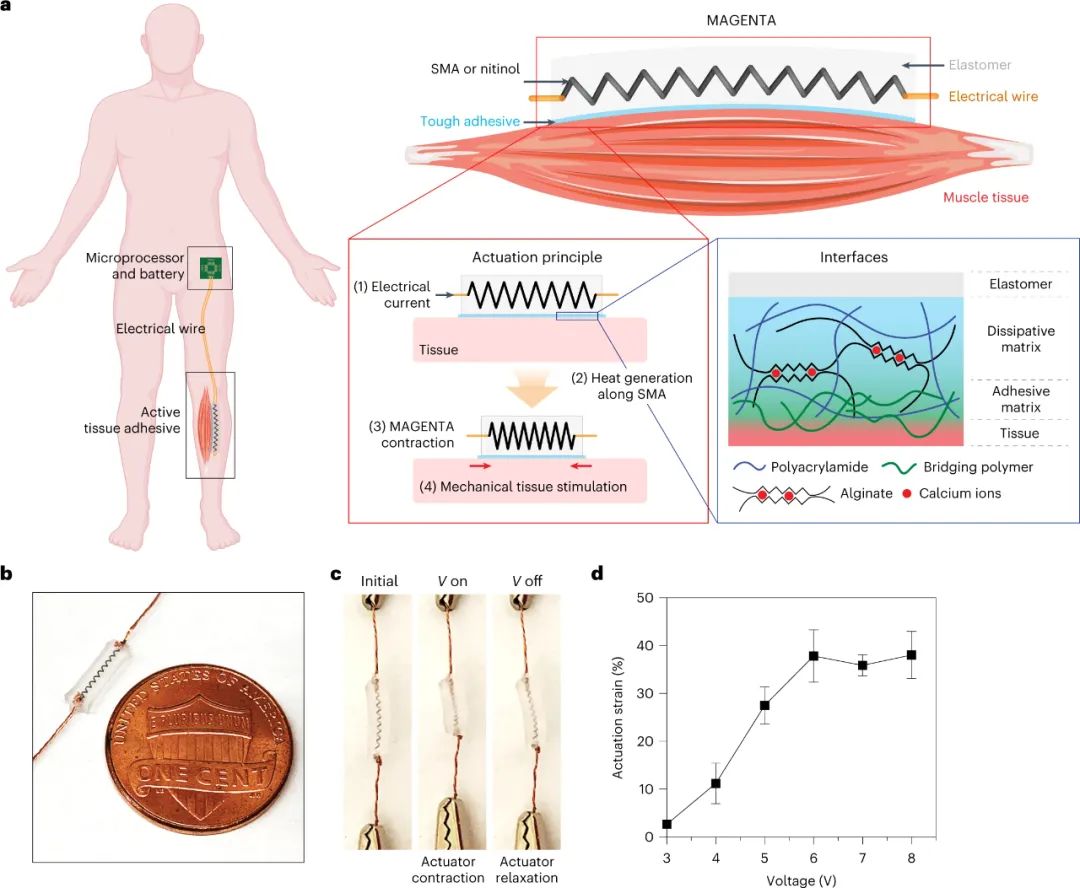
图|MAGENTA 为目标组织提供机械刺激
MAGENTA的体外和体内应用
在体外实验结果中,MAGENTA 的机械刺激显著增加了 C2C12 细胞的增殖,并增强了它们的融合。然后研究了MAGENTA 对肌肉萎缩的生理影响;研究发现MAGENTA 激活涉及 yes 相关蛋白和心肌素相关转录因子 A 的机械传感通路,并增加肌肉蛋白合成的速率。与未经处理的肌肉相比,用 MAGENTA 处理过的废用肌肉表现出更大的尺寸和重量,并产生更大的力量,这些结果证明了MAGENTA可以预防肌肉萎缩。
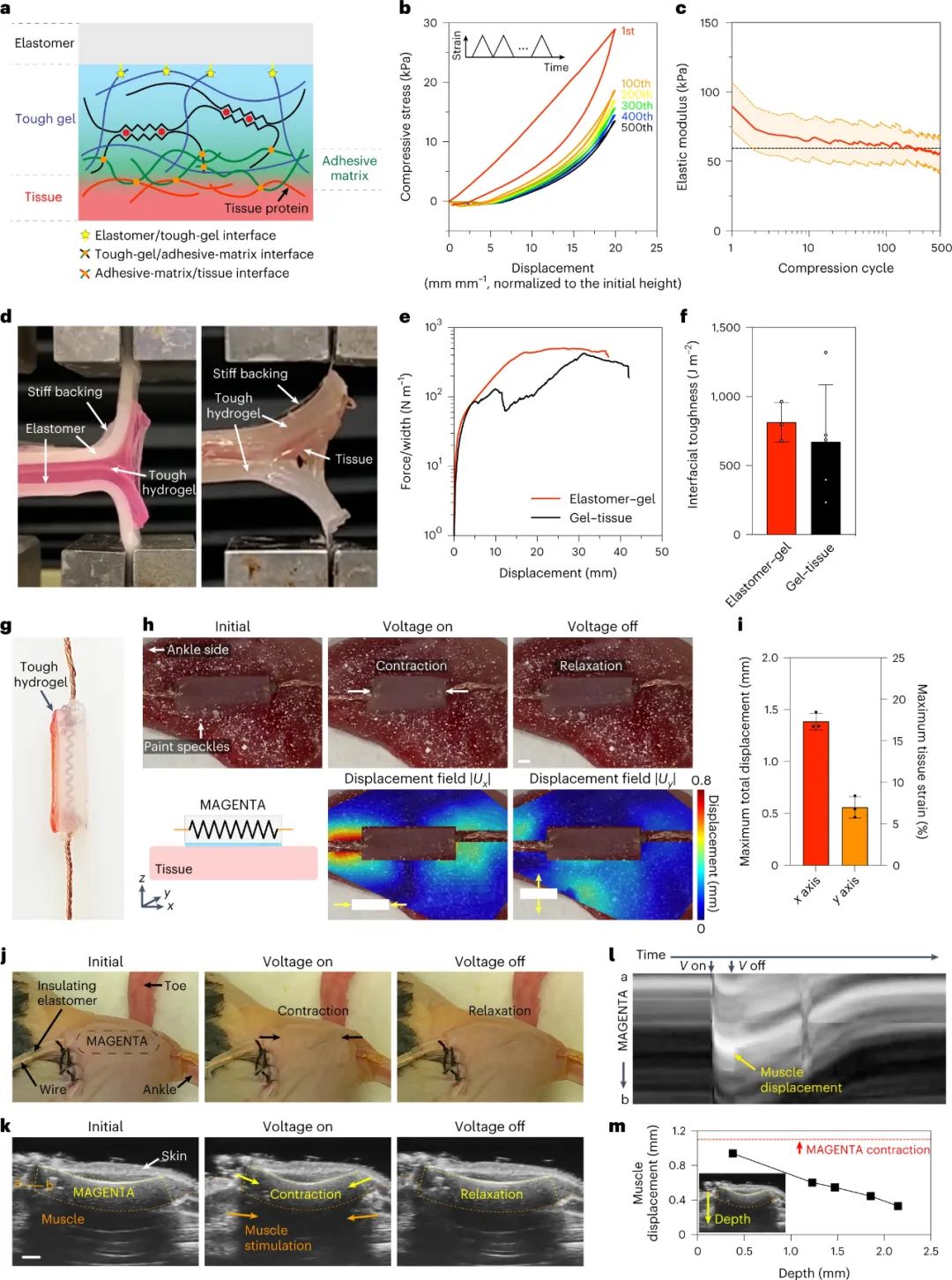
图|MAGENTA 的离体和体内应用
远程控制!
确定了由电信号驱动的 MAGENTA 的性能和治疗潜力后,研究人员最终探索了远程控制 MAGENTA 的可能性。研究发现镍钛诺弹簧在 420–1,000 nm 范围内的所有波长下都表现出非常低的反射率,表明弹簧可以吸收光来驱动。因此,研究人员使用光响应致动器创建无线、可远程控制的 MAGENTA。通过体内外实验观察,无线 MAGENTA在激光照射确实可以使其下方的组织实现收缩。这些结果表明远程控制的可能性。
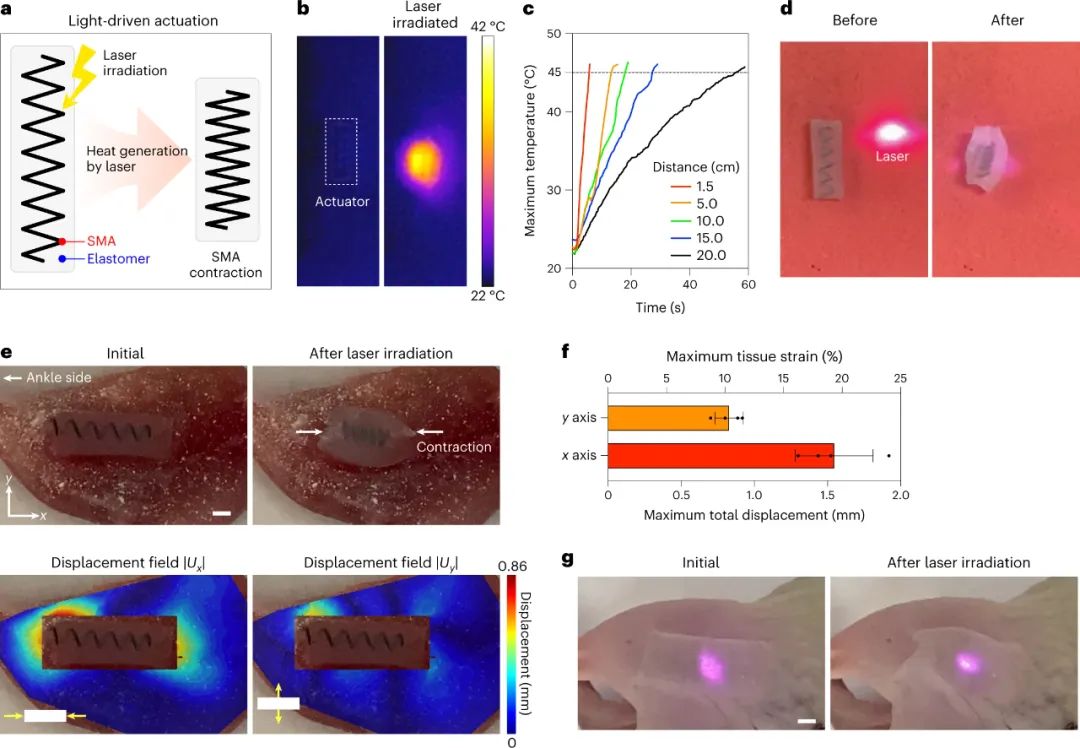
图|用激光无线遥控 MAGENTA
小结:
综上所述,该研究开发了 MAGENTA,这是一种组织界面生物医学设备,能够粘附到目标组织并以受控方式提供模拟肌肉收缩的机械刺激,以促进组织再生和康复。由镍钛诺弹簧收缩驱动的 MAGENTA 致动不仅在组织表面而且在组织内部导致组织位移。MAGENTA 的治疗效果在废用性肌肉萎缩模型中得到证实。通过机械刺激,延缓了萎缩的发生,促进了恢复。
虽然目前的工作主要集中在废用性萎缩背景下的骨骼肌刺激,但该系统也可能直接适用于其他类型的组织,包括皮肤和心脏。最后,为了扩大 MAGENTA 在各种医疗环境中的潜在用途,作者展示了其使用激光的无线遥控驱动。未来对无线 MAGENTA 进行表面改性以提高其光敏性的工作可以解决光穿透深部组织的限制并提高设备的性能。因此,MAGENTA 在治疗肌肉萎缩和再生医学方面具有广阔的应用前景。
值得注意的是,7月11日,哈佛大学David J. Mooney和丹娜法伯癌症研究院Kai W. Wucherpfennig等人在Nature Materials发表研究论文表明骨髓纤维化的机械特性,即骨髓的液-固特性(粘弹性),有助于单核细胞的异常分化。

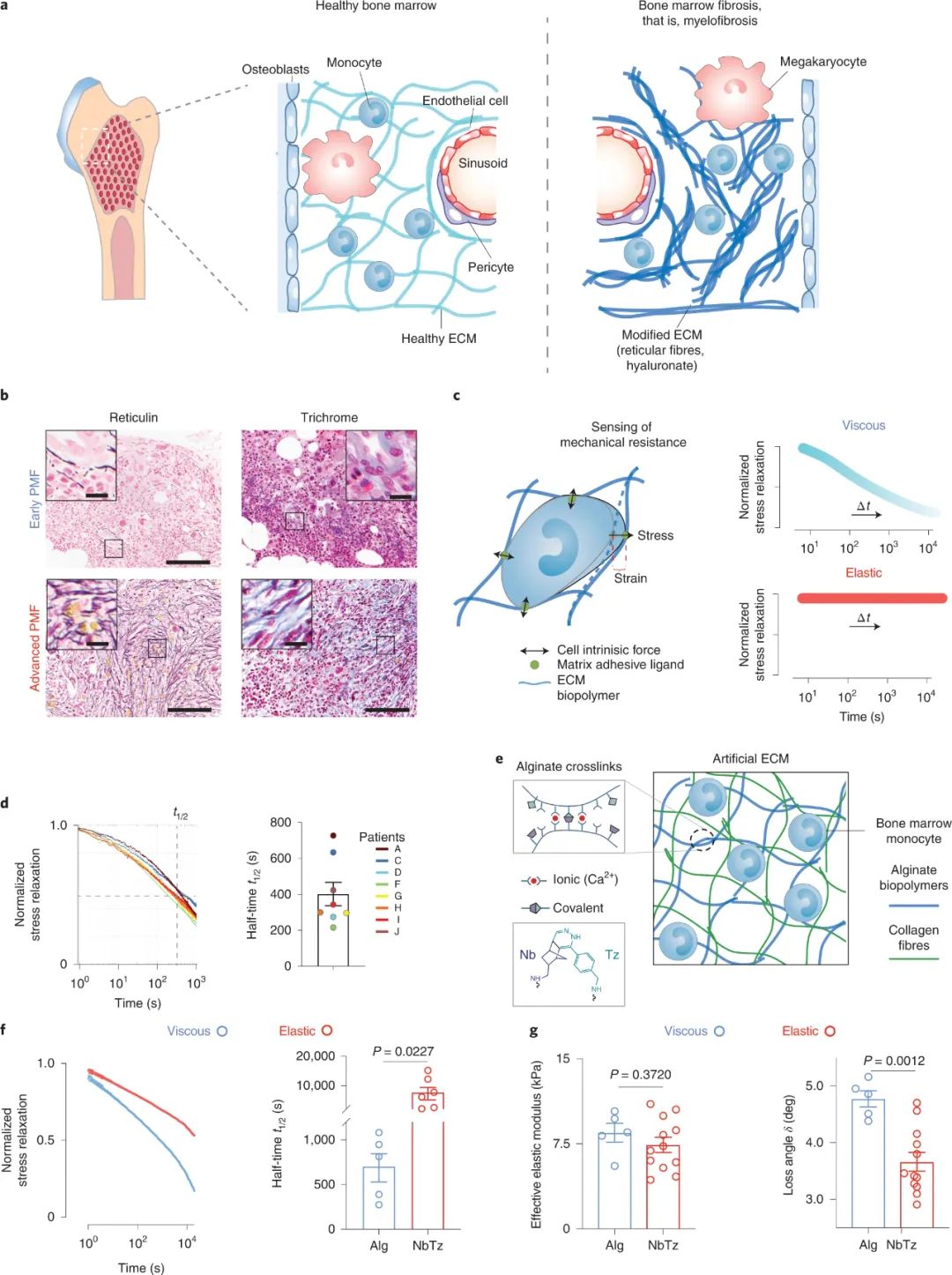
图|互穿纤维状胶原蛋白和点击修饰的藻酸盐网络水凝胶可调节 ECM 的机械抗力
参考文献:
Nam, S., Seo, B.R., Najibi, A.J. et al. Active tissue adhesive activates mechanosensors and prevents muscle atrophy. Nat. Mater. (2022).
https://doi.org/10.1038/s41563-022-01396-x
个人简介












