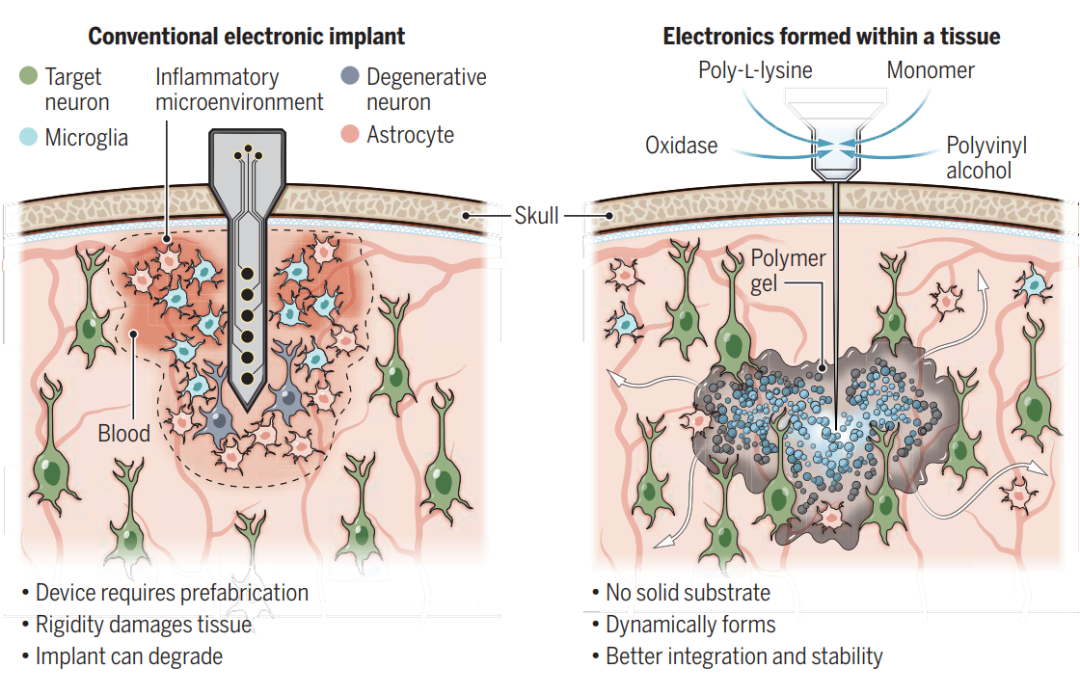
植入感兴趣神经元附近组织的电子设备旨在与神经系统交换信号。这种生物电子设备不仅有助于神经通信的研究,它们还可以在一种称为生物电子医学的治疗方法中劫持神经回路。这些应用的成功取决于植入设备的稳健性及其与身体的兼容性。传统的生物电子设备具有承载导电膜的固体基板。它们的刚性会损坏软组织并降低植入物的长期性能。
为了规避这一限制,导电聚合物已在目标生物系统内形成,作为单体从溶液中引入并在体内聚合以衍生“浸满”电极,甚至与神经组织双连续融合。然而,聚合需要化学能和或电能,这可能对敏感的神经组织有害。为了进一步推进体内聚合的概念,对动物进行基因工程以表达酶,这些酶可促进秀丽隐杆线虫体内靠近目标组织的特定细胞中的局部聚合。然而,由于它依赖于基因工程,这种技术不能在伦理上扩展到人类以提供与大脑的先进接口。
在利用内源性酶活性催化前体的氧化聚合以在体内产生混合离子-电子传导聚合物方面取得了进展。过氧化物酶利用局部 H2O2作为催化剂产生自由基单体,自由基单体进一步聚合和聚集形成与组织结合的导电聚合物。要生产真正多功能的混合离子-电子传导电极系统,还必须迈出一大步,该系统将满足高性能、微创且稳定的自组织体内神经接口系统的所有要求。
因此,建议这种电极技术将表现出以下特征:(a)作为与目标神经组织环境相容的流体分配,并可以在注射部位的所需距离内扩散;(b) 仅包含并产生无毒成分以驱动聚合和交联;形成一个电极,该电极是 (c) 均匀的,(d) 长期稳定的,和 (e) 胶凝(软)的,具有 (f) 高电导率和高体积电容,同时 (g) 在不同长度尺度上与神经结构共形连接。
成果简介
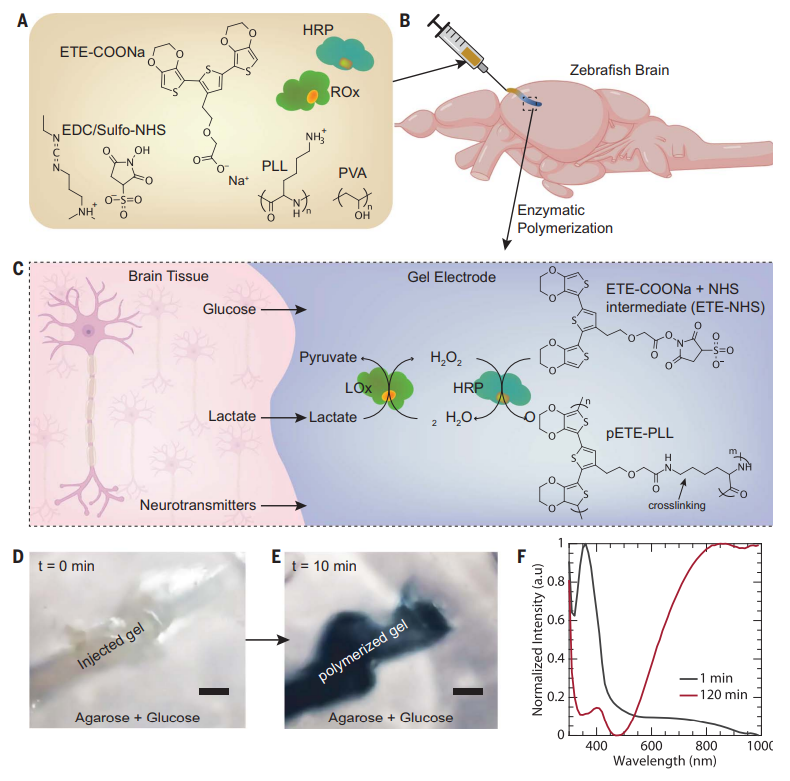
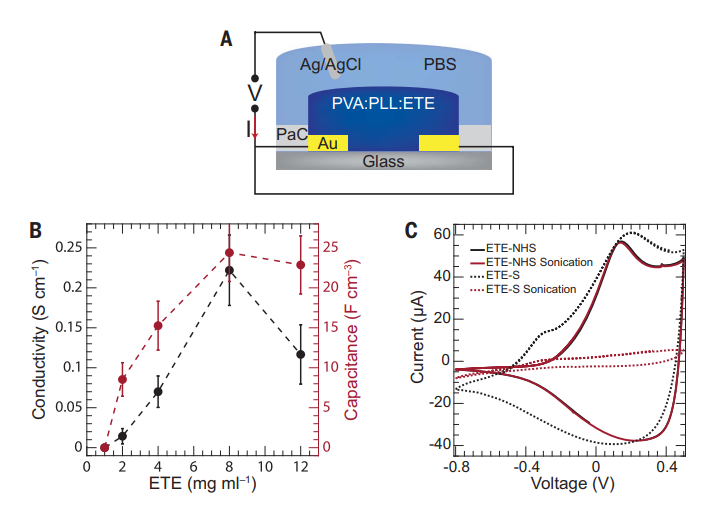
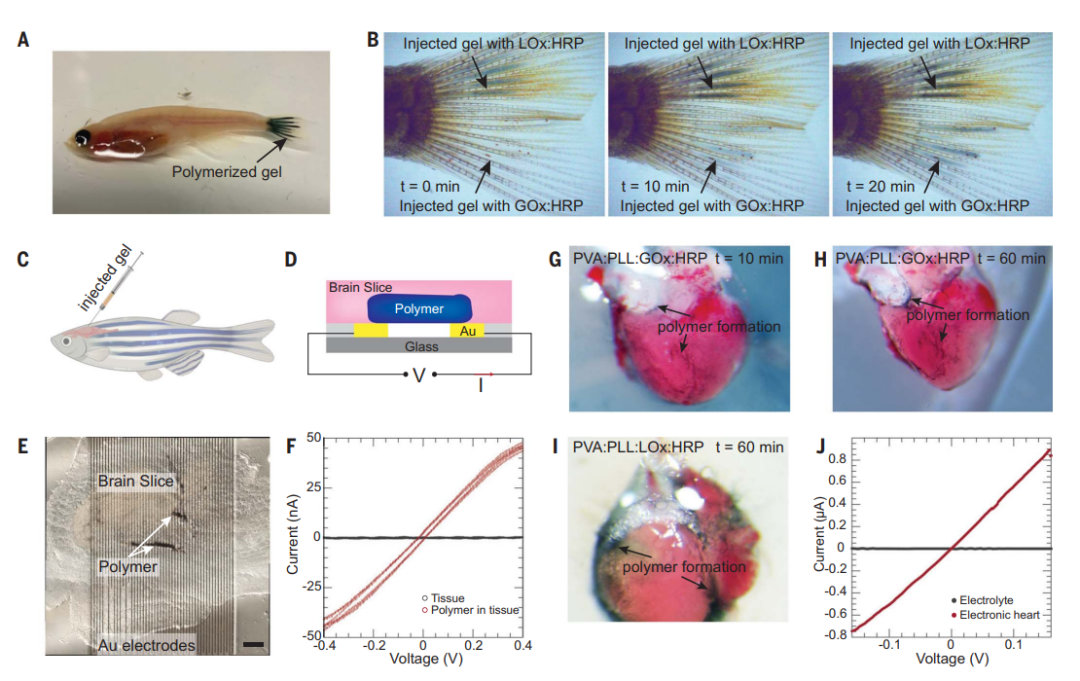
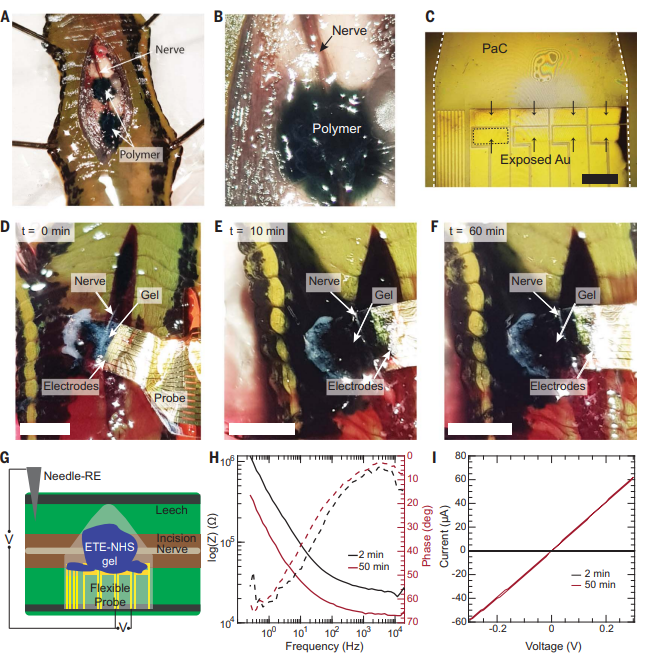
鉴于此,瑞典林雪平大学Magnus Berggren等人报告了一种在周围神经系统 (PNS) 和中枢神经系统 (CNS) 内产生自组织、高性能电极结构的方法,该方法适用于广泛的组织和动物模型。该方法依赖于注入多组分混合物,该混合物旨在满足上面列出的所有标准 (a) - (g)。该混合物包括具有 2-乙氧基乙酸钠盐侧链的 ETE 衍生物 [ETE-COONa:解决了 (a)、(b)、(d)、(f)的要求]、聚(乙烯醇)[(PVA):解决(c),(e)],聚-L-赖氨酸[(PLL:解决(d),(e),(g)],辣根过氧化物酶[HRP:解决(b)],氧化酶[ROx:解决(b)],和EDC/ NHS [解决(d)]。ETE-COONa的聚合由 ROx-HRP 酶级联介导,其中 ROx 消耗生理靶标内的内源性代谢物,局部产生 H2O2,然后在HRP氧化ETE-COONa时充当电子受体。研究人员表明,通过利用神经组织周围的酶促聚合和交联,可以在多种模型生物体内制造软电极。研究人员使用ETE-S的单体,并通过在动物组织中引入氧化酶酶和双氧水来催化ETE-S的聚合。为了提高聚合物的稳定性,研究人员还添加了一种名为ETE-COONa的单体和PVA:PLL的聚合物基质。通过注射酶和单体溶液的混合物并在适当的条件下催化反应,可以在注射的组织中形成一种软的电导聚合物凝胶电极。该方法的优点是可以形成非常细的电极,且能够在体内进行形成,因此可用于记录动物神经元的电活动。研究人员进行了多种实验来证明这种聚合物的形成,包括荧光成像、紫外-可见吸收光谱、流变学测量等。研究人员介绍了电化学凝胶的制备和性能特点。研究人员通过混合MES缓冲液中的不同组分来制备这种电化学凝胶,但由于其中的一些组分之间存在电荷相互作用,因此会形成颗粒并使悬浊液变浑浊。研究人员利用密度泛函理论和分子动力学计算确认了这种凝胶的聚集现象。为了改善凝胶悬浊液的均匀性,研究人员添加了PVA,并在金微电极阵列上测试了不同ETE-NHS浓度下电化学凝胶的电学特性。结果表明,当ETE-NHS浓度为8mg/mL时,凝胶的电导率为0.25 S/cm,比电容率为25 F/cm3。这种电化学凝胶可以作为有机电化学晶体管的通道材料,具有潜在的应用价值。该研究在活体斑马鱼中注射凝胶,验证了酶触发的体内聚合。研究人员注射了混合物凝胶到斑马鱼的尾鳍和脑部,并观察到凝胶在体内聚合,导致颜色变暗。葡萄糖和乳酸都被证明可作为催化剂,其中乳酸诱导的聚合速度相对较快。通过测量电流,研究人员还观察到了形成聚合物后的电学性质。研究人员还发现,含有葡萄糖氧化酶的凝胶在斑马鱼的脑部和心脏中无法诱导聚合,而含有乳酸氧化酶的凝胶能够诱导聚合。此外,研究表明,聚合物对斑马鱼没有毒性。随后,研究人员尝试使用药用水蛭作为模型,在神经组织和金电极之间的界面处诱导凝胶离体聚合。他们发现,以 LOx 作为主要酶的凝胶会在水蛭的连接神经周围和水蛭肌肉中聚合。柔性探针上的图案化 Au 电极用于通过在神经周围聚合的凝胶与水蛭神经连接,并在聚合过程中监测 Au 电极的阻抗。通过在两个相邻电极之间施加电压扫描来验证 Au 电极之间的连接。然后还使用图案化的聚合物电极来研究聚合凝胶是否可以作为扩展电极来刺激半完整水蛭模型中的连接神经并诱导肌肉收缩。结果表明,聚合图案化的凝胶电极可以刺激神经并诱导肌肉收缩,与对照金电极相比,刺激阈值没有明显差异。该研究表明,体内聚合凝胶可以改善电流电极的特性和性能,但需要进一步优化。图|水蛭神经系统周围的体内聚合和柔性探针上电化学特性的动态变化研究人员提出了一种酶催化的聚合策略,利用内源代谢物质在生物体内形成无底物有机电子材料。将含有酶和小分子电活性单体的凝胶注入生物组织中,内源代谢物诱导单体聚合,形成无需刚性底物的有机电子凝胶。该方法在琼脂凝胶、细胞培养、斑马鱼和水蛭模型系统以及哺乳动物肌肉组织中进行了验证,并作为OECTs的通道材料,展示了内源催化聚合法的广泛适用性。研究表明,这种电极技术与生物体完美结合,性能和兼容性均满足无缝集成的要求,超越了薄膜和基板生物电子学的当前技术水平。该方法不需要对目标细胞或组织进行基因操作,更易于转化。研究人员认为,这种在局部和体内形成的有机电子系统将为电子学与生物学的接口开创新的模式,无缝地模糊了生物和技术或电子材料和系统之间的区别。
参考文献:
Metabolite-induced in vivo fabrication of substrate-free organic bioelectronics. Science 2023.
https://www.science.org/doi/10.1126/science.adc9998