近日,莫纳什大学Daniela Loessner等人在Nature Reviews Materials上综述了基于生物材料的肿瘤组织工程平台的相关进展。

癌症是全球最常见的死因之一,但由于肿瘤异质性、患者间差异、对治疗的抵抗以及疾病进展等因素的困扰,开发治疗方法变得困难。因此,为了进行临床前研究,人们已经做出了许多努力,例如使用肿瘤组织工程建模癌症。在肿瘤组织工程中,生物材料是构建三维癌症模型的关键成分,这些模型可以模拟实体肿瘤的组织维度、组织结构和功能。使用合成聚合物、生物聚合物和多肽等构建单元的多种水凝胶和支架材料用于组织工程和再生医学应用,并作为三维癌症模型的基质。新的工程方法使得可以有理设计含有多种结构和信号组分的水凝胶和支架材料,以更准确地重现肿瘤微环境的异质性,肿瘤微环境是一个复杂的实体或生境,其中包含恶性(或癌症)和非恶性(或基质)细胞。
最初的三维癌症模型仅限于培养癌细胞或与一个其他细胞类型的共培养,这不能充分捕捉肿瘤组织内的复杂细胞相互作用。更先进的多细胞三维癌症模型已经发展出来,使用三元共培养、四元共培养或甚至五元共培养。三维细胞生物学也可以整合第四个维度(4D),实现时间分析,如实时蛋白酶解或信号级联的活细胞成像。
利用生物学增强生物材料设计具有独特优势。材料科学和肿瘤生物学的结合已经产生了先进的方法,以可控的、灵活的和可重复的方式捕捉肿瘤微环境的参数。肿瘤组织工程是一个多学科领域,它将生物学、材料科学和工程学等多个学科相结合,为肿瘤研究和治疗提供了新的方法和手段。通过建立更真实、更准确的三维肿瘤模型,肿瘤组织工程可以帮助研究人员更好地了解肿瘤微环境,发现新的治疗方法,并最终提高治疗效果。
在这篇综述中,研究人员重点关注了生物工程和生物学之间的相互作用,以设计改进的3D癌症模型。作者分析了基于生物材料的三维癌症模型是如何被设计为生理相关分析,以再现肿瘤组织的特征。排除了塑料基质上的细胞单层培养或不基于生物材料的3D技术,如悬滴或非粘附细胞培养方法。
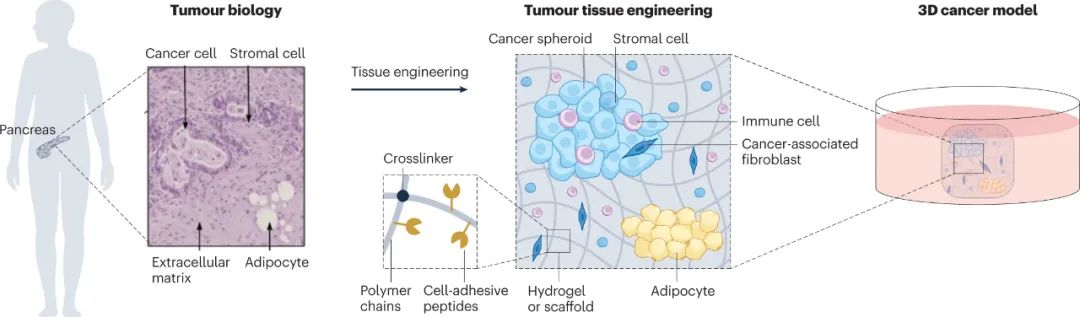
图|肿瘤组织工程的概念
肿瘤生物学中的关键参数
肿瘤的发育受肿瘤微环境(TME)的影响,肿瘤微环境由多种细胞类型组成,包括基质细胞、免疫细胞、内皮细胞、脂肪细胞、细胞外基质(ECM)蛋白和可溶性分子。TME可以调节肿瘤的生长、侵袭和扩散,并在不同癌症类型的肿瘤发生中发挥重要作用。在疾病进展过程中,癌症细胞分泌并重塑自己的ECM,改变其生物力学特性,并产生允许细胞入侵的TME。ECM也是生长因子、细胞因子和趋化因子的库,这些因子在基质分子裂解时释放并激活各种信号通路。癌相关成纤维细胞(CAF)是构成TME重要组成部分的主要基质细胞类型。它们沉积了许多纤维化基质分子,形成一个密集的网络,导致基质硬化、疾病进展和炎症反应。免疫环境在肿瘤发生中也起着至关重要的作用。在一些恶性肿瘤中,持续的炎症与肿瘤的发展和进展有关,免疫细胞浸润并聚集在TME中,建立了促进肿瘤发生的独特生态位。
用于重建TME的工具
作者讨论了由于实体瘤的异质性,工程肿瘤组织面临的挑战,以及整合不同细胞类型以重建肿瘤微环境(TME)复杂性的重要性。各种生物材料,包括天然生物材料、复合生物材料和合成生物材料,已经被开发来模拟TME,但每种类型的生物材料都有局限性。胶原等天然生物材料的机械特性较差,而聚乙二醇等合成生物材料对单个蛋白质的控制更为精确,但难以控制生物活性信号的局部可用性。复合生物材料结合了天然和合成聚合物,在部分复制TME中蛋白质和糖基成分的复杂混合物方面显示出了希望。文章强调了肿瘤组织工程多学科方法的重要性,将材料科学、生物学和医学相结合,以开发药物发现和个性化医学的有效模型。
生物工程化原发肿瘤生态位
使用组织模型重建原发肿瘤生态位需要重建肿瘤组织的细胞和细胞外元素。重要成分包括改变的ECM和癌症,以及与可溶性因子结合的基质细胞,这些可溶性因子可以重建癌症细胞的代谢和炎症特征。组织工程方法通过结合水凝胶基质和支持原发肿瘤部位细胞-细胞和细胞-基质相互作用的多细胞3D培养物,帮助模拟这些生物力学、生物化学和生理学特性。
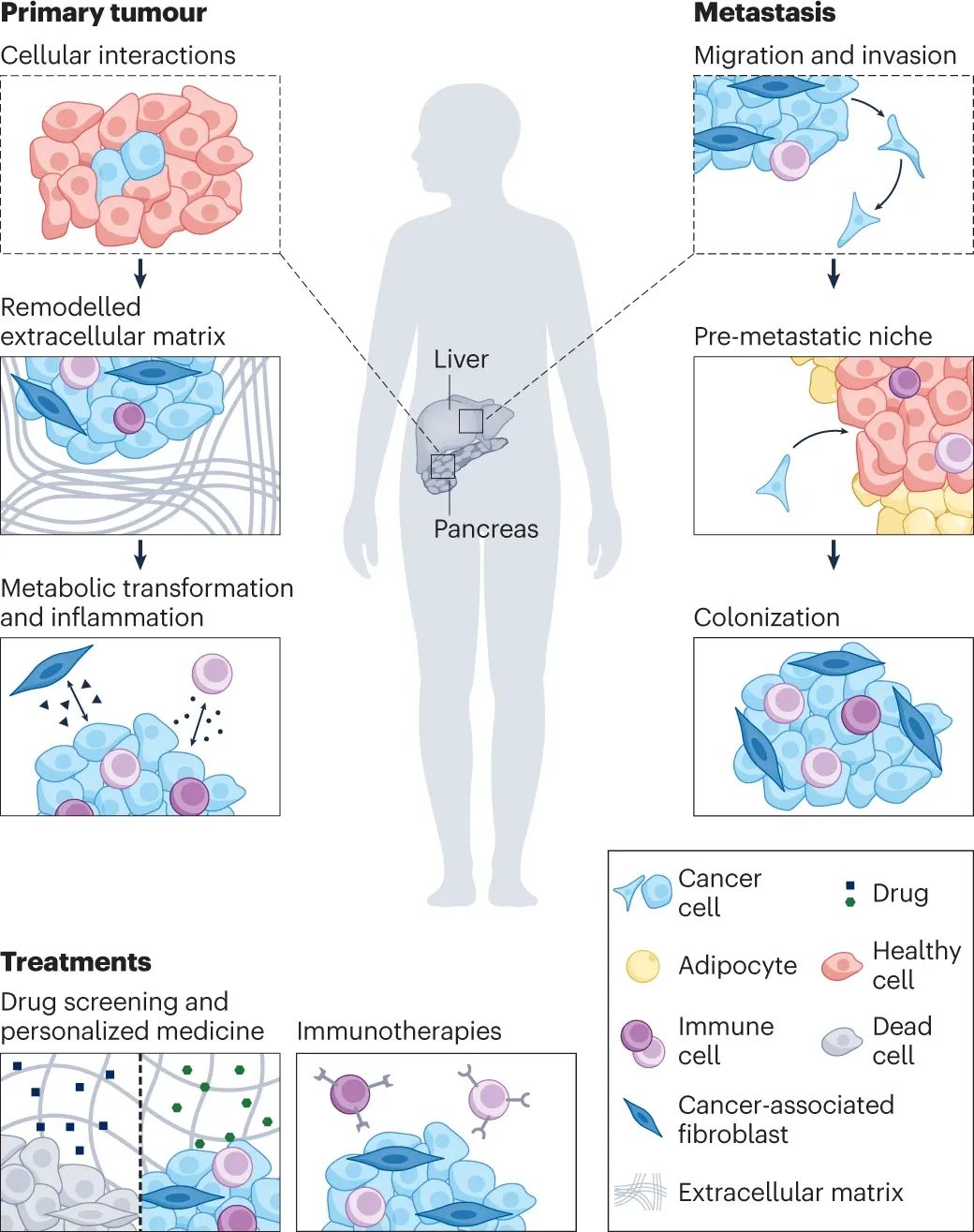
图|应用肿瘤工程模型研究原发性肿瘤、转移和抗癌治疗
生物工程化转移前和转移灶
转移是一个多步骤的过程,其中细胞从原发肿瘤迁移,侵入邻近组织,侵入血管,存活直到到达远处的器官并定植新的器官。细胞启动二次肿瘤的小生境提供了基质信号,这些信号对这种扩张过程至关重要。由于90%以上的患者死于转移性病变,已经做出了巨大的努力来模拟转移前和转移灶。为了模拟这一过程,研究人员已经使用了结合微流体平台和高通量技术的生物材料。
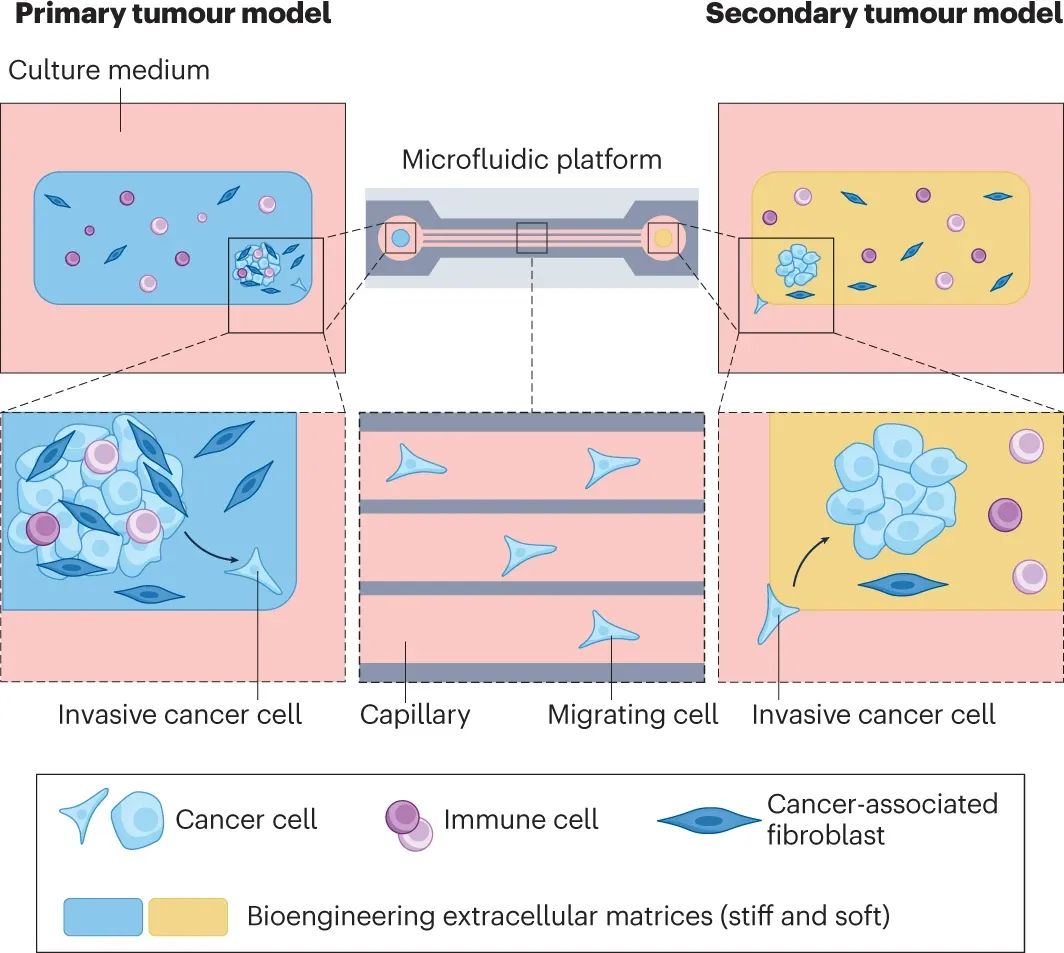
图|生物工程转移前和转移生态位
生物工程化细胞对治疗的反应
迄今为止,3D体外模型尚不足以测试药物反应。目前,在临床前研究中测试的肿瘤药物中,只有不到5%的药物在临床试验中获得成功。因此,需要改进3D癌症模型,以重现临床场景,研究患者对抗癌药物的特定反应。肿瘤工程模型结合微流体平台和高通量组学技术为癌症研究提供了一种创新方法。领域包括:药物筛选和个性化医疗、免疫疗法。
肿瘤工程模型使癌症细胞能够生长、迁移和侵袭,以及研究药物反应。在癌症组织工程中,还采取措施整合肿瘤-基质相互作用和TME的其他元素。为了有效地代表由特定组织TME包围的特定癌症类型,利用了诸如设计具有可修改的机械特性的生物材料基质等策略。此外,使用其他学科的当代组学方法可以改善癌症患者的治疗和临床结果。组织工程技术与癌症研究的结合始于20多年前,通过3D癌症模型和3D支架工程乳腺肿瘤组织。这两个领域之间的协同作用对于加快我们在21世纪的研究进展至关重要。
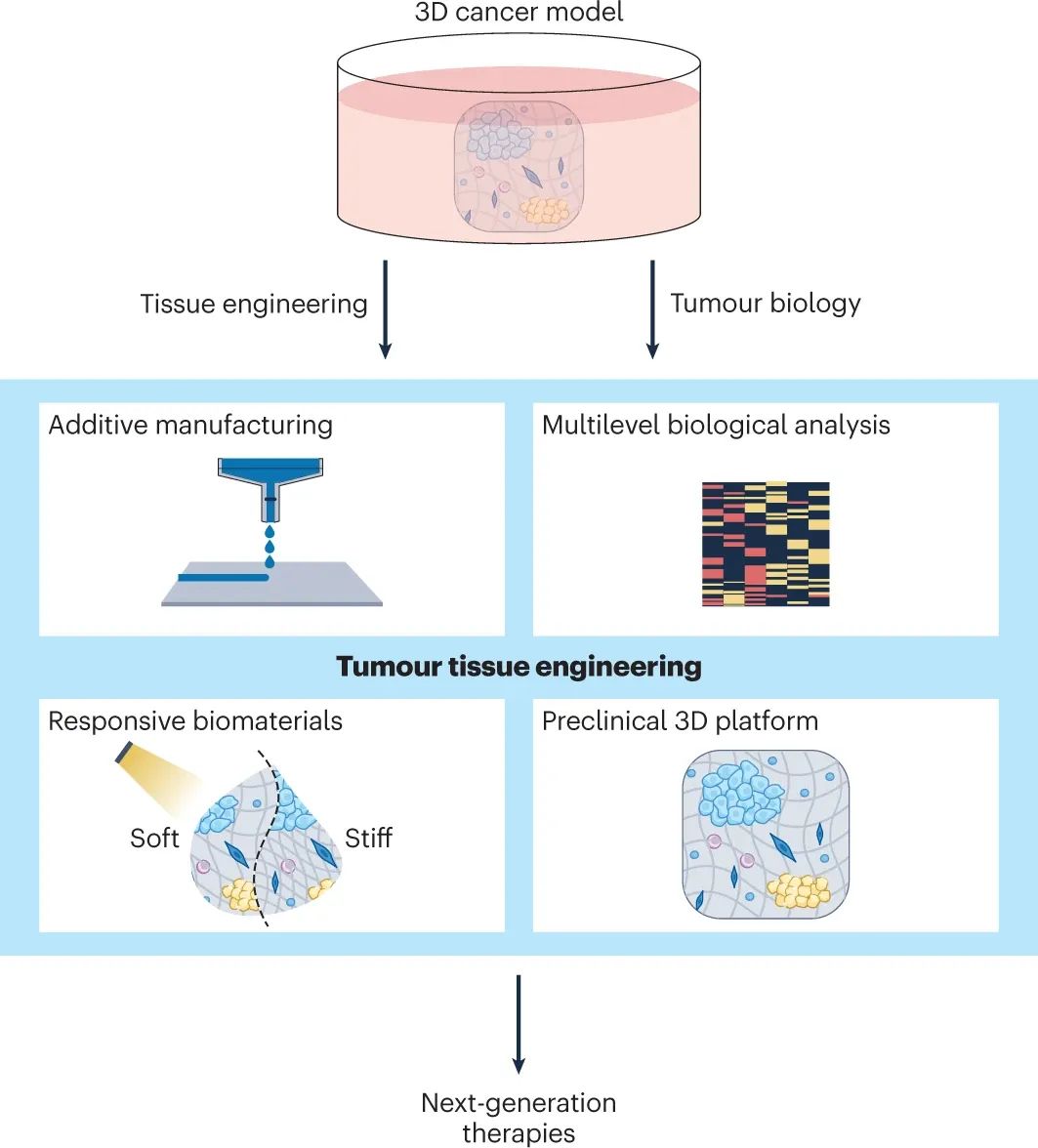
图|组织工程和肿瘤生物学的融合
小结
基于多材料或3D打印支架的先进3D肿瘤学方法正在成为评估新疗法的疗效和安全性、联合疗法的潜力以及高通量药物发现的强大临床前平台。临床前3D平台整合患者来源的细胞,以筛选靶向疗法、个性化药物或免疫疗法。
尽管取得了这些进展,但一些限制因素阻碍了工程师和生物学家之间的协同研究工作。用于交流合作研究数据的术语经常被误用或误导,例如,“仿生”或“生物支架”的含义。目前,仍需要专业用户培训来操作。
当前3D癌症模型的一个主要挑战是,用于研究转移定植过程和复杂性的平台目前大多是微加工的或基于微流体的。这限制了不熟悉这些技术的研究人员以及大规模和长期3D研究的性能。循环肿瘤细胞具有内在机制,可以在血液中生存,找到支持性组织微环境并侵入远处器官。不同转移前途径的数量、转移灶的模式、机械环境和耐药癌症细胞使设计组织特异性转移模型变得极为困难。然而,组织工程骨肿瘤模型代表了癌症细胞如何定植骨龛的转化方法,可进一步用于临床前药物测试。人性化的3D疾病模型将帮助我们了解疾病进展和治疗抵抗的基本、分子和机械机制,无疑将在癌症和转化医学方面取得突破。
另一个限制是设计逼真或生理相关的3D癌症模型的复杂性以及相关的分析困难。包含多种细胞群和生物材料使单个细胞类型和TME成分的行为和功能的确定变得复杂。降解或分离水凝胶和支架以进行细胞恢复和分离的技术,同时限制细胞损失,目前正在完善中。需要进行多层次的生物学分析,以确定细胞对模型参数、TME因素和药物治疗的变化的反应。迄今为止,3D模型结果的验证仅限于结合患者来源的细胞、将结果与临床结果相关联以及使用多组学技术。预测或监管要求也阻碍了它们的广泛使用。
本文回顾的策略强调了聚合物化学家、生物工程师和细胞和分子生物学家之间合作研究的必要性,以充分利用不断扩展的基于生物材料的3D技术。预计这将促进跨学科思维和研究努力。
尽管仍存在一些挑战,但肿瘤组织工程的未来看起来很光明。这种方法将有助于提高我们对基本过程的理解,并为不同类型的癌症开发更有效的治疗方法。3D细胞生物学现在已经进入第四维,组织工程继续提供操纵生物分子和细胞的工具。先进的生物制造技术,如添加剂制造、分子自组装或其组合,提高了构建生物相关结构的能力。这些能力使3D对象和微环境的设计成为可能,在其上可以进行空间和时间控制,并且可以响应和适应外部刺激,例如水、光或温度。在未来,这些新的生物启发材料可能会导致更复杂和定制的3D癌症模型。
参考文献:
Curvello, R., Kast, V., Ordóñez-Morán, P. et al. Biomaterial-based platforms for tumour tissue engineering. Nat Rev Mater (2023).
https://doi.org/10.1038/s41578-023-00535-3











