大多数人类脊髓损伤 (SCI) 病例在解剖学上是不完整的,这意味着损伤附近、上方和下方的神经元回路中的某些连接得以保留。然而,至少有两个主要的病理过程会阻止这些备用连接发挥作用。首先,创伤性损伤导致的细胞死亡和血管破裂会引发炎症,并通过一个称为继发性损伤的过程产生活性氧(ROS)等细胞毒性因子,进一步损害原发性损伤中未发生的脊柱连接,加剧功能缺陷。
在过去的十年中,人们付出了巨大的努力来开发可以挽救幸免的脊柱连接的保护性治疗策略,例如神经保护材料的移植。然而,这些程序可能会进一步损伤受伤的脊髓并导致不可预测的副作用。其次,SCI 会引发兴奋性的巨大变化,破坏受损脊髓中神经回路的整体平衡。先前的研究报道,通过 KCC2 的基因激活抑制作用的抑制性而非兴奋性中间神经元,可以增加整体兴奋性,并将最初休眠的中继或内源性脊髓回路转变为 SCI 后的功能状态。然而,这种策略在临床可转化的 SCI 模型中是否有效尚不清楚。此外,选择性靶向抑制性神经元并改变其活性的微创药理学方法的发展仍然是该策略临床应用的瓶颈。
将药物伪装成神经递质可以促进它们输送到合成这些神经递质的神经元中。因此,浙江大学王绪化等人假设可以使用类似的策略来递送靶向抑制性中间神经元的药物。具体而言,研究人员将药物CLP-257与γ-氨基丁酸(GABA)或多巴胺偶联,后者是一种经验证的KCC2激活剂,可降低细胞内氯离子浓度并降低神经元兴奋性,据报道在运动控制中发挥重要作用。

为了促进微创给药和 ROS 响应性释放,研究人员设计并合成了一种具有聚乙二醇(PEG)基亲水链段和具有硼基ROS清除剂的疏水链段的两亲性嵌段共聚物,以包封疏水性前药。这些基于胶束的纳米药物可以静脉注射,并且 ROS 响应性地在损伤部位释放前药。该药理学方法在患有 SCI 的大鼠中引起了实质性的功能恢复,表明了针对 SCI 和其他神经系统疾病的治疗有希望的方向。
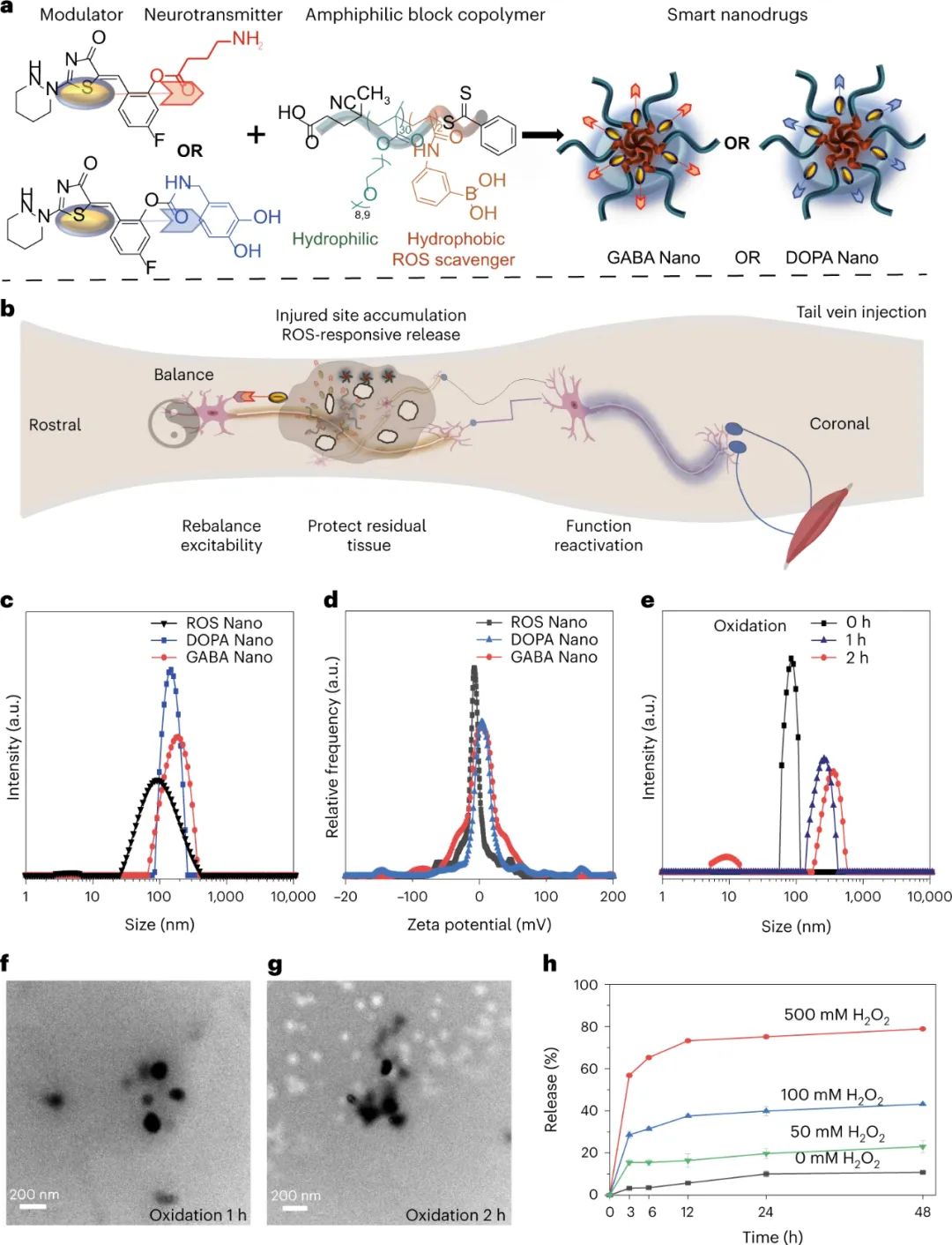
图|智能纳米药物的设计和表征
为了验证纳米载体的ROS响应性,研究人员在大鼠身上使用了严重挫伤性 SCI 模型,并给予了载有前药 GABA 和多巴胺盐酸盐 (DOPA) 的纳米药物。使用荧光染料 Cy5.5 研究了纳米药物的分布和释放曲线。结果表明,纳米药物在注射后不久就在脊柱病变部位周围聚集,约6小时达到最大浓度,并持续48小时。分布分析揭示了在邻近病变的延髓区域的聚集偏好,这可能是由于脊髓血管闭塞。进一步的分析包括对带有 GABA 能和多巴胺能神经元标记的脊髓切片进行免疫染色。共定位分析表明,很大一部分用 GABA Nano 或 DOPA Nano 标记的细胞确实是目标神经元。定量分析表明,大约 80% 的标记细胞是预期的目标神经元。纳米药物表现出高选择性和效力,毒性极小。
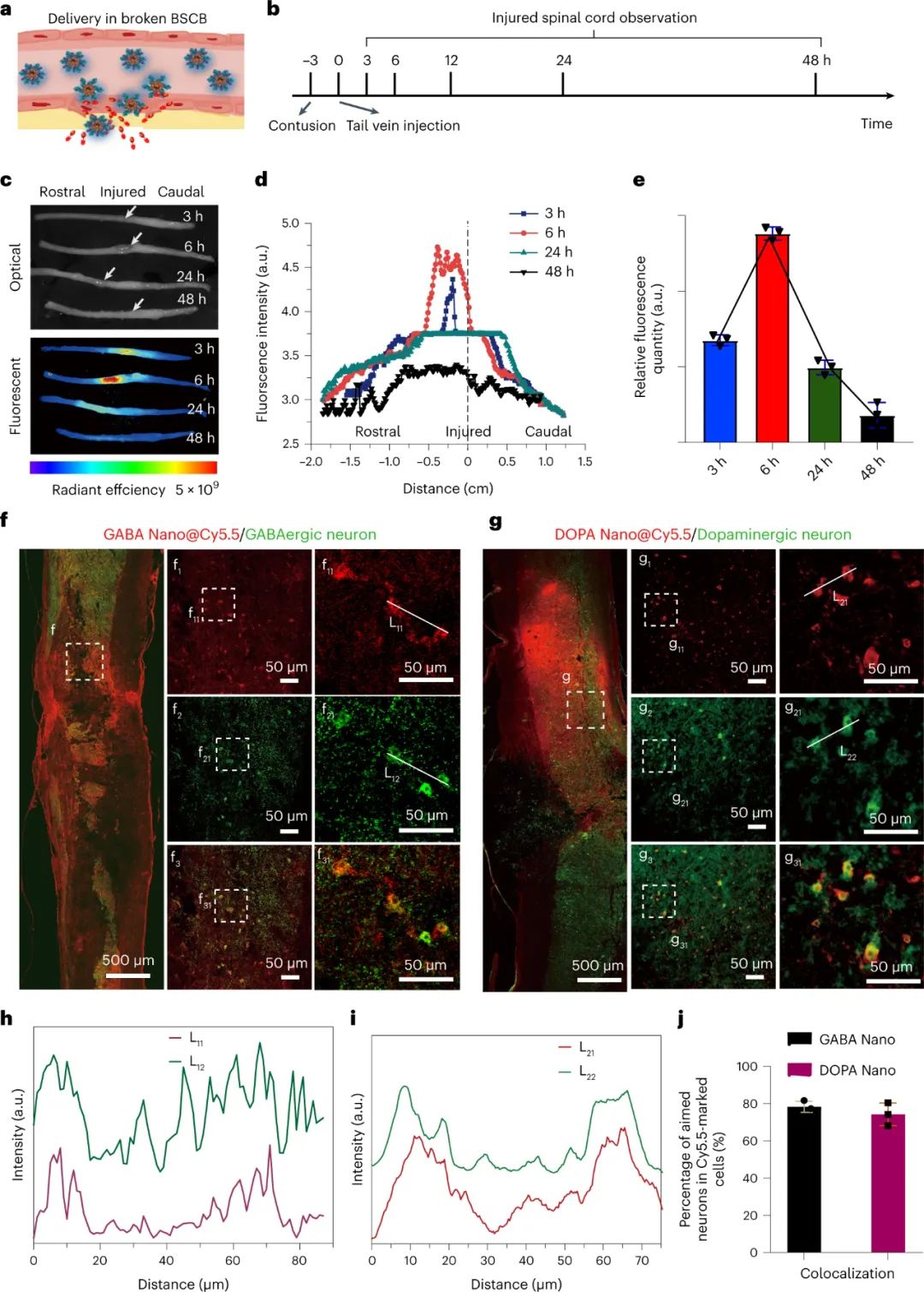
图|智能纳米药物在脊髓损伤部位积聚,并选择性地靶向特定神经元
此外,研究发现,即使在脊髓损伤晚期,纳米药物可以通过响应ROS释放药物前体,渗透到受损脊髓中。研究人员观察到纳米药物可以将荧光染料运送到受损脊髓的邻近区域,尤其在SCI后7天注射的大鼠中荧光强度最高。这种现象与预期相反,但解释是药物穿透与纳米粒子解聚和释放小分子药物的效率相关。研究还发现纳米药物优先靶向神经元而不是星形胶质细胞,并能在恢复的血脊髓屏障(BSCB)中渗透,而在未受损的脊髓中没有观察到荧光。这些结果表明,该药物传递系统可以在脊髓损伤晚期将疏水性小分子化合物送入脊髓。
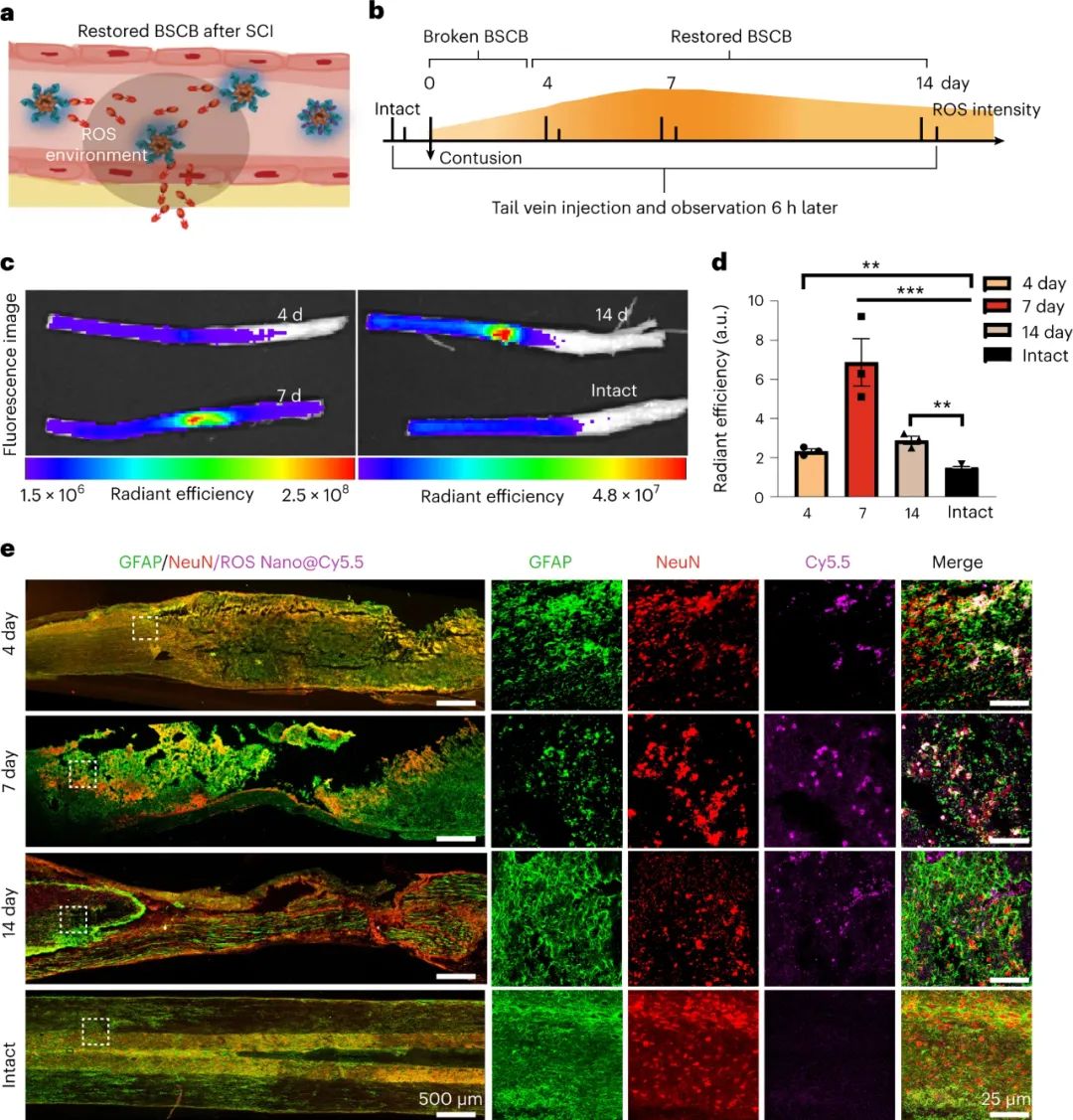
图|ROS响应性纳米药物递送系统即使在BSCB恢复后也能将小分子递送到脊髓中
研究结果表明,经过纳米药物治疗的大鼠在脊髓损伤后9周,与对照组相比,脊髓形态变形明显减少。对脊髓切片进行H&E染色显示,治疗组的囊性腔明显较小。进一步定量分析发现,在PBS治疗组,腔体占据了约27.3%的脊髓体积,而在ROS纳米粒子治疗组,腔体体积仅为PBS治疗组的一半左右,约为15.8%。此外,治疗组显示了更多的灰质和减少的病理组织。此外,通过追踪下行轴突,研究发现ROS纳米粒子治疗组的大鼠下行轴突数量明显增加。这些数据进一步验证了纳米药物治疗脊髓损伤的神经保护效果。

图|ROS纳米治疗保护备用组织/轴突免受二次损伤
研究人员发现,在脊髓损伤后使用神经元靶向治疗可以改善下肢运动功能。他们发现,GABA纳米粒子治疗在严重脊髓损伤模型中显著改善下肢步态功能,而DOPA纳米粒子治疗则仅能引起踝关节运动。详细分析显示,接受GABA纳米粒子治疗的大鼠在体重支撑、足趾高度和踝关节振幅等方面有显著改善。肌肉电图记录显示,接受GABA纳米粒子治疗的大鼠的踝关节肌肉显示出一定的活动。这表明GABA纳米粒子治疗通过神经保护和神经调节作用协同作用,促进了功能恢复。
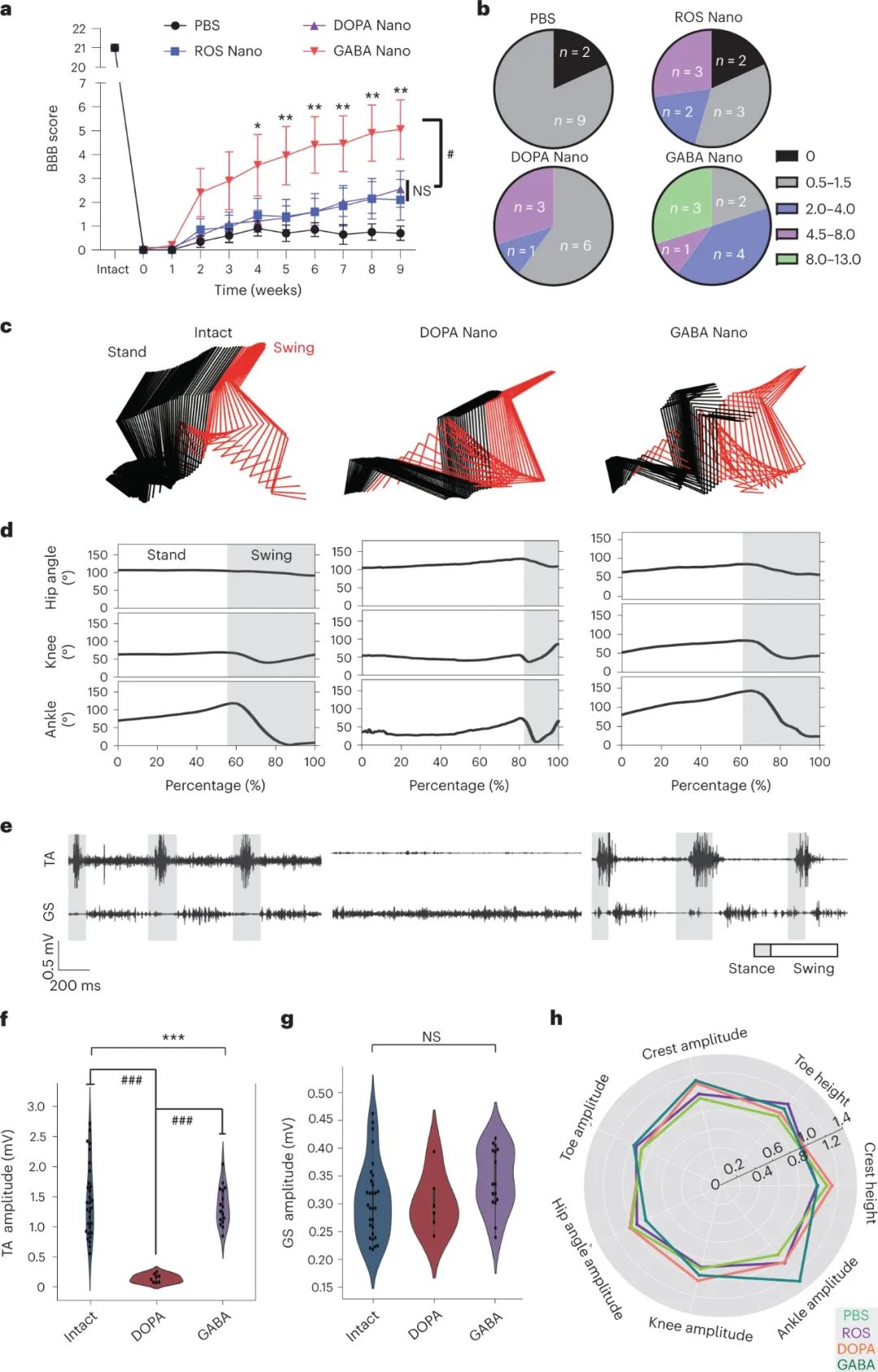
图|GABA纳米治疗可改善严重挫伤性脊髓损伤大鼠后肢运动功能的恢复
最后,研究人员发现,GABA纳米粒子治疗通过减少抑制性中间神经元的兴奋性,在脊髓损伤后促进功能恢复。他们利用c-Fos蛋白免疫反应作为检测脊髓中间神经元活动的指标。结果显示,GABA纳米粒子治疗降低了T8背角中c-Fos阳性神经元的密度,并增加了中间和腹侧脊髓中的存在,使其与原始神经元的分布更加接近。此外,GABA纳米粒子治疗还显著增加了L2节段中的c-Fos阳性神经元数量。这些结果表明,GABA纳米粒子治疗能够改变脊髓损伤引起的不规则活动模式,使得保存的神经回路能够与脊髓局部回路相互融合,并重新参与腰骶中枢模式生成器的功能。
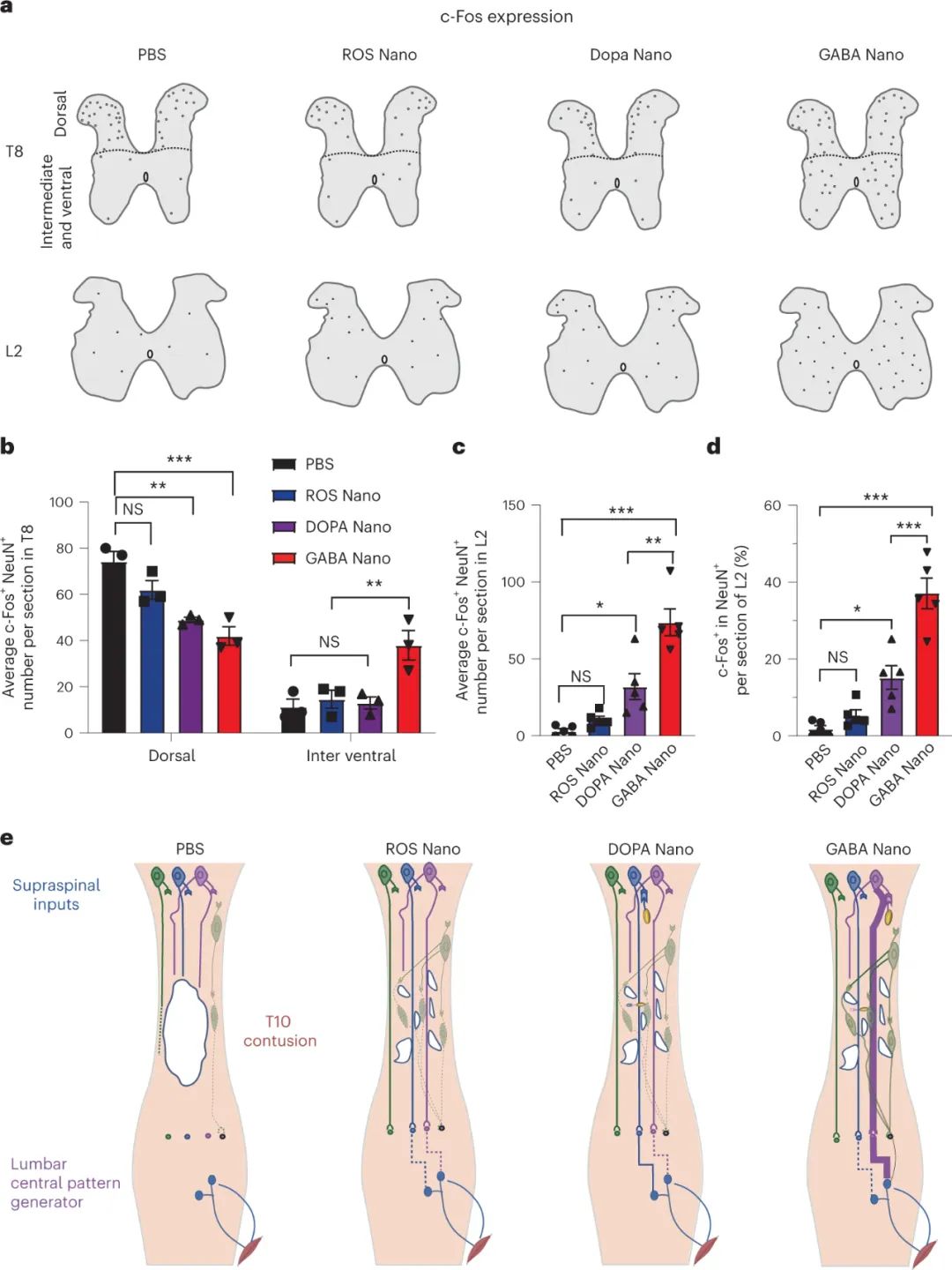
图|GABA纳米治疗可重新平衡神经元活动,并激活挽救的残余脊髓回路以发挥功能
综上所述,本文提供了一种纳米系统,用于在 SCI 治疗中将药物输送到脊髓,并提出了一种开创性的药理学方法,通过靶向特定神经元亚型、保护幸存组织和重新平衡神经调节作用来治疗 SCI。这允许源自损伤部位保存的轴突和中间神经元的脊髓回路正确地整合到脊柱网络中并触发后肢运动。虽然 CLP-257 已被证明可以穿透 BSCB,但在进入临床试验之前,将纳米药物系统的递送效率与裸 CLP-257 药物的递送效率进行比较至关重要。
参考文献:
Zuo, Y., Ye, J., Cai, W. et al. Controlled delivery of a neurotransmitter–agonist conjugate for functional recovery after severe spinal cord injury. Nat. Nanotechnol. (2023).
https://doi.org/10.1038/s41565-023-01416-0











