
氟化反应在药物研发和功能小分子设计中具有重要作用,但天然存在的有机氟化合物相对稀缺,因此需要开发新的合成途径。过去的研究主要集中在烯烃的氟化反应中,通过催化剂诱导的芳基离子重排实现了芳基的二氟化。碘(I)/碘(III)催化已成功地从烯烃底物生成氟化产物。烯烃被提议作为苯乙烯的合适代理物,可以简单地生成同丙炔基二氟化物。
如何实现烯烃的双氟化
氟化为定制API的理化性质和扩大功能驱动合成的化学空间提供了强大的工具,从而发现了和开发新的和改进的药物化合物。尽管氟源可及,但天然存在的有机氟的稀缺性以及存在5,000多种含卤素的天然产物可归因于这样一个事实,即自然界尚未进化出实质性的氟生物化学。虽然氯和溴等其他卤素常见于天然产物中,但氟掺入有机分子的情况相对较少。
近日,德国明斯特大学Ryan Gilmour团队报道了一种通过稳定的乙烯基阳离子实现1,2-炔基转移的方法,从而取代了基于苯离子重排的区域化学范式。此外,该方法还扩展了催化二氟化反应的影响力,使得直接获得同伴二氟化物成为可能。论文还介绍了该方法在药物合成中的应用,并探索了不同底物的适用性。因此,该论文提供了一种技术路线,可以用于实现炔基转移和二氟化反应,并在药物合成中具有潜在的应用价值。
技术优势:
提出了一种基于催化剂的芳基-氟基化反应,通过在位生成ArIF2物种来促进烯烃的活化和氟化序列。该方法利用稳定的氟离子作为辅助基团,使产物阳离子得到稳定,从而提供了一种简便的合成途径,可以合成具有炔烃基团的二氟代烯烃。此外,该方法还展示了对不同官能团的兼容性,包括电子吸引基团、卤素和小的烷基片段。通过调整反应条件,还可以合成具有复杂杂环结构的化合物,展示了该方法在药物发现领域的应用潜力。此外,该方法还展示了在大规模反应和产物衍生反应中的合成实用性。
研究内容
催化反应结果及讨论
通过使用各种廉价的芳基碘化物、氧化剂和氢氟酸源,以及催化条件,制备了炔烃S1,并进行了反应条件的验证。在这些条件下,可以以88%的收率生成所需的同位素丙烯基氟化物1,而邻位异构体的形成率低于5%。然而,在没有催化剂的情况下,邻位二氟化物的产率为13%。此外,还对电子调控的催化剂进行了筛选,结果表明p-TolI具有优越性,并且p-Me > p-H > p-CO2Me > p-OMe。调整胺:氢氟酸比例或氧化剂会对反应结果产生不利影响。此外,还研究了该转化的范围和限制,并发现胺:氢氟酸比例的微小变化会导致反应活性的差异。在优化条件下,通过改变覆盖芳基基团而保持烯烃取代基不变(R = Me),可以生成一系列的双氟代化合物,并且可以与电子吸引基团、卤素和小的烷基片段(1-10,最高83%)具有功能团的兼容性。此外,该方法还适用于药物相关的杂环化合物,如吡啶、喹啉和吗啉(11-13,最高56%)。此外,还可以将R = Me替换为R = CH2X(X = Br和Cl),以在近端C(sp3)位置上进行官能团化(15和16,最高91%)。最后,还验证了该方法与更复杂的天然产物衍生支架的兼容性(17-19)。
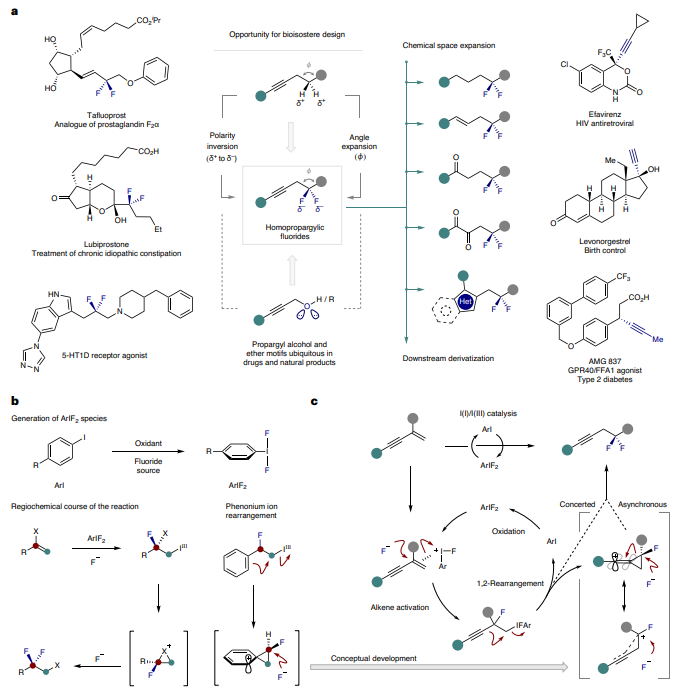
图1 烯炔催化宝石二氟化反应的开发
对炔烃进行双氟化反应的合成实用性验证
实验在4.0 mmol的规模上进行,通过一系列产物衍生反应进行了验证。首先,炔烃20被完全和部分还原为烷烃和烯烃产物34和35。为了展示同源丙炔氟化物在杂环形成中的价值,化合物4通过Ru催化氧化炔烃并与1,2-苯二胺缩合反应,生成了喹啉36。使用四丁基铵氟化物(TBAF)对化合物33进行脱硅化反应,得到了终端炔烃37,收率为85%:然后可以通过铜催化的点击反应将其进一步处理为三唑38。对33的原位去保护和随后的Sonogashira交叉偶联反应进行了处理。
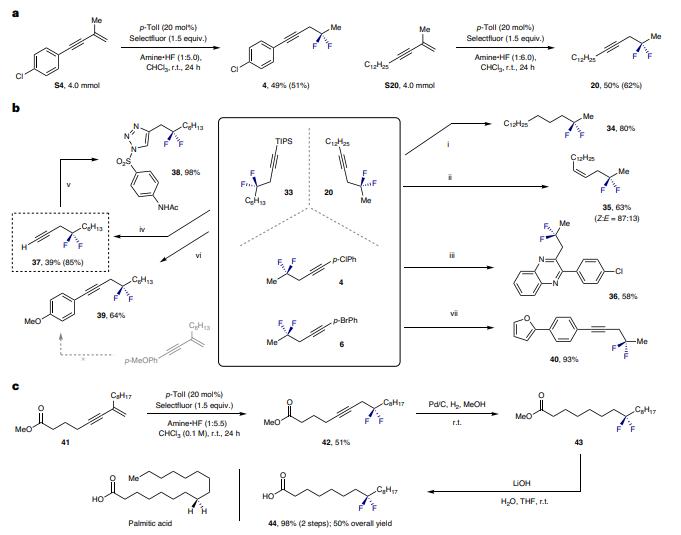
图2 合成应用
反应范围和限制的研究
在这个过程中,对胺:氢氟酸比例的微小变化做出了反应差异的观察。通过保持烯烃取代基不变(R = Me),研究了改变帽基芳基的影响。这使得一系列的双氟基化物得以生成,并且展示了与电子吸引基团、卤素和小的烷基片段的官能团兼容性(1-10,最高达83%)。在产品2的情况下,通过单晶X射线衍射(Table 2; CCDC 2256836)严格确定了分子连接性。令人满意的是,该方法还证明了与药物相关的杂环化合物(如吡啶、喹啉和吗啉,11-13,最高达56%)的兼容性。此外,还可以用R = CH2X(X = Br和Cl)替换R = Me,以在近端C(sp3)位置上创建可官能化的关键结构(15和16,最高达91%)。最后,还验证了该方法与更复杂的天然产物衍生支架的兼容性(17-19)。
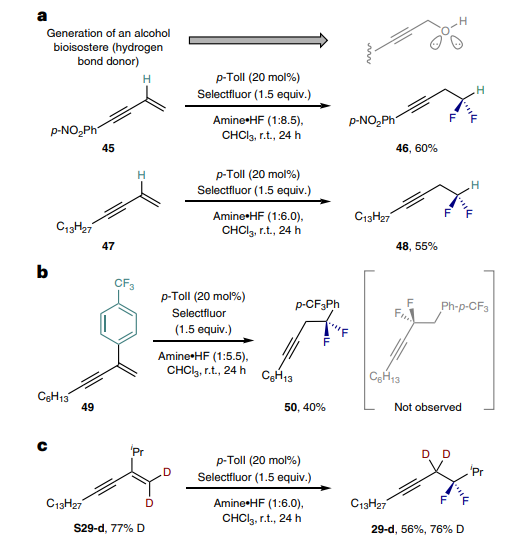
图3 对照实验
总结展望
总的来说,近日,明斯特大学Ryan Gilmour团队利用碘(I)/碘(III)催化剂实现烯烃的1,1-二氟化反应,以合成高附加值的(二)氟化产物;探索烯烃作为苯基代用物的潜力,从而简化合成过程并生成高度多功能的同伦丙炔基二氟化物;强调了氟化反应在药物发现和设计中的重要性,以及天然和合成有机氟化物之间的差异;提出了基于催化剂的氟化反应策略,以实现烯烃骨架重排和1,1-选择性氟化的挑战。这些问题对于开发新的药物和功能小分子具有重要意义。
参考文献:
Zi-Xuan Wang, Keith Livingstone, Carla Hümpel, Constantin G. Daniliuc, Christian Mück-Lichtenfeld & Ryan Gilmouret*. Regioselective, catalytic 1,1-difluorination of enynes Nature Chemistry. (2023).
https://doi.org/10.1038/s41557-023-01344-5











