
向大脑输送纳米颗粒一直是改善脑部疾病和损伤的诊断和治疗结果的技术开发的重要领域。到目前为止,大多数使用纳米粒子进行大脑应用的研究都集中在递送方面——将纳米粒子到达感兴趣的部位并达到预期的效果定义了许多研究的范围。一般来说,基于纳米的递送策略旨在克服全身递送中的高度选择性血脑屏障,并引导大脑微环境以靶向并增加特定脑细胞内的摄取。这种对递送的关注,而不是递送成功(或失败)后发生的情况,忽略了将纳米粒子用于大脑应用的一个关键组成部分:清除。
近日,上海交通大学高小玲、上海中医药大学陈红专、加拿大玛格丽特公主癌症中心郑刚等人试图填补这一知识空白并回答一个重要问题:纳米颗粒到达大脑后会发生什么?

图|纳米颗粒在大脑中的命运
了解纳米颗粒在大脑(人体最受保护的器官之一)中的命运和停留时间对于纳米颗粒的临床使用非常重要:之前的文献表明,纳米颗粒在大脑中的积累和毒性可以改变细胞信号传导、细胞对压力的反应和细胞命运。例如,可用于诊断、治疗或诊断应用的无机纳米材料在大脑中持续停留并可能引发神经毒性,可能阻碍聚合物或脂质颗粒等有机材料可能使用的清除机制。
为了确定纳米颗粒从大脑中清除的机制,研究人员配制了两种有机纳米颗粒——重组高密度脂蛋白(rHDL)和聚乙二醇-b-聚乳酸纳米颗粒(PEG-PLA)——并使用了两种类型的无机纳米颗粒——带和不带PEG的量子点和金纳米颗粒。有趣的是,他们的结果表明,纳米颗粒从大脑中的清除可能取决于成分,而不是任何单一的物理化学特性,例如尺寸、zeta 电位、表面功能化和硬度,所有这些因素都会影响纳米颗粒向特定器官和细胞的输送。
大脑的清除可以通过血管旁途径进行,通常称为类淋巴途径,它是大脑中主要的废物清除系统,驱动脑脊液和间质液之间的可溶性蛋白质和代谢物交换。利用小鼠活体成像,研究人员发现,rHDL 和 PEG-PLA 纳米颗粒在海马内注射后均迅速从大脑中消除,尽管rHDL 和 PEG-PLA 纳米颗粒的平均直径显著不同(分别为 21.4 nm 和 107.5 nm)和通过 zeta 电位测量的平均表面电荷(分别为 -11 mV 和 -28 mV)。相比之下,聚乙二醇化量子点(平均直径 23.4 nm,-24 mV)和金纳米颗粒(9.9 nm,-19 mV)保留在大脑实质中,与血管旁空间的间隙最小。清除率的差异是惊人的:在相同剂量下,即使给药后 8 小时,大脑中残留的有机纳米颗粒也不足 15%;对于无机纳米颗粒,给药后48小时保留了超过70%的注射剂量。这些观察结果在所有测试剂量中都是一致的,即使增加纳米粒子剂量略微降低了清除率。
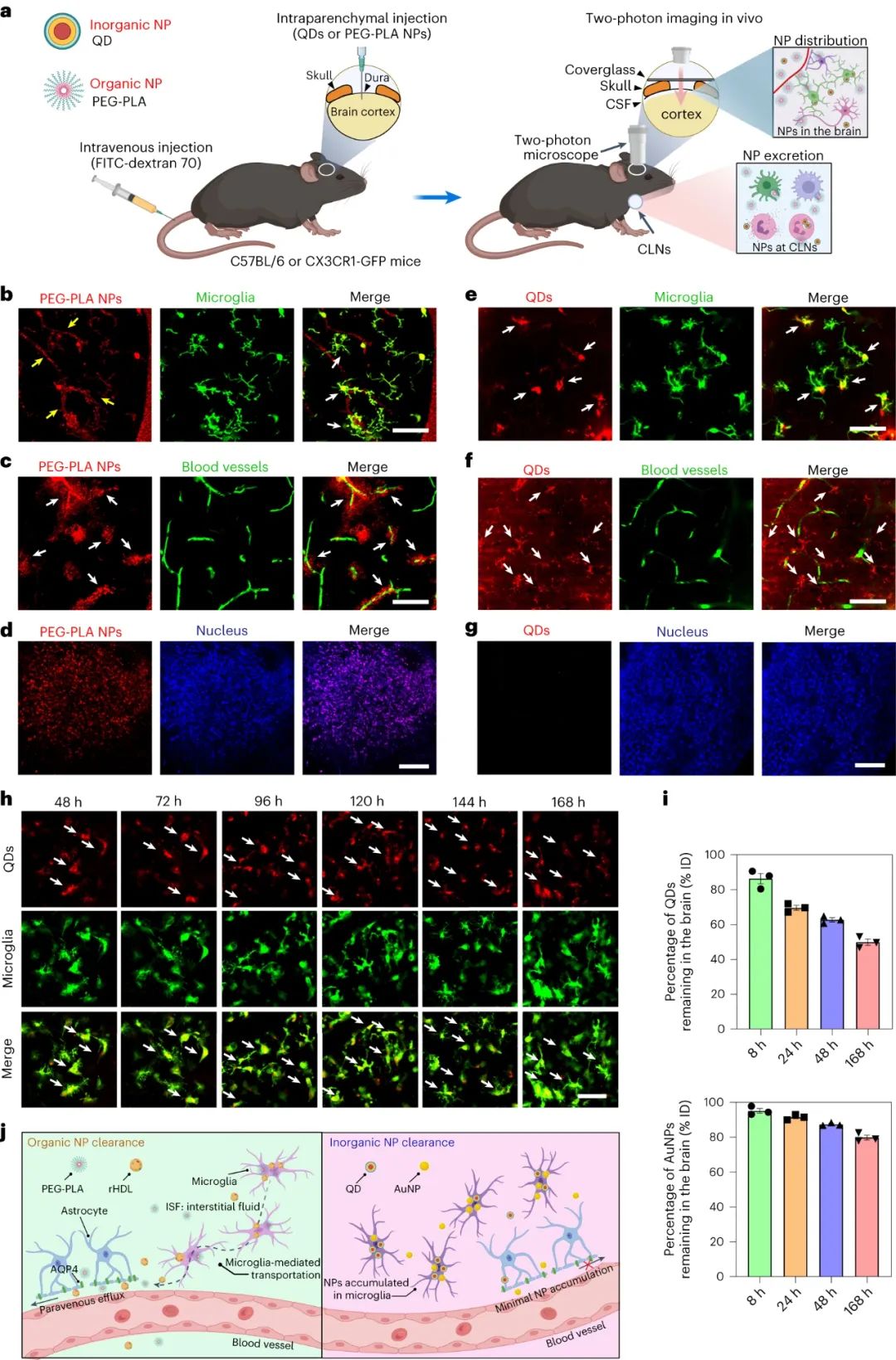
图|无机和有机NPs表现出不同的脑分布和清除率分布
未被清除的无机颗粒被隔离在小胶质细胞中,小胶质细胞是大脑中的吞噬细胞,通常被描述为大脑的常驻免疫细胞。在过去的几十年里,我们对小胶质细胞的了解迅速发展,并且小胶质细胞经常成为纳米颗粒治疗策略的目标,因为它们在维持体内平衡以及对大脑疾病或损伤的反应中发挥着明显的作用。研究人员在体外证明,有机和无机纳米颗粒都在小胶质细胞中内化,但从早期内体或溶酶体运输到晚期内体或溶酶体的无机纳米颗粒的胞吐速度比有机纳米颗粒慢约10倍。
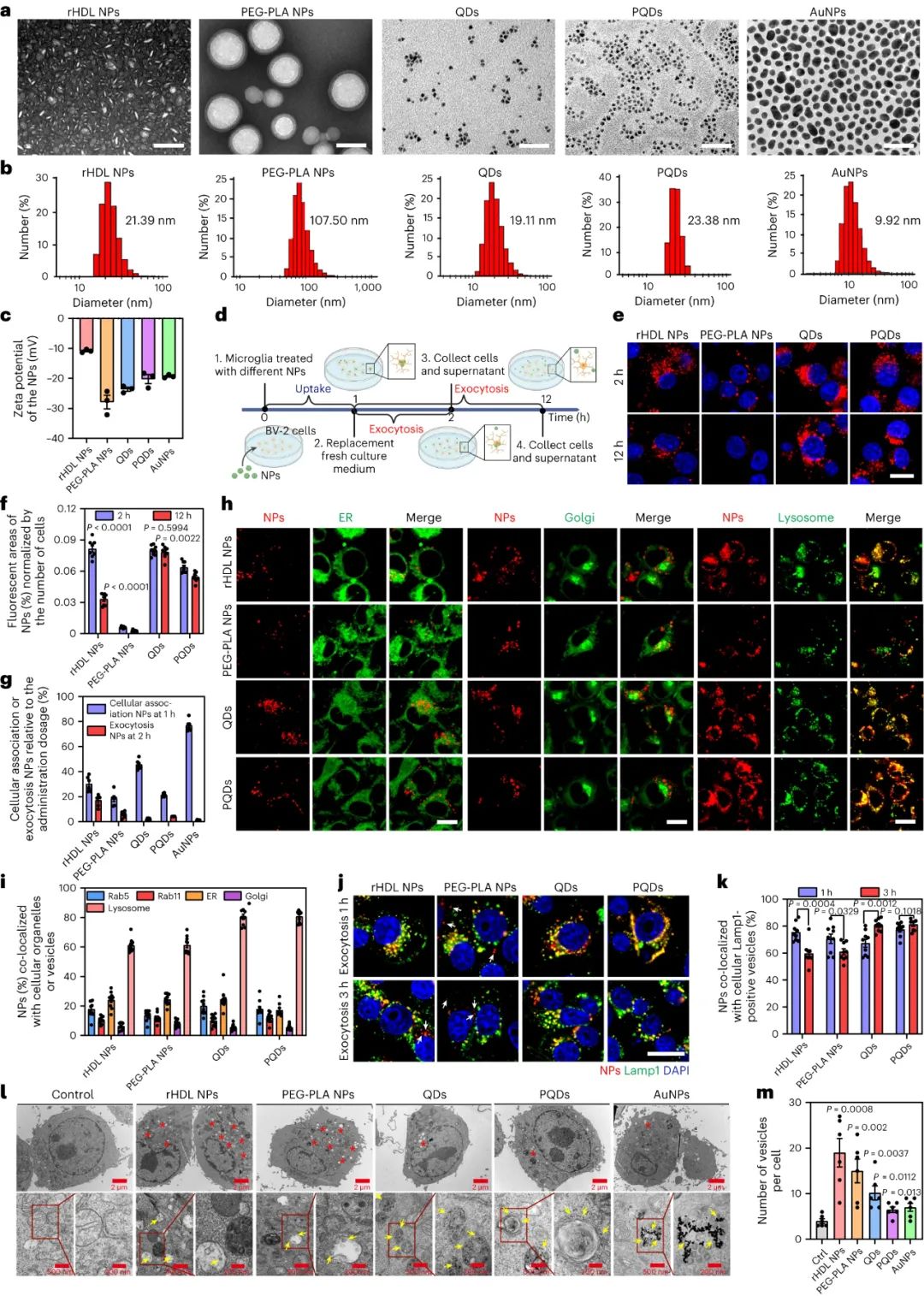
图|无机和有机纳米颗粒在小胶质细胞中表现出不同的细胞内转运和胞吐作用模式
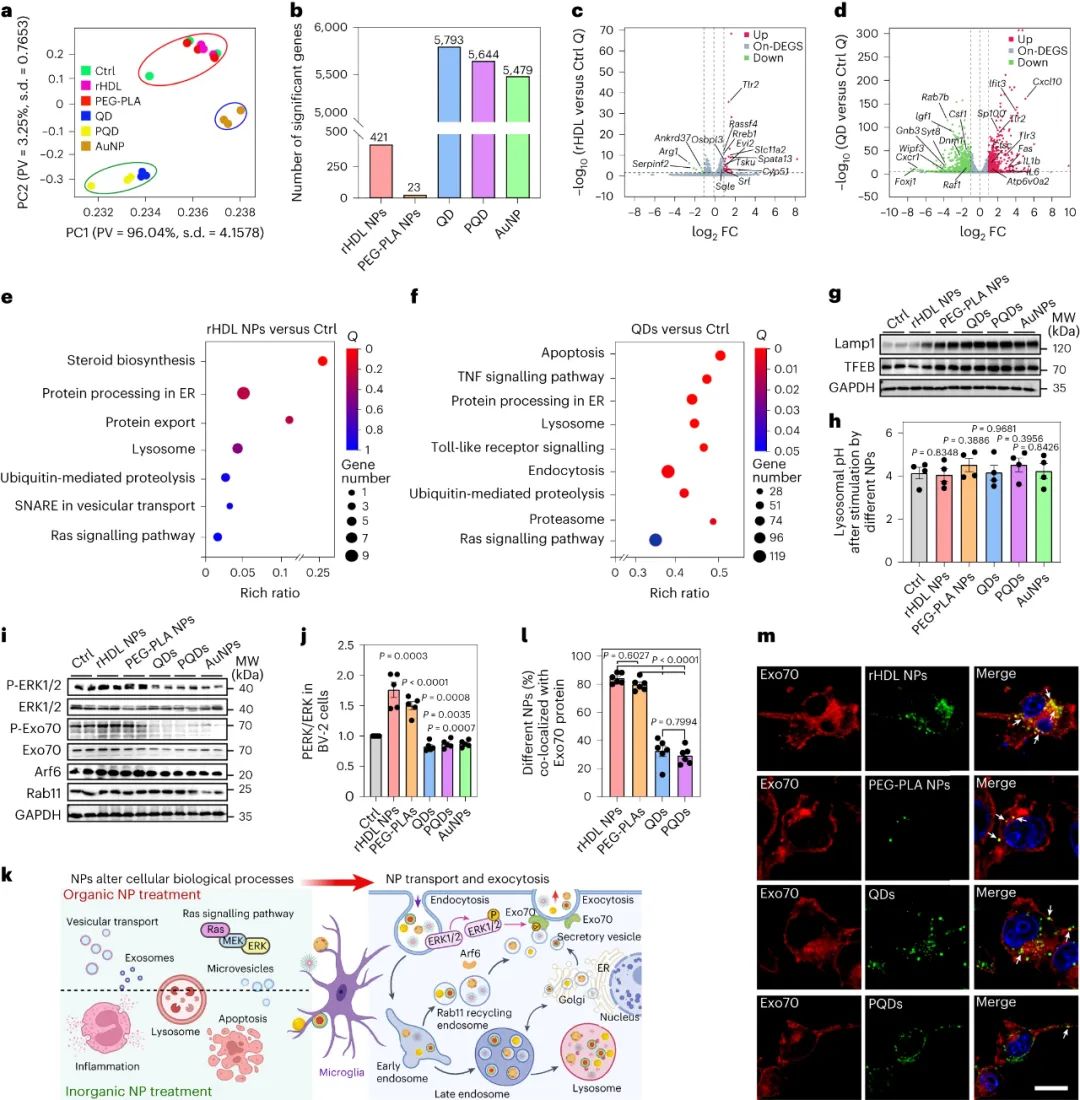
图|NP 治疗改变小胶质细胞信号传导和胞吐作用过程
根据纳米材料成分分离这种改变速率的机制具有挑战性,但研究人员使用RNA序列分析和敲除模型来探索通过小胶质细胞进行纳米颗粒运输和从大脑清除的途径。
无机纳米颗粒内化到小胶质细胞中,驱动了与细胞凋亡、炎症和溶酶体加工相关的小胶质细胞基因表达的变化,以及ERK1/2 信号通路的增加,从而导致细胞外囊泡 (EV) 生物合成和分泌的减少。
在暴露于有机纳米粒子的细胞中,EV 分泌上调,导致小胶质细胞中更快的胞吐作用和更少的有机颗粒积累;事实上,通过非竞争性中性鞘磷脂酶抑制剂治疗或敲除 Rab7 表达来阻止小胶质细胞中 EV 的释放,会导致所有纳米颗粒的累积加剧。在体内,抑制EV释放导致rHDL颗粒在大脑中的更大积聚,并减少对血管旁空间中rHDL粒子的检测,尽管当ERK1/2激活通过帕莫酸处理上调时,抑制的EV释放可以逆转。ERK1/2激活还通过增强量子点和金纳米颗粒以及氧化铁(临床上最普遍的无机纳米颗粒)的小胶质细胞EV释放,减少了纳米颗粒的积累,增加了清除率。
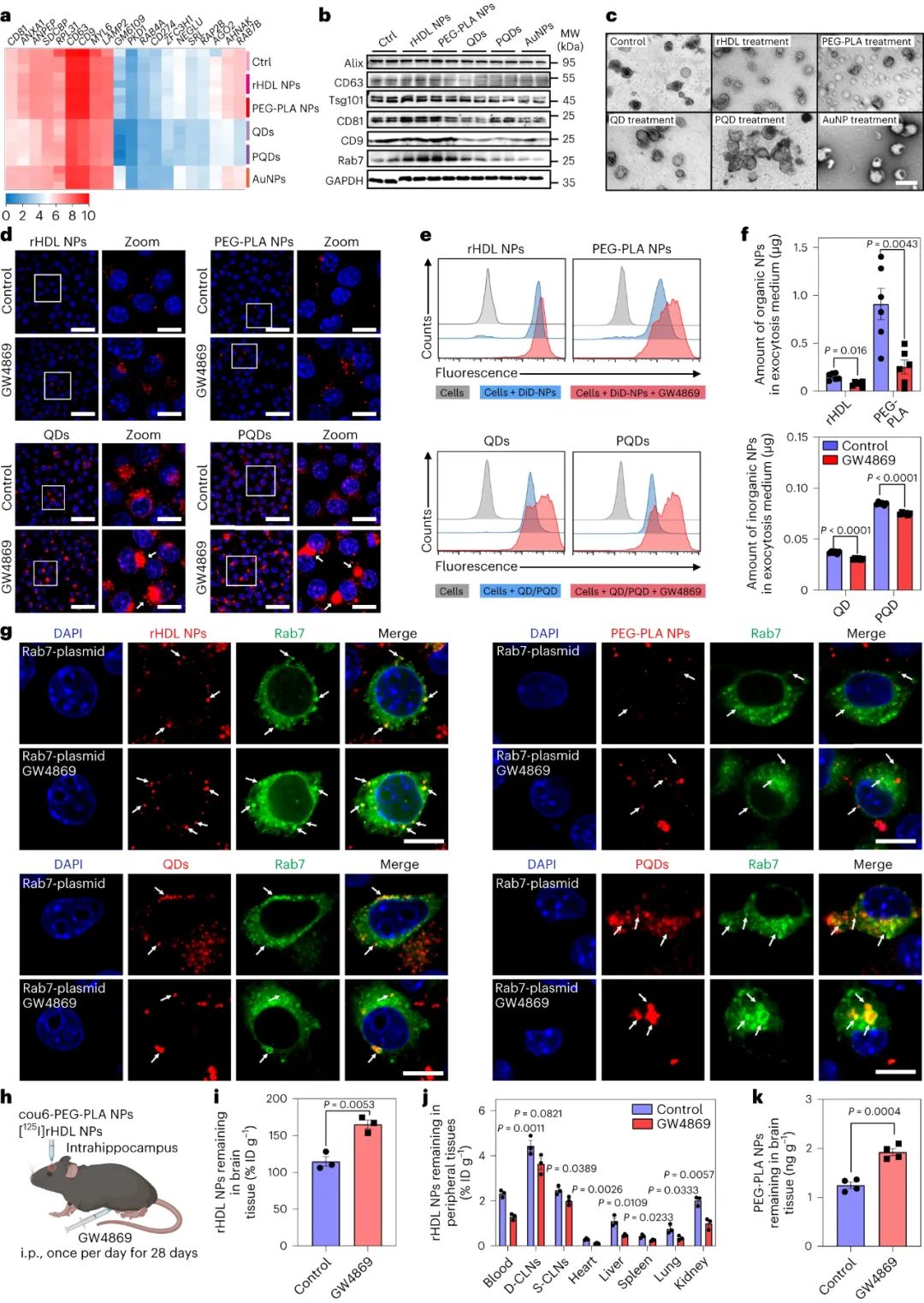
图|小胶质细胞 EV 的释放对于 NP 的消除至关重要
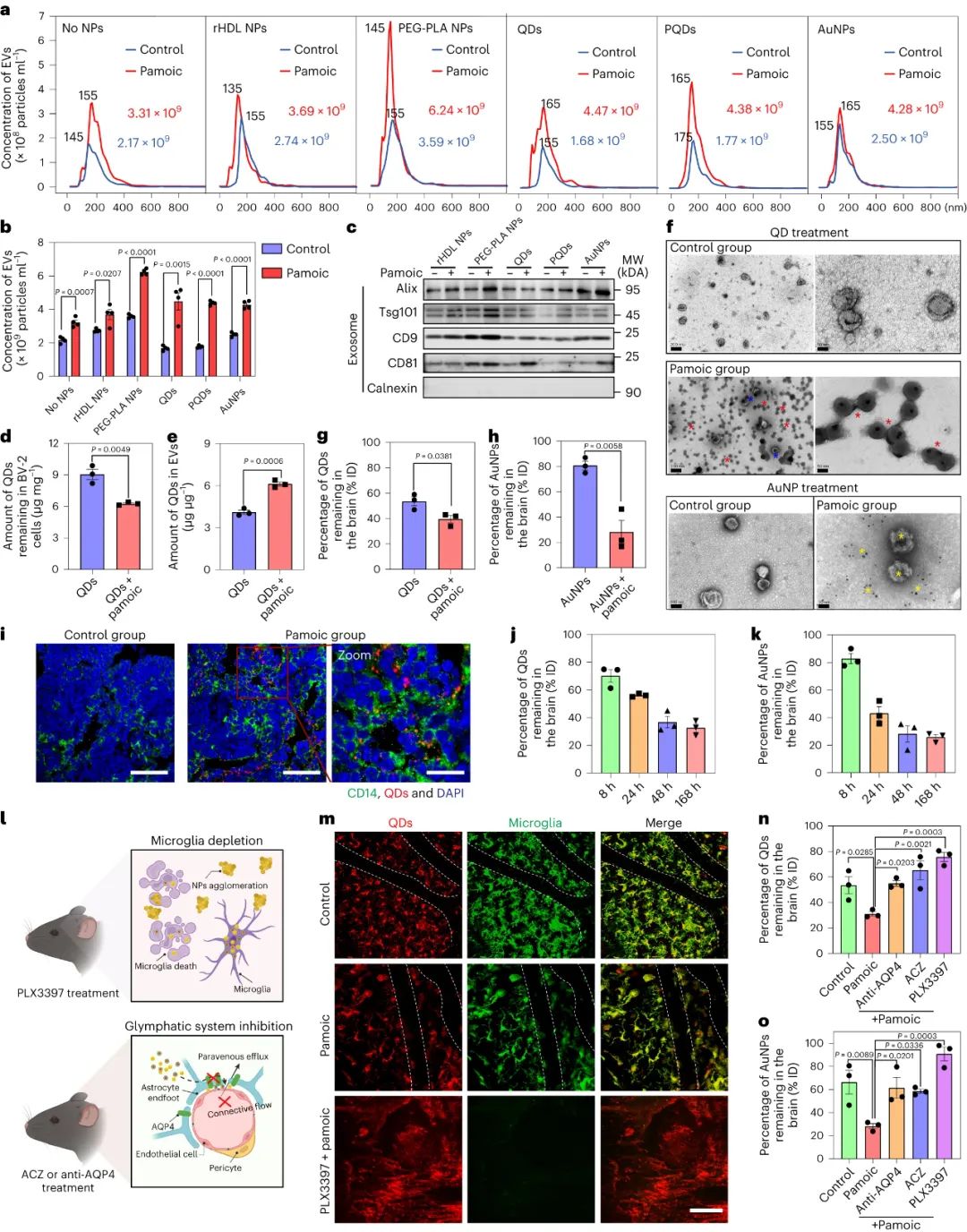
图|ERK1/2 激活促进 NP 从大脑中清除
总的来说,该广泛而严格的结果为纳米颗粒递送至大脑领域中纳米颗粒命运和清除的重要问题提供了机制见解。尽管该研究报告了使用的许多不同纳米颗粒系统的物理化学特性,分离每种性质对纳米颗粒在大脑中运输的单独贡献仍然是该领域需要解决的一个持续挑战,因为改变一种物理化学性质可能会从本质上改变另一种。
此外,许多中枢神经系统疾病的临床治疗策略不会像本研究中使用的那样使用脑内给药,这就需要继续进行研究,以了解不同的给药途径是否足以改变纳米颗粒的组成或表面表现,从而改变小胶质细胞EV分泌在纳米颗粒清除中的作用。尽管如此,研究人员使用的研究结果和技术的结合可以应用于任何纳米颗粒系统,其结果也为在疾病存在或治疗后比较纳米颗粒的保留和清除建立了基线。
参考文献:
Gao, J., Song, Q., Gu, X. et al. Intracerebral fate of organic and inorganic nanoparticles is dependent on microglial extracellular vesicle function. Nat. Nanotechnol. (2023).
https://doi.org/10.1038/s41565-023-01551-8











