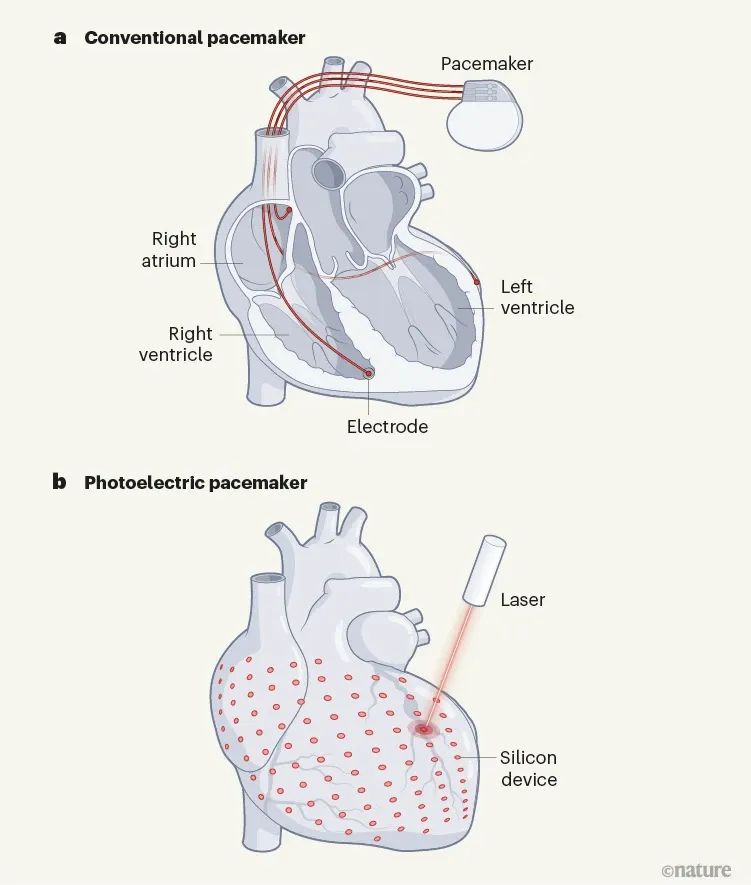
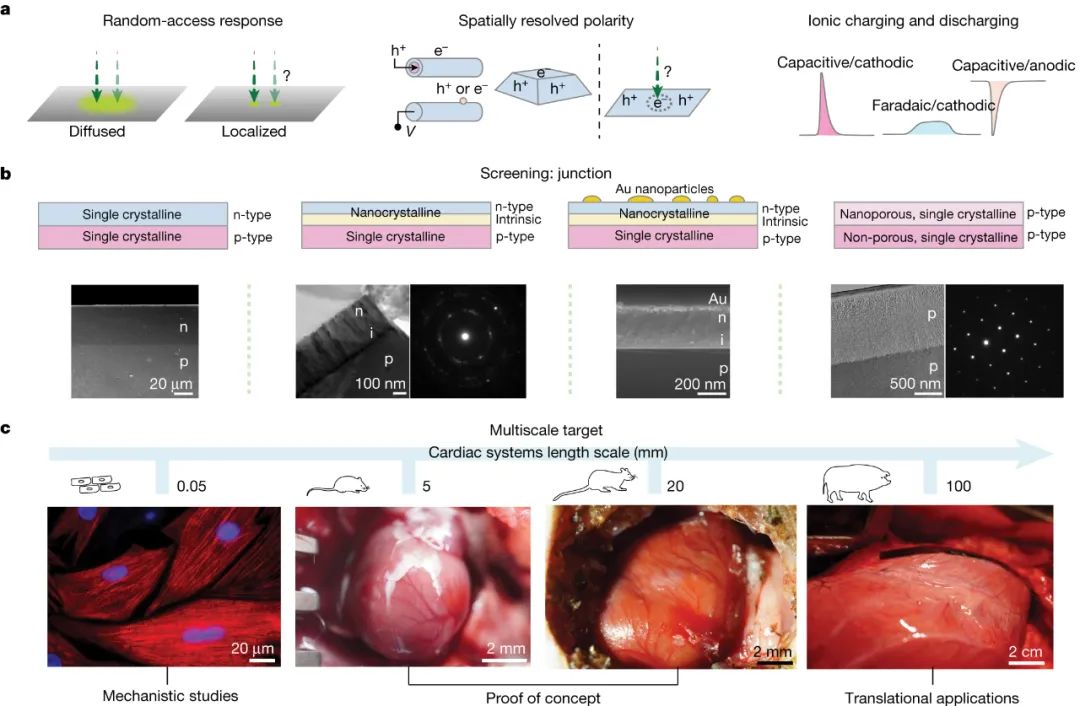
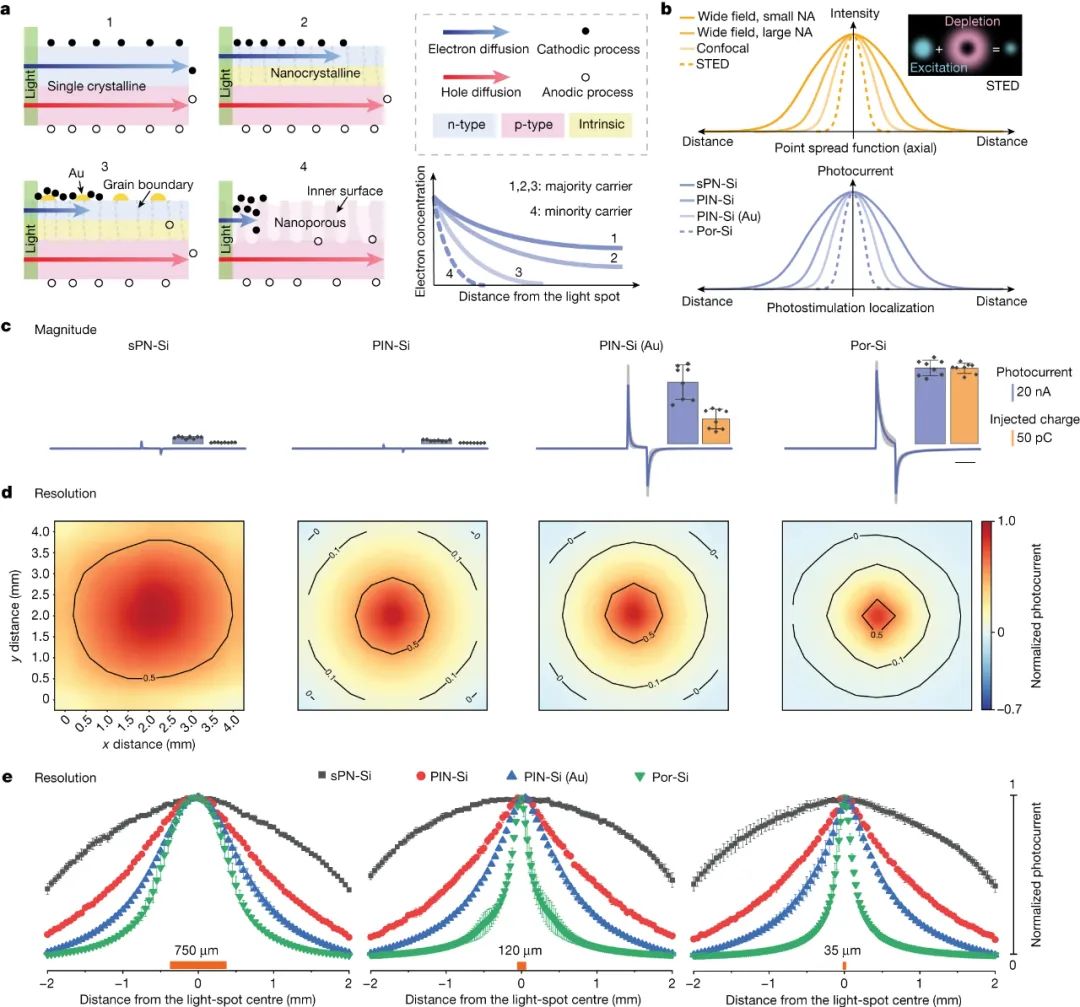
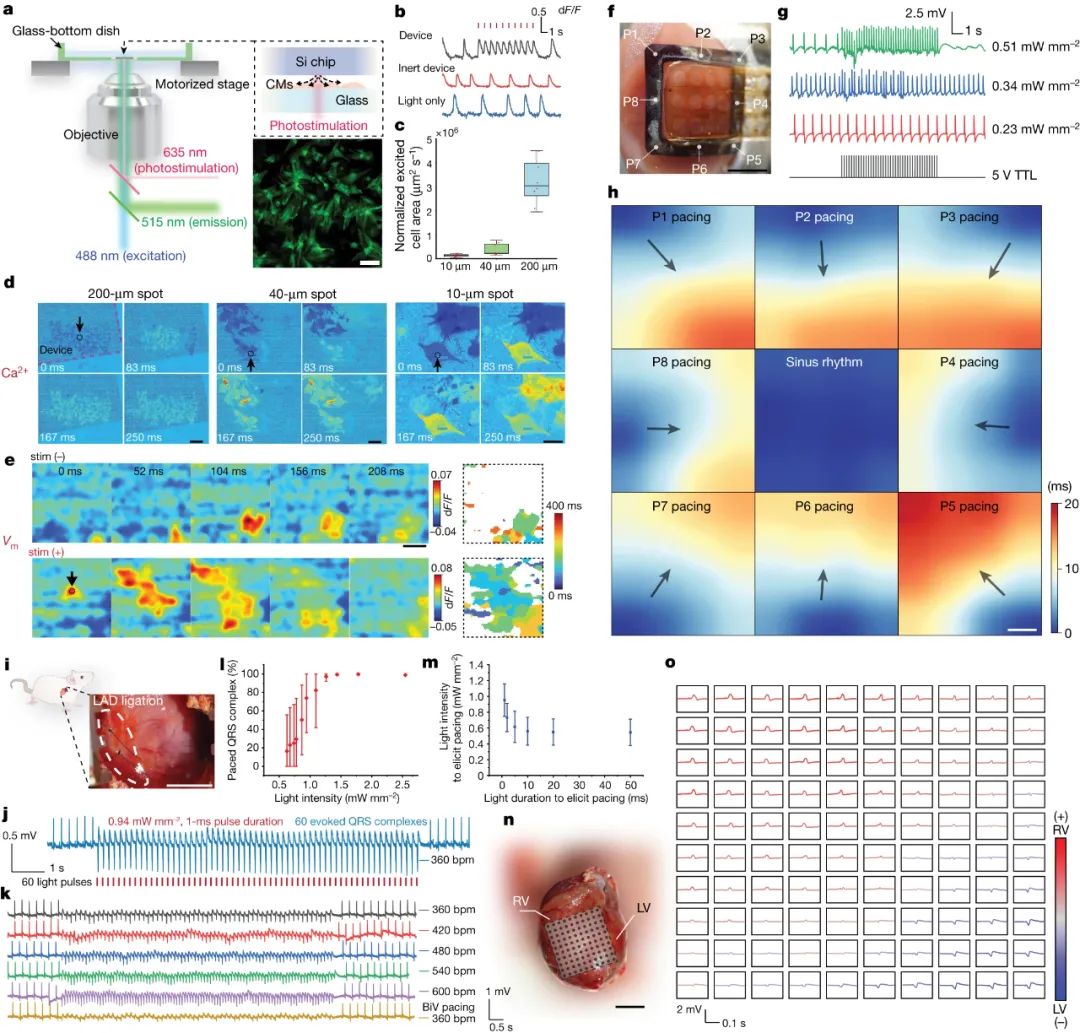
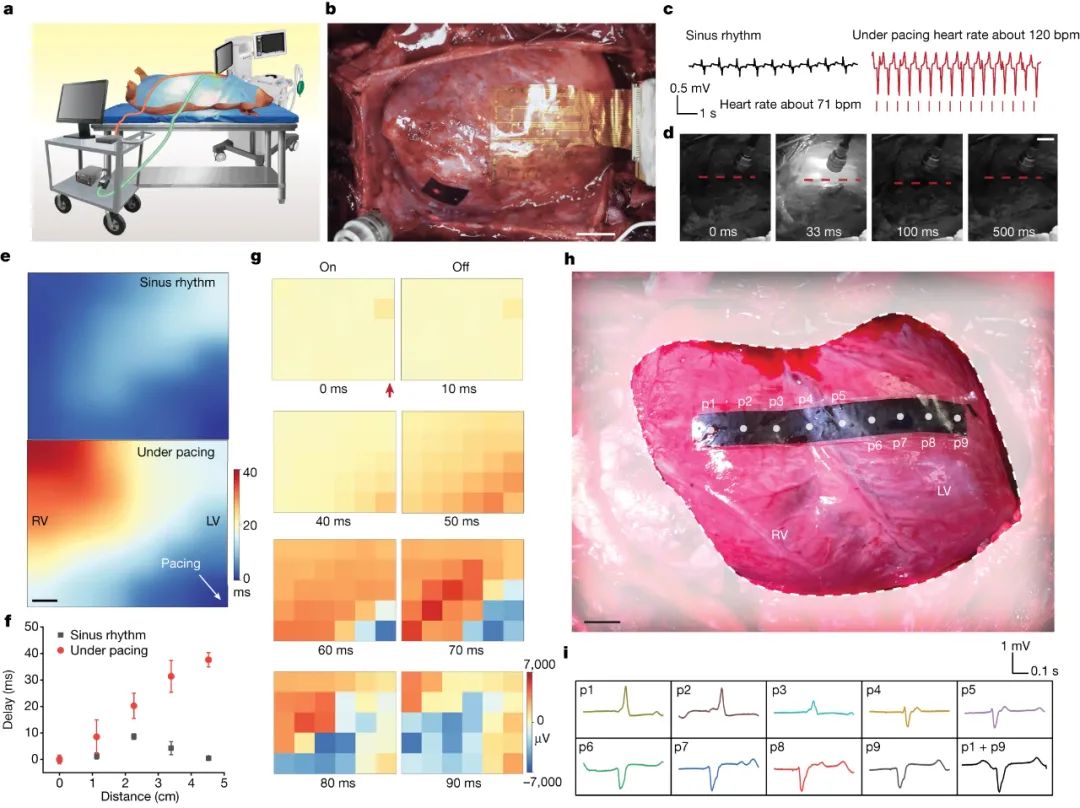
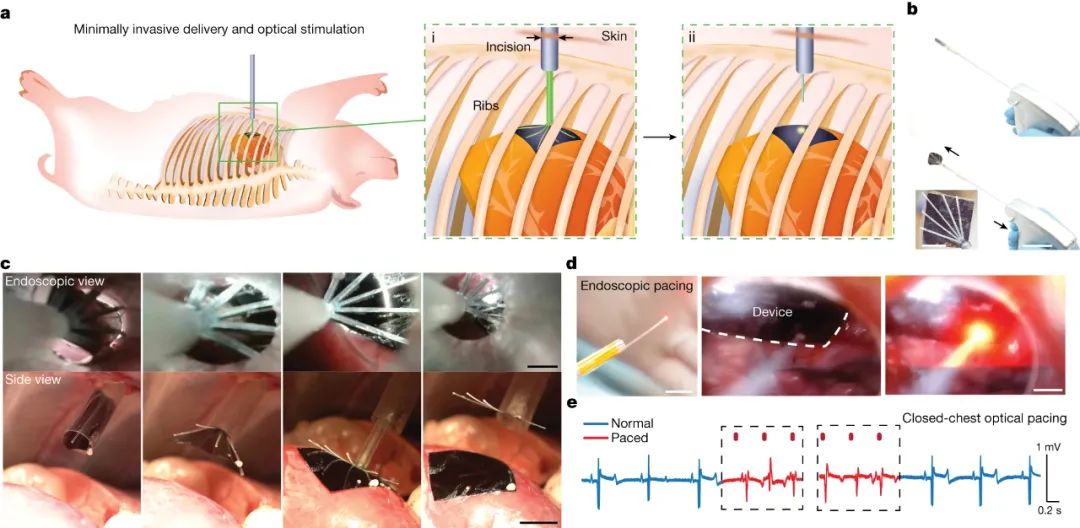
生命以心跳开始,也以心跳结束。这种规律的节律是由身体的自然起搏器设定的:一组称为窦房结的细胞。当该节点出现故障时,心脏病专家可以植入电动起搏器来刺激人的心脏恢复正常心率。但标准起搏器由寿命有限的电化学电池供电,并且这些设备容易出现电极故障和外部电磁场的干扰。植入式起搏器的主要挑战之一是它们可能导致心脏不同部位收缩不同步。与由身体传导系统刺激的健康心脏不同,由起搏器控制的心脏由通常植入右心房或心室的电极刺激。尽管电信号快速穿过整个器官,但这种局部刺激可能会导致异步兴奋,从而导致不同步的收缩。各种再同步装置添加了左心室电极,可预防和减轻此类情况下的心力衰竭。然而,这些设备要么只针对心脏中的几个部位,要么需要在传导系统的特定点精确植入一个电极。近日,芝加哥大学田博之、Narutoshi Hibino等人提出一种利用光能刺激心脏的技术,可以解决这些问题。无引线柔性生物电子器件以类似于人体自身调节机制的方式调节生物电信号,可以为神经退行性疾病和心脏病提供新的治疗途径。光介导的遗传系统提供高时空分辨率和可调性,具有细胞和组织刺激的随机访问能力。对于临床转化,最新的基于非遗传光电二极管的光电设备可将光转换为电流,以与光遗传学中使用的光功率水平相当的光功率水平有效地调节细胞和组织。微图案像素化光电极能够实现高分辨率的局部刺激,展示了视网膜假体的巨大潜力。尽管如此,促进多位点生物刺激的单片光电化学装置的转化潜力取决于光刺激响应曲线在精度、准确性和分辨率方面的清晰表征。在细胞水平上,单个神经元同时具有电流源和电流汇,从而形成一个全局电荷平衡网络,具有偶极子甚至 n 极形式的局部异质细胞外电位。在分子水平上,神经元兴奋可涉及快速钠内向电流、慢速钙内向电流以及快速或慢速钾电流。这些离子电流类似于光电化学系统中的稳定法拉第电流和快速电容性阴极和阳极电流。这两方面的成就为用于生物电调制的无引线光电化学系统铺平了道路。研究人员提出时空光电化学器件剖析作为一种新方法,用于评估半导体-盐水系统的时空能力。制造了四种不同配置的基于硅的光电二极管器件,分别为单晶p-n硅(sPN-Si)、p-i-n型硅(PIN-Si)、Au纳米颗粒修饰的p-i-n硅(PIN-Si(Au))和基于多孔结构的异质结(Por-Si)。研究结果发现Por-Si在相同光照条件下的绝对光电流大小最大,而且经过1000次循环后保持了85%以上的初始光电流值。在器件精度、准确性和分辨率方面的评估中,Por-Si表现出最佳的性能,其光电流定位和分辨率最优。Por-Si的时空图显示,其具有最优的光电流定位和光电化学电流半高全宽(FWHM)的变化,表明具有更高的光学可调分辨率。此外,实验结果表明,Por-Si的光生空穴比电子扩散更远,使得器件可以在没有独立返回电极的情况下工作。Por-Si在用于高时间精度的光刺激应用非常具有潜力,且具有内在的电荷平衡特性,可能增强其在生物电应用中的安全性。图|具有高时空分辨率光响应的单片光电化学器件的设计概念该研究通过使用单体Por-Si芯片对心肌细胞进行光刺激实验,成功实现了精准的细胞激活控制。光驱动能够引发心肌细胞的同步钙内流,并调控兴奋细胞区域大小。近场电刺激和远场电刺激产生了不同的膜去极化模式。光刺激引发的局部效应对细胞内Ca2+动态和药物反应具有重要影响。该研究为未来的细胞机制研究和体外长期刺激研究提供了一个有前景的工具。在体外大鼠心脏光刺激实验中,Por-Si芯片表现出了可靠的心脏起搏效果,其最低稳定起搏光强降至0.166 mW mm−2,实现了360 bpm的心率。此外,通过工程化的Por-Si设备,可实现高时空多点起搏,并成功控制心肌组织的激活起始点。在体内大鼠心脏光刺激实验中,Por-Si设备可在较低光强下(0.94 mW mm−2)可靠地实现心脏起搏,且能够达到高达600 bpm的心率,同时能够实现双心室同时起搏。此外,在非侵入性胸腔起搏实验中,Por-Si设备可通过胸壁实现360 bpm的心率起搏,而无需开胸手术。研究人员在活体猪模型中应用非基因光电子技术调节心脏活动,成功实现了对心脏的光刺激。通过将Por-Si器件放置在右心室心外膜壁上,实现了对心室起搏的精准控制,无需缝合或黏合剂。光刺激后,观察到明显的心室起搏波形,光脉冲频率为2 Hz时,心率达到120 bpm。通过调节光强度,可获得确定性的起搏效果,解决了同步不一致性的问题。在猪心起搏实验中,研究人员确定了适用于不同心脏区域的光刺激阈值,为20–30 mW mm−2的光强度和1 ms的脉冲持续时间。使用柔性的多通道MEA,研究人员能够直接记录心外膜表面的电信号,以实时监测心脏电活动的传播路径和时空分布。通过多点和双心室起搏,研究人员展示了对心脏激活的空间精准控制。这些结果为光刺激技术在临床心脏调控中的应用提供了重要的实验基础。最后,研究人员开发了一种微创的设备输送技术,用于光学心脏调控,通过猪心模型模拟临床手术程序。这种技术只需要在两根肋骨之间进行直径为0.5–1厘米的小切口,避免了传统手术中的骨切割和扩张,减少了术后创伤。通过微型外科手术程序,在心包膜上暴露一个小窗口,然后通过切口引入输送设备导管,使Si膜设备安全地铺设在心外膜表面。在引入光纤耦合内窥镜后,研究人员成功地在封闭的胸腔环境中实现了对猪心的微创光刺激。这些发现表明了该技术的潜在临床转化价值,为微创心脏干预提供了理论基础。Li, P., Zhang, J., Hayashi, H. et al. Monolithic silicon for high spatiotemporal translational photostimulation. Nature (2024).https://doi.org/10.1038/s41586-024-07016-9