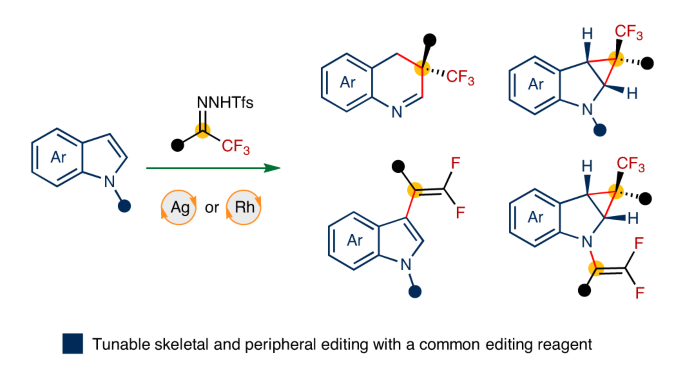
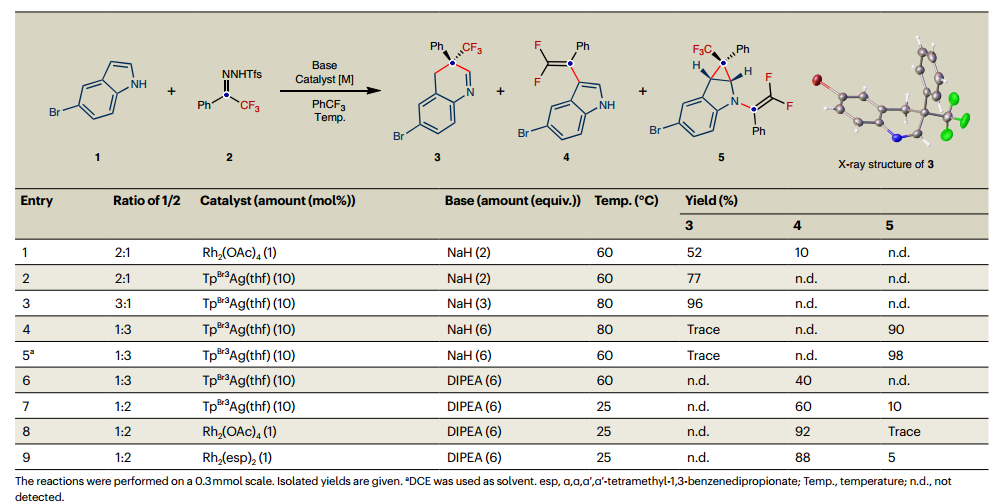
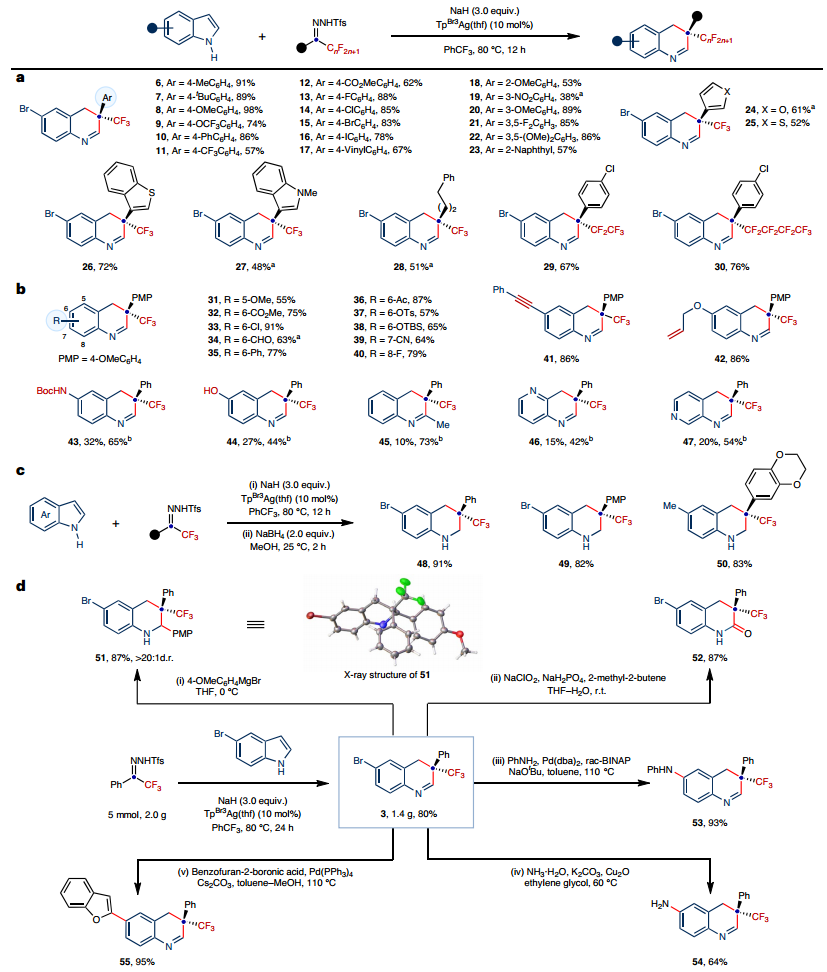
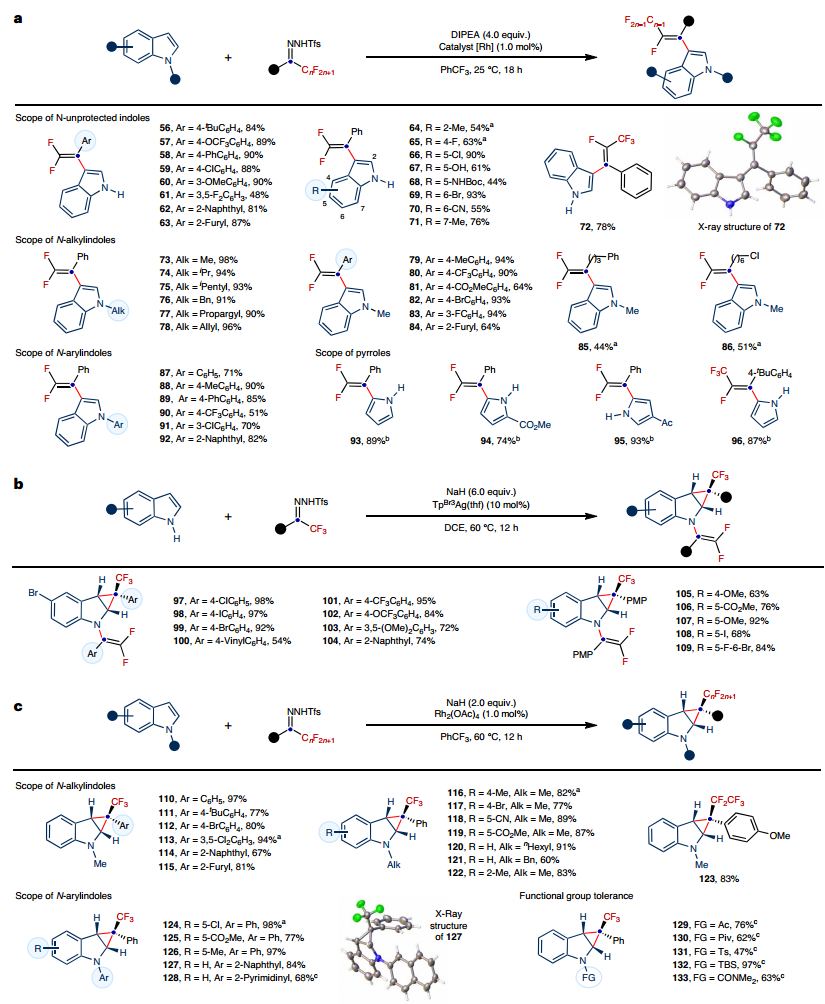
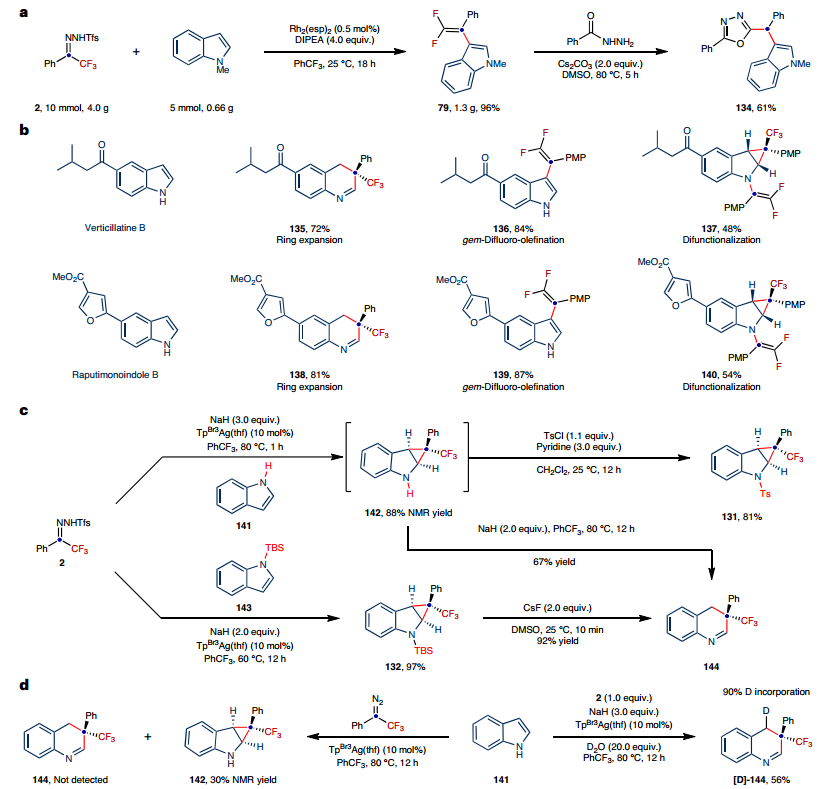
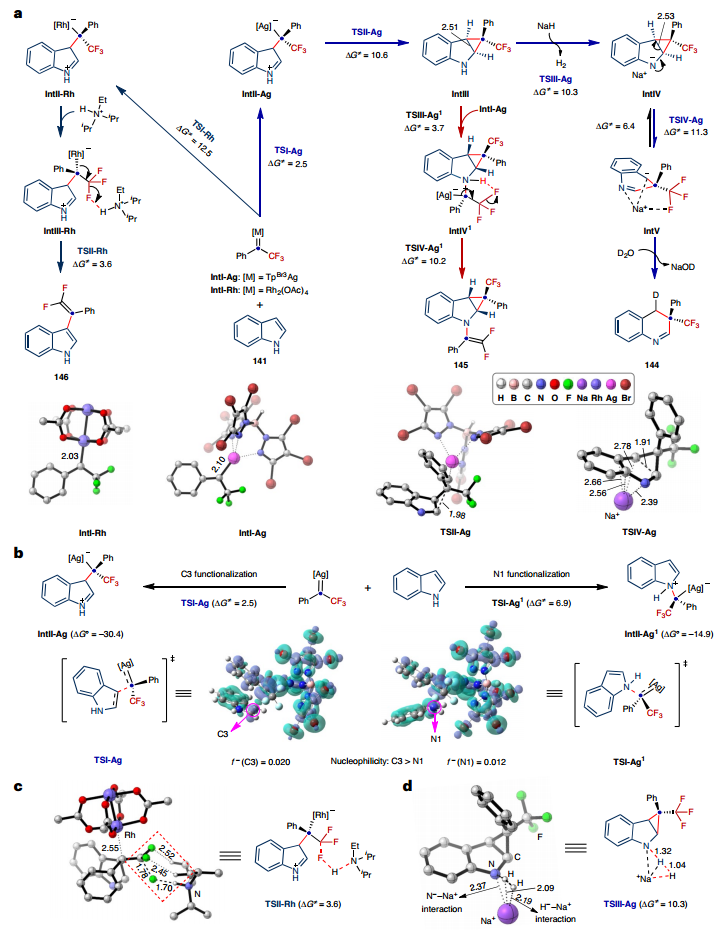
特别说明:本文由米测技术中心原创撰写,旨在分享相关科研知识。因学识有限,难免有所疏漏和错误,请读者批判性阅读,也恳请大方之家批评指正。从简单的原料通过精确的外围和骨架修饰构建分子复杂性是现代有机合成的核心。然而,尽管具有最大限度地增加结构多样性和应用的潜力,但通过共同底物修饰芳香杂环的核心骨架和外围的可控策略仍然难以实现。有鉴于此,东北师范大学毕锡和、刘兆洪等人报道了一种卡宾引发的吲哚化学趋异性分子编辑,通过捕获由氟烷基N-三氟甲苯基腙原位产生的亲电子氟烷基卡宾,可以进行骨架和外围编辑。通过在吲哚骨架或外围进行可调节的化学选择性编辑反应,可以有效地实现多种含氟N-杂环支架,包括单碳插入、C3偕二氟烯化、串联环丙烷化和N1偕二氟烯化和环丙烷化。这种化学趋异性分子编辑策略的力量已经通过以可控和化学选择性的方式对天然产物的骨架或外围进行修饰而凸显出来。通过实验和理论方法探讨了化学选择性和区域选择性的反应机制和起源。 为了实现用氟烷基卡宾对N-未保护的吲哚进行化学趋异性分子编辑,需要解决与C3-H键和亲核氮原子的反应性相关的位点和化学选择性控制问题。作者首先研究了重点是选择性骨架编辑反应的发展,证实了通过捕获由氟烷基N-三氟甲苯基腙原位产生的亲电子氟烷基卡宾能够实现N-未受保护的吲哚的C3偕二氟烯化。 作者接下来探索了碳插入反应的底物范围,表明具有给电子基团或吸电子基团基团的三氟甲基苯基N-三甲苯基腙提供了良好至优异的产率碳插入产品 此外,方案对于将全氟烷基纳入候选药物也是有效的,具有不饱和单元的吲哚在骨架环扩张反应中也表现良好。作者HIA开发了脱芳环丙烷化反应,并研究了底物范围。接着,通过C3偕二氟烯化反应进行的克级合成证明了工艺的可扩展性。 作者进行了一系列对照实验以深入了解碳插入过程的机制,通过1H NMR等多种反应过程表征,结果表明环丙烷中间体可能参与一碳插入过程,反应溶剂中的外来水参与了质子化过程。进一步地,在高精度SMD(DCM)-DLPNO-CCSD(T)/def2-TZVPP//SMD(DCM)-B3LYP/上进行了理论计算以探讨不同转化的机制并确定不寻常的化学选择性的起源。作者进一步了解反应途径催化调节的本质,表明Rh基和Ag基催化剂都能顺利生产产物144、145和146。C3偕二氟烯化和环丙烷化反应的反应路径主要受碱的选择控制。 图 天然产物的放大合成、化学发散分子编辑及机理研究Liu, S., Yang, Y., Song, Q. et al. Tunable molecular editing of indoles with fluoroalkyl carbenes. Nat. Chem. (2024). https://doi.org/10.1038/s41557-024-01468-2