胶质母细胞瘤(GBM)的代谢重编程会影响免疫抑制微环境,是实现有效的免疫治疗面临的一项严峻挑战。有鉴于此,中国科学院长春应化所张洪杰院士、Yang Liu和王樱蕙副研究员利用在中枢神经系统(CNS)中相对孤立的胆固醇代谢微环境开发了一种专门为实现GBM免疫治疗“量身定制”的氢键有机框架(HOF)。
本文要点:
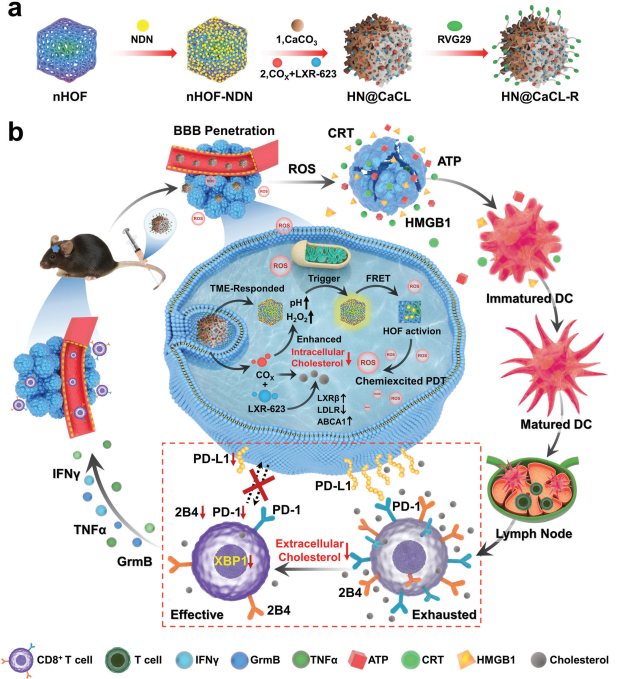
(1)基于HOF的生物调节剂能够调节细胞外/胞内的胆固醇代谢,有效阻断程序性死亡蛋白1/程序性死亡配体1(PD-1/PD-L1)通路,降低2B4表达,进而从代谢上破坏GBM的免疫抑制微环境,并使CD8+ T细胞恢复活力。研究发现,调节胆固醇代谢也有助于治疗GBM侵袭。
(2)在调节胆固醇代谢过程中,肿瘤微环境(TME)介导、化学激发的光动力疗法(PDT)也能够得到增强。实验结果表明,该生物调谐器可有效触发免疫原性细胞死亡(ICD),增加细胞毒性T淋巴细胞(CTLs)在GBM中的浸润。通过逆转免疫抑制微环境和化学激发PDT,该方法可实现对GBM的高效非抗体依赖性免疫治疗。综上所述,该研究能够为通过调节胆固醇代谢增强免疫治疗提供重要的理论基础,进一步探索了"代谢检查点"策略在GBM治疗中的可行性。
Na Yin. et al. A Cholesterol Metabolic Regulated Hydrogen-Bonded Organic Framework (HOF)-Based Biotuner for Antibody Non-Dependent Immunotherapy Tailored for Glioblastoma. Advanced Materials. 2023
DOI: 10.1002/adma.202303567
https://onlinelibrary.wiley.com/doi/10.1002/adma.202303567



















