构建集成了近红外二区(NIR-II)窗口荧光成像能力和肿瘤微环境响应性多模态治疗功能的纳米平台对于实时反馈治疗效果和优化肿瘤抑制效率而言具有重要意义。有鉴于此,中国科学院理化技术研究所汪鹏飞研究员、郑秀丽博士和香港城市大学Chun-Sing Lee开发了一种对pH敏感的吡咯吡咯aza-BODIPY基两亲性分子(PTG),该分子具有平衡的NIR-II荧光亮度和光热效应。
本文要点:
(1)实验进一步将PTG与血管破坏剂(DMXAA)共组装,制备得到了PTDG纳米粒,以用于联合抗血管/光热治疗和实时监测肿瘤血管破坏情况。研究发现,每个PTG分子都有一个活性的PT-3核心,其可通过对pH敏感的酯键与两条PEG链进行连接。在酸性肿瘤环境中,酯键的裂解会导致DMXAA被释放以用于抗血管治疗,并进一步将PT-3核组装成微米颗粒,以长期监测肿瘤进展。
(2)此外,得益于PTDG纳米粒在NIR-II区域的高亮度(119.61 M-1 cm-1)和较长的血液循环时间(t1/2 = 235.6 min),该纳米平台可在治疗过程中实现对肿瘤血管的破坏过程的实时、原位可视化成像。综上所述,该研究设计了一种能够用于构建pH响应性NIR-II纳米平台的自组装策略,该平台可实现对肿瘤血管破坏情况的实时监测,并且能够长期示踪肿瘤进展和进行抗血管/光热联合治疗。
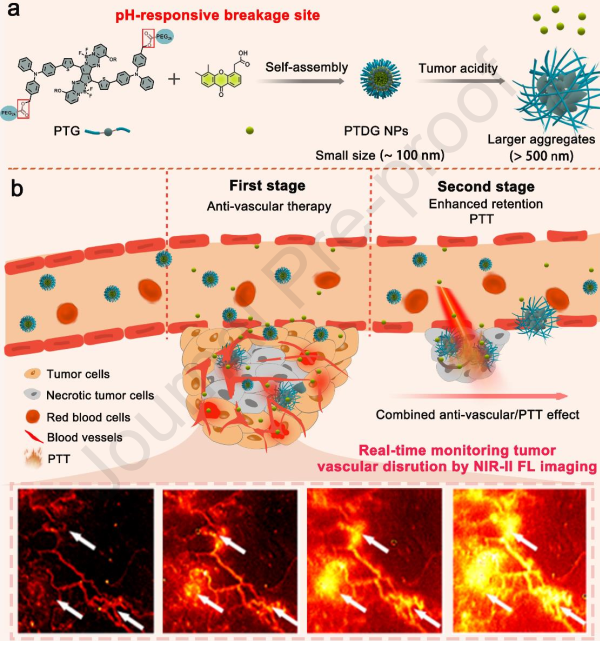
Shuaishuai Bian. et al. pH-responsive NIR-II phototheranostic agents for in situ tumor vascular monitoring and combined anti vascular/photothermal therapy. Biomaterials. 2023
https://www.sciencedirect.com/science/article/pii/S0142961223003885



















