肿瘤相关巨噬细胞(TAMs)在肿瘤微环境中含量丰富,其可通过多种机制促进免疫抑制性肿瘤微环境(ITME)的形成,从而严重影响免疫治疗的疗效。有鉴于此,同济大学周敏研究员、中国科学院上海硅酸盐研究所施剑林院士和Wencheng Wu开发了一种新型的仿生铁死亡诱导剂(D@FMN-M),该诱导剂能够通过调控ITME来增强肿瘤铁死亡-免疫治疗。
本文要点:
(1)当D@FMN-M在肿瘤内富集时,瘤内的温和酸性会触发富铁纳米载体的生物降解,以同时释放二氢青蒿素(DHA)和Fe3+。释放的Fe3+可通过消耗瘤内的谷胱甘肽(GSH)而被还原为Fe2+,进而触发类芬顿反应和Fe2+-DHA反应以促进大量自由基的生成,从而诱导癌细胞和M2型TAMs发生铁死亡。研究发现,铁死亡的癌细胞会释放大量的肿瘤相关抗原,从而激活产生显著的抗癌免疫反应。
(2)实验结果表明,对铁死亡敏感的M2型TAMs会被铁死亡应激损伤或逐渐驯化为对铁死亡耐受的M1型TAMs,从而有利于实现ITME的正常化,增强肿瘤铁死亡的免疫治疗效果。综上所述,该研究设计了一种能够双重诱导肿瘤细胞和M2型TAMs发生铁死亡的重要方法,从而为实现具有TAMs浸润和免疫抑制性的实体肿瘤的铁死亡免疫治疗提供了一个新的有效策略。
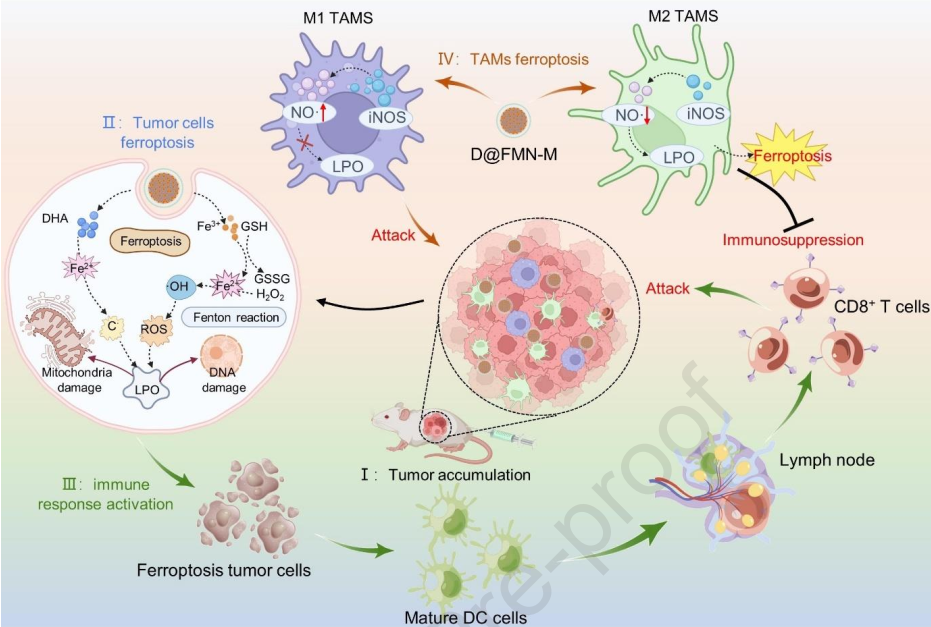
Mingqi Chen. et al. Biomimetic inducer enabled dual ferroptosis of tumor and M2-type macrophages for enhanced tumor immunotherapy. Biomaterials. 2023
https://www.sciencedirect.com/science/article/pii/S0142961223003940



















