免疫"冷"微环境会导致三阴性乳腺癌(TNBC)的免疫治疗效果不够理想。研究发现,具核梭杆菌(F. nucleatum)会定植于三阴性乳腺癌中,并且与免疫抑制性肿瘤微环境和肿瘤转移相关。有鉴于此,中国科学院长春应化所曲晓刚研究员、任劲松研究员和蒲芳研究员构建了一种细菌源性外膜囊泡(OMV)包被的纳米平台,其可以精确地靶向肿瘤组织,以对F. nucleatum和癌细胞进行双重杀伤,从而将瘤内细菌转化为免疫增效剂以提高对三阴性乳腺癌的免疫治疗效果。
本文要点:
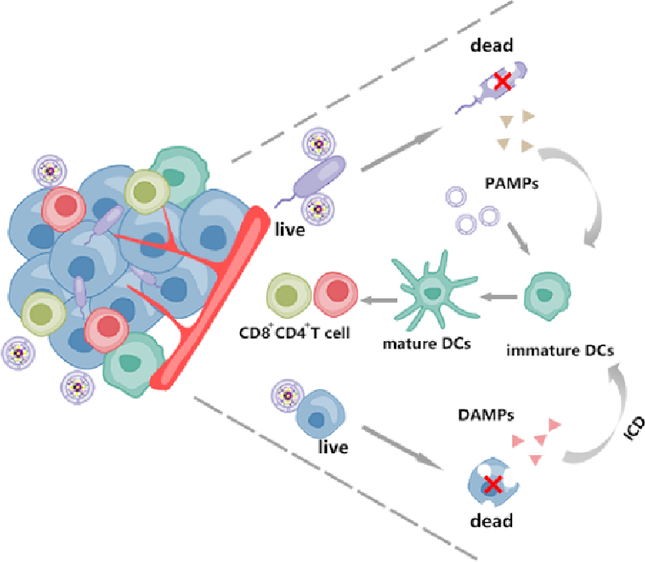
(1)制实验备的纳米粒子可通过类芬顿反应有效地诱导免疫原性细胞死亡,从而增强免疫原性。与此同时,肿瘤内的F. nucleatum会被甲硝唑杀死,导致病原体相关分子模式(PAMPs)的释放。研究发现,PAMPs与OMVs的协同作用能够进一步促进树突状细胞的成熟和T细胞的浸润。
(2)实验结果表明,这种“一石二鸟”的策略能够逆转肿瘤的免疫“冷”微环境,实现抗肿瘤免疫反应的最大化,从而达到有效治疗TNBC和预防肿瘤转移的目的。综上所述,这种基于肿瘤与正常组织的微生态差异以及微生物群诱导的冷肿瘤逆转的策略能够为实现精准、高效的TNBC免疫治疗提供新的思路。
Xuemeng Liu. et al. Transforming Intratumor Bacteria into Immunopotentiators to Reverse Cold Tumors for Enhanced Immuno-chemodynamic Therapy of Triple-Negative Breast Cancer. Journal of the American Chemical Society. 2023
DOI: 10.1021/jacs.3c09472
https://pubs.acs.org/doi/10.1021/jacs.3c09472



















