化疗药物在肿瘤内的积累效率不佳和复杂的免疫抑制微环境等问题会降低免疫应答率和治疗效果。利用靶向配体对对药物进行表面修饰可以促进其被细胞内吞,但修饰后的药物往往也会受到免疫识别和清除。有鉴于此,四川大学罗奎教授开发了一种结合免疫原性细胞死亡(ICD)诱导剂(表柔比星,Epi)和吲哚胺2,3-双加氧酶1(IDO1)抑制剂(NLG919)、苯基硼酸(PBA)基团保护的树状纳米药物,并将其用于肿瘤化学-免疫治疗。
本文要点:
(1)负载NLG919、与Epi共轭的聚乙二醇化树状聚合物与硼酸键(NLG919@Epi-DBP)桥接后能够在循环过程中保持稳定的纳米结构。在偏酸性的条件下,PBA基团会被暴露并与肿瘤细胞膜上的唾液酸残基发生相互作用,以增强NLG919@Epi-DBP的细胞内化和穿透。在pH为5.0时,NLG919@Epi-DBP会迅速解体,以释放Epi和NLG919。研究发现,Epi可高效地诱导肿瘤细胞发生ICD,以引起强烈的免疫反应。
(2)此外,抑制IDO1的活性能够下调L-色氨酸向犬尿氨酸的代谢,进而导致免疫抑制细胞募集减少,从而实现对肿瘤免疫微环境的调节。实验结果表明,该研究设计的策略能够诱导产生强大的免疫反应,并重塑免疫抑制微环境,以显著增强化学-免疫治疗效果。
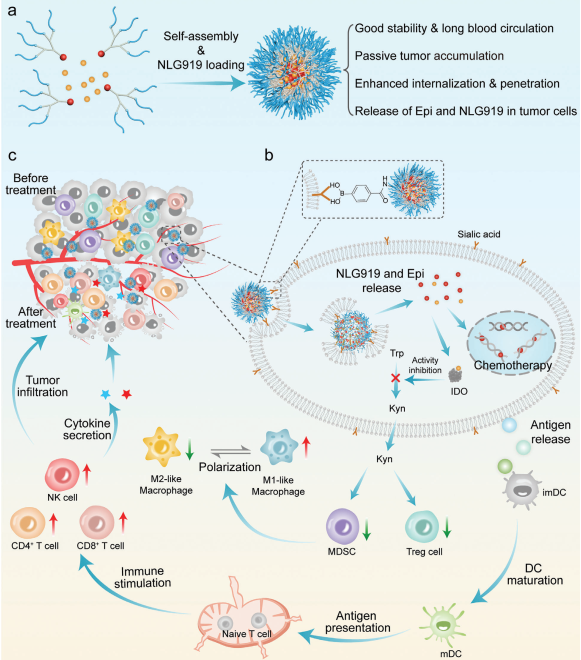
Yunkun Li. et al. Dendritic Nanomedicine with Boronate Bonds for Augmented Chemo-Immunotherapy via Synergistic Modulation of Tumor Immune Microenvironment. Advanced Materials. 2023
DOI: 10.1002/adma.202307263
https://onlinelibrary.wiley.com/doi/10.1002/adma.202307263



















