肿瘤微环境(TME)的异质性是导致肿瘤治疗无效和肿瘤进展失控的主要原因。基于焦亡的免疫原性细胞死亡(ICD)治疗是克服TME异质性以提高抗肿瘤效果的理想策略。然而,目前主要依赖于单一内源性或外源性刺激的焦亡治疗方法的有效性仍会受到恶性细胞固有病理特征的限制。因此,开发一种具有高肿瘤特异性和可调性的协同策略是非常必要的。有鉴于此,安徽医科大学何晓燕教授和赣南医科大学Xiaoqing Yi通过将中性粒细胞伪装壳和负载活性氧(ROS)供应体的自协同聚合物相结合,构建了一种具有协同功能的纳米平台。
本文要点:
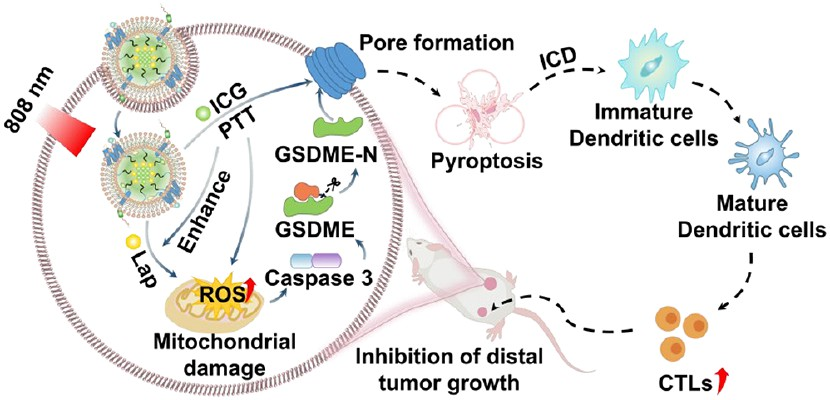
(1)包覆的中性粒细胞膜使得该纳米平台具有“隐身”特性,并有利于其在肿瘤中实现有效的聚集。在激光照射下,光敏剂(吲哚菁绿)能够触发ROS的生成,并可将激光照射转化为热量,以上调NAD(P)H:醌氧化还原酶1。该酶可进一步催化β-拉帕酮以自产生充足的内源性ROS,实现增强的ICD。
(2)实验结果表明,持续扩增产生的ROS不仅能够消除原发肿瘤,同时也可以增强gasdermin E介导的细胞焦亡,启动ICD级联反应,“重新教育”异质性TME,促进全身免疫响应,以抑制远端肿瘤的生长。综上所述,该研究开发的自协同纳米平台能够为调控免疫系统以实现对肿瘤的靶向抑制提供一种高效、持久的新方法。
Weiji Qin. et al. Advancing Precision: A Controllable SelfSynergistic Nanoplatform Initiating Pyroptosis-Based Immunogenic Cell Death Cascade for Targeted Tumor Therapy. ACS Nano. 2024
DOI: 10.1021/acsnano.3c09499
https://pubs.acs.org/doi/10.1021/acsnano.3c09499



















