锰离子(Mn2+)配位的纳米粒子是一类极具发展前景的抗肿瘤纳米治疗药物,能够同时破坏具有免疫抑制作用的肿瘤微环境(TME)和触发依赖于干扰素基因刺激因子(STING)通路的抗肿瘤免疫。然而,在TME中,利用Mn2+基单药疗法激活的STING信号通路往往无法高效地刺激抗原提呈细胞和逆转免疫抑制。有鉴于此,汕头大学姜红岩教授开发了一种Mn2+/CpG寡脱氧核苷酸(ODNs)共修饰的黑磷纳米片(BPNS@Mn2+/CpG)平台。
本文要点:
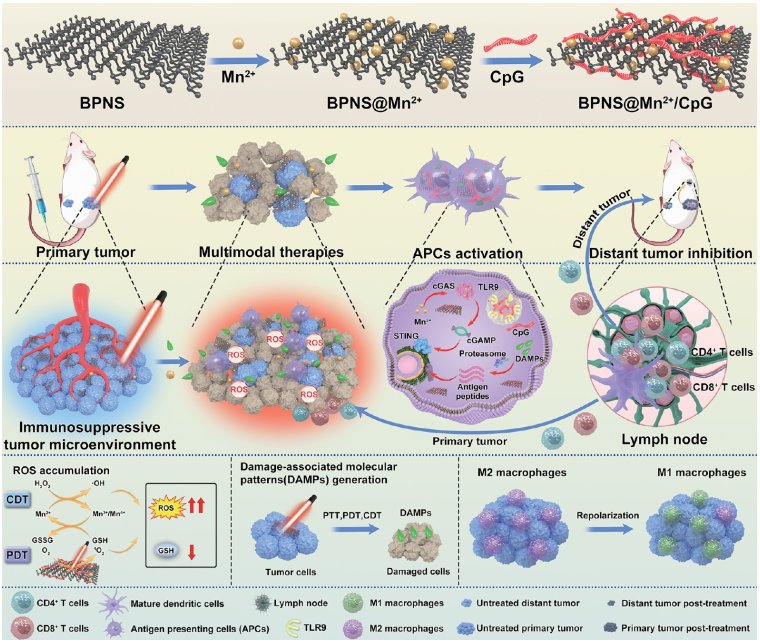
(1)Mn2+的配位可显著提高BPNS的稳定性和对CpG ODNs的吸附。酸性的TME和核内体区室会破坏Mn2+的配位,从而触发对pH响应的CpG ODNs和Mn2+的释放,以有效激活Toll样受体9和STING通路,导致TME中的M2型巨噬细胞和未成熟的树突状细胞受到强烈刺激,从而增加T淋巴细胞的浸润和逆转免疫抑制性TME。研究发现,BPNS@Mn2+/CpG平台能够实现光学治疗和化学动力学治疗,其在808 nm激光的照射下能够诱导免疫原性细胞死亡。
(2)经激光照射后,BPNS@Mn2+/CpG能够对原发肿瘤产生显著的治疗效果,并有效地抑制未经照射的远端肿瘤的生长。此外,BPNS@Mn2+/CpG也可以诱导产生强大的免疫记忆,以持久地对抗肿瘤复发。综上所述,该研究构建的BPNS@Mn2+/CpG能够实现增强的多模态抗肿瘤治疗,并进一步证明了金属离子修饰的BPNS材料在DNA/药物递送和肿瘤免疫治疗等方面具有非常广阔的应用前景。
Kai Ling. et al. Mn2+/CpG Oligodeoxynucleotides Codecorated Black Phosphorus Nanosheet Platform for Enhanced Antitumor Potency in Multimodal Therapy. ACS Nano. 2024
DOI: 10.1021/acsnano.3c07123
https://pubs.acs.org/doi/10.1021/acsnano.3c07123



















