乳腺癌的免疫抑制性环境会严重影响免疫治疗的有效性。溶瘤病毒有望通过靶向肿瘤细胞和改变微环境来解决这一问题。然而,中和抗体和免疫清除等问题仍会阻碍溶瘤病毒的临床应用。有鉴于此,不列颠哥伦比亚大学Honglin Luo构建了microRNA修饰的柯萨奇病毒B3(miR-CVB3),并对该新型溶瘤病毒在乳腺癌治疗中的应用潜力进行了探究。
本文要点:
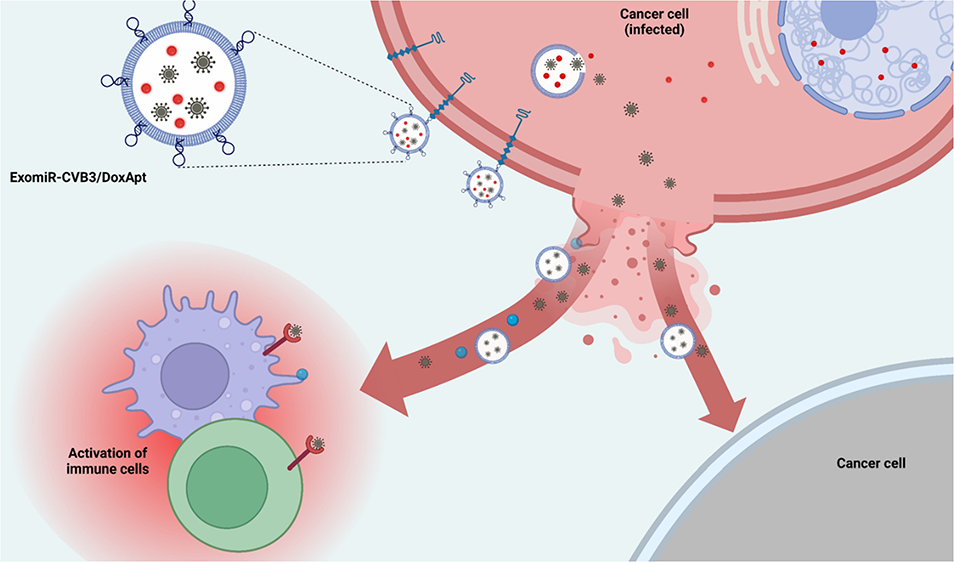
(1)实验研究了miR-CVB3对免疫相关蛋白的影响,并将外泌体作为保护屏障和递送载体。结果表明,miR-CVB3能够重塑免疫相关蛋白谱,使其向更强的免疫刺激状态发展,并增强外泌体介导的免疫细胞活化。此外,肿瘤细胞释放的包裹miR-CVB3的外泌体(ExomiR-CVB3)能够保持其抗肿瘤细胞毒性,并增强其其免疫刺激作用。
(2)ExomiR-CVB3可在全身给药时保护miR-CVB3免受中和抗体和快速的免疫清除等作用。基于此,研究者进一步利用AS1411适配体和阿霉素对ExomiR-CVB3进行工程化(ExomiR-CVB3/DoxApt),以提高其疗效。这种结合了基因组修饰、适配体表面修饰和阿霉素的方法可以将CVB3安全地递送至癌细胞。体内外实验结果表明,该策略能够实现选择性的乳腺癌细胞靶向、细胞死亡诱导和肿瘤微环境中显著的免疫细胞浸润,并同时保护健康器官。综上所述,该研究构建的ExomiR-CVB3/DoxApt是一种适用于多种类型癌症的开创性乳腺癌治疗策略,有望为重塑癌症免疫治疗提供一种有效通用的新方法。
Amirhossein Bahreyni. et al. Synergistic Viro-chemoimmunotherapy in Breast Cancer Enabled by Bioengineered Immunostimulatory Exosomes and Dual-Targeted Coxsackievirus B3. ACS Nano. 2024
DOI: 10.1021/acsnano.3c09491
https://pubs.acs.org/doi/10.1021/acsnano.3c09491



















