
现有的抗体/药物缀合物(ADC)接头,无论是可切割接头还是不可切割接头,都被设计成一旦ADC被内化到细胞中就释放高毒性有效载荷或有效载荷衍生物。然而,临床研究表明,只有<1%的给药ADC在肿瘤细胞中积累。其余>99%的ADC在健康组织细胞中非特异性分布,因此不可避免地导致ADC的脱靶毒性。
军事医学科学院Xinbo Zhou等描述了一种智能肿瘤特异性连接策略来解决这些限制。
本文要点:
(1)
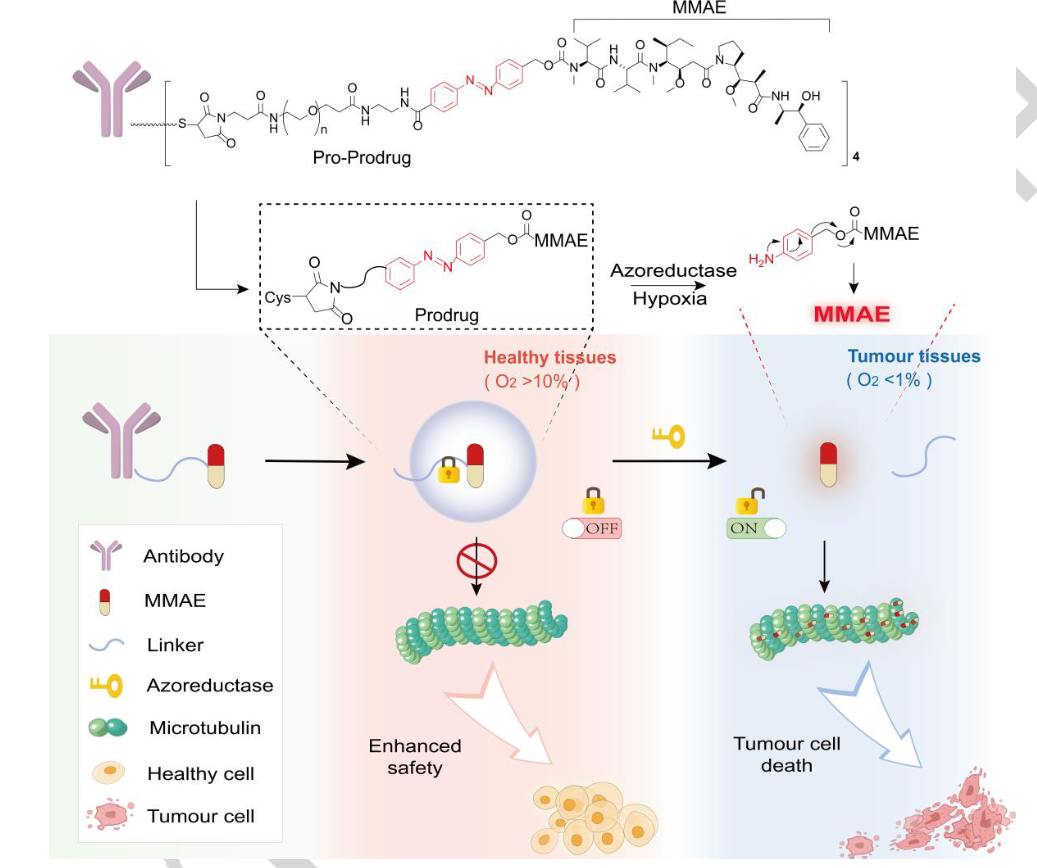
通过引入低氧激活的偶氮苯基团作为毒性控制剂来构建肿瘤特异性接头。作者证明这种基于偶氮苯的接头在健康组织中是不可裂解的(O2>10%),相应的有效载荷衍生物MMAE,可以作为安全的前药来掩盖MMAE的毒性(关闭)。在暴露于低氧肿瘤微环境(O2<1%)时,该接头被切割以释放MMAE并完全恢复ADC的高细胞毒性(开启)。值得注意的是,与传统的含有ADC的可切割接头或不可切割接头相比,含有ADC的偶氮苯接头在体内表现出令人满意的抗肿瘤效果和更好的治疗窗。
(2)
因此,作者基于偶氮苯的连接体为下一代ADC连接体的开发带来了新的希望。
参考文献:
Dian Xiao, Lianqi Liu, Fei Xie, Jingwen Dong, Yanming Wang, Xin Xu, Wu Zhong, Hongbin Deng, Xinbo Zhou, Song Li, Azobenzene-based Linker Strategy for Selective Activation of Antibody-Drug Conjugates,Angew. Chem. Int. Ed. 2024, e202310318.
DOI: 10.1002/anie.202310318
https://doi.org/10.1002/anie.202310318


















