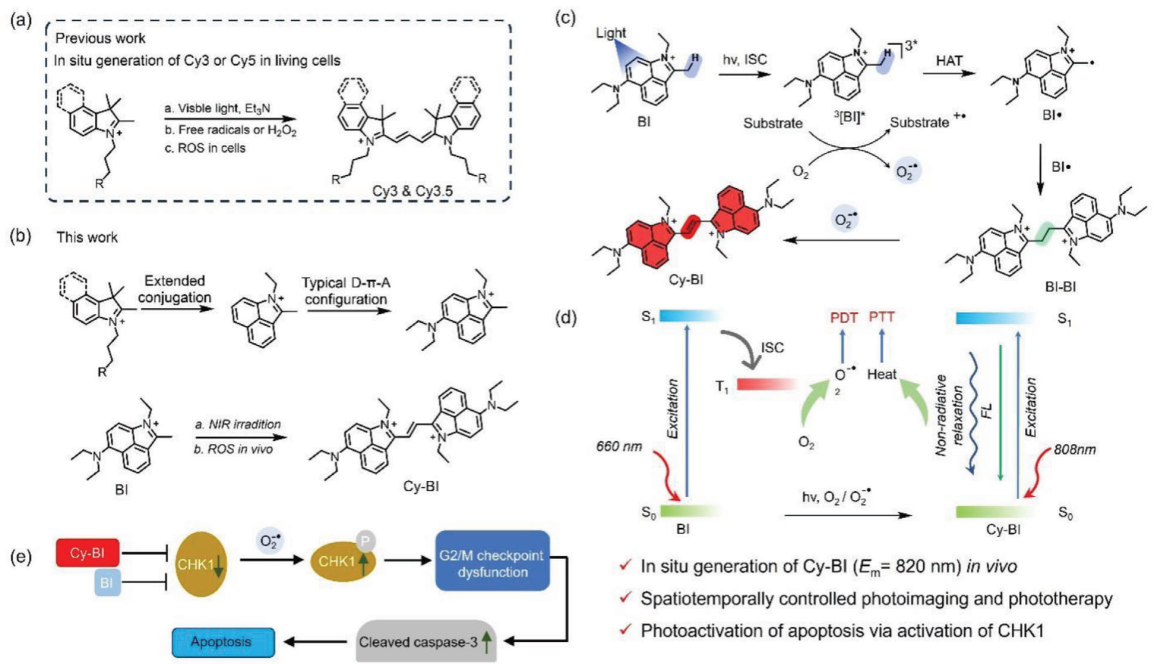
光激活分子具有高精度的时空控制性能,极大地促进了荧光染料的生物成像和光学治疗应用。有鉴于此,山西大学阴彩霞教授和云洋教授构建了首个可被宽激发光(405-660 nm)触发的光激活传感器(BI),该传感器可通过系间交叉和H原子转移等过程形成超氧阴离子自由基(O2−•)和碳自由基。
本文要点:
(1)光诱导的碳中心自由基(BI•)能够通过自由基-自由基偶联产生组合的交联产物(BI─BI)。在O2−•存在的情况下,该交联产物会被氧化,从而产生具有近红外发射(820 nm)的扩展共轭体系。研究发现,光化学生成的产物(Cy─BI)具有高达90.9%的超高光热转换效率,可显著优化光学治疗的效果。
(2)Western Blot结果显示,BI和光产物Cy─BI均能有效抑制CHK1的表达,并进一步诱导细胞凋亡,最终增强光学治疗的效果。实验结果表明,将细胞周期阻滞诱导的凋亡、光动力治疗和光热治疗进行联合应用可实现对体内实体瘤的有效抑制,进而产生显著的抗肿瘤疗效。综上所述,该研究能够为开发光激活分子提供新的借鉴,并有望进一步推动光激活分子在光学成像和光学治疗等肿瘤相关领域中的应用。
Weijie Zhang. et al. Photoactivation Inducing Multifunctional Coupling of
Fluorophore for Efficient Tumor Therapy In Situ. Advanced Materials. 2024
DOI: 10.1002/adma.202314021
https://onlinelibrary.wiley.com/doi/10.1002/adma.202314021



















