基因组编辑策略有望能够改善抗肿瘤免疫治疗的效果。然而,细胞质膜会阻止几乎所有的游离基因组调控制剂的进入。因此,研究者亟需开发一种时空可控、并且能够立即打开细胞膜的系统,从而使得基因组编辑制剂可以进入靶细胞。受T细胞可通过穿孔将细胞毒素递送至癌细胞的能力启发,温州医科大学王钦阳研究员开发了一种超声(US)控制的穿孔系统(UPS),以增强对游离的基因组调控药物的递送。
本文要点:
(1)UPS可以穿透肿瘤细胞膜,并同时能够通过可控的脂质过氧化反应维持细胞的活力。在体外,无跨膜功能的质粒可以在UPS的辅助下进入细胞并进行基因组编辑,效率高达90%。在体内,具有可生物降解性、非免疫原性和肿瘤靶向性的UPS能够在超声作用下实现肿瘤细胞穿孔。
(2)实验结果表明,UPS辅助的基因组编辑技术可成功恢复4T1荷瘤小鼠体内的gasdermin-E的表达,从而能够在低剂量X射线的照射下实现焦亡介导的抗肿瘤免疫治疗。综上所述,该研究能够为设计用于基因组编辑的声孔系统提供新的见解,并进一步证明了利用基因组编辑技术恢复gasdermin的表达可显著提高放射免疫治疗的疗效。
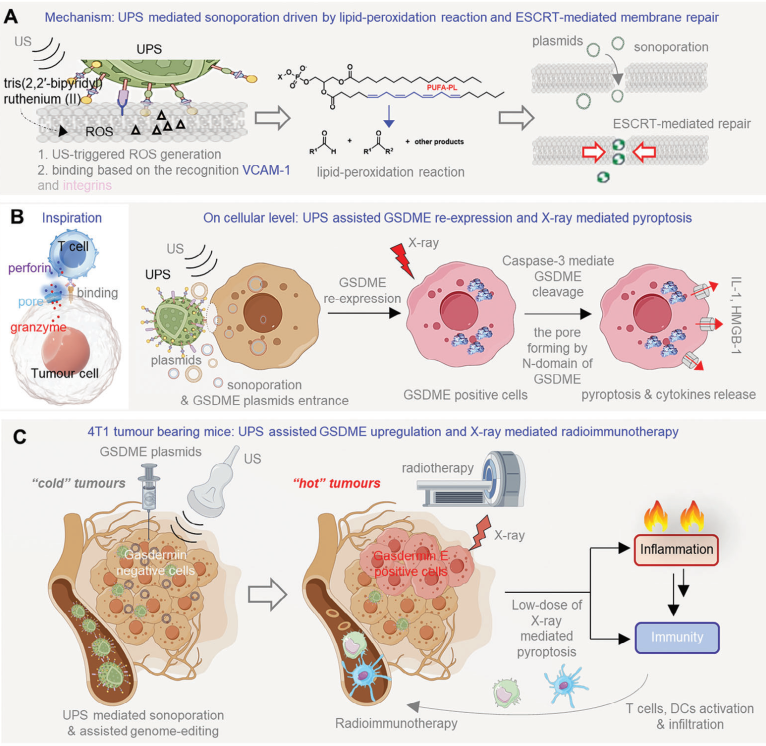
Hao Yin. et al. A T-Cell Inspired Sonoporation System Enhances Low-Dose X-Ray-Mediated Pyroptosis and Radioimmunotherapy Efficacy by Restoring Gasdermin-E Expression. Advanced Materials. 2024
DOI: 10.1002/adma.202401384
https://onlinelibrary.wiley.com/doi/10.1002/adma.202401384



















