胶质母细胞瘤(GBM)是一种侵袭性脑癌,其对包括嵌合抗原受体(CAR)-T细胞在内的多种治疗方法具有高度的耐药性。肿瘤相关小胶质细胞和巨噬细胞(TAMs)是导致免疫抑制性GBM微环境的主要因素,可促进肿瘤进展和治疗耐药。因此,对TAMs进行调节有望能够提高CAR-T细胞抗GBM免疫治疗的效果。分子靶向药物培西达替尼(PLX)已被证明可将TAMs再教育为具有抗肿瘤作用的M1表型。有鉴于此,中国药科大学张灿教授和郝玫茜博士开发了一种细胞-药物集成技术,将含PLX的脂质体(PLX-Lip)可逆地偶联到CAR-T细胞上,构建了肿瘤响应性集成型CAR-T细胞(PLX-Lip/AZO-T细胞),以实现对GBM的联合治疗。
本文要点:
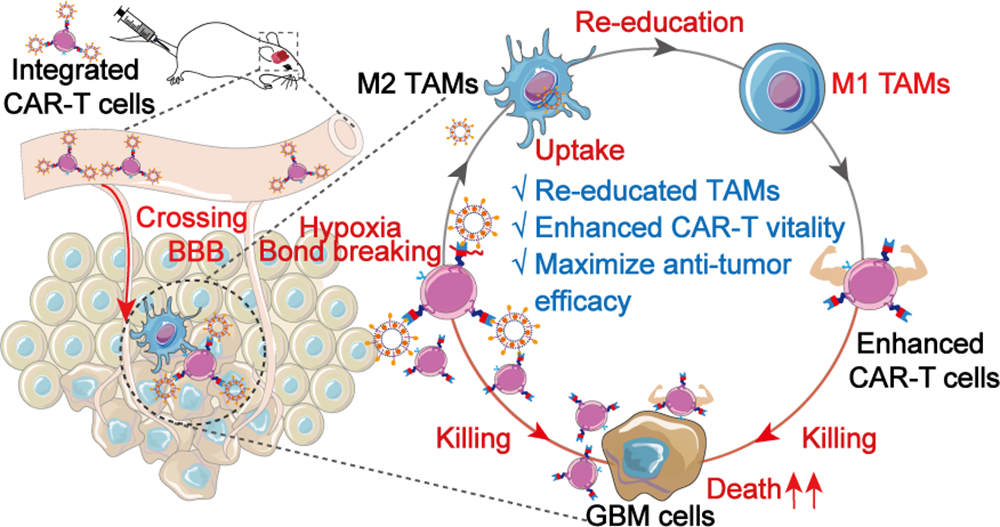
(1)在GBM小鼠模型中,PLX-Lip能够在循环的PLX-Lip/AZO-T细胞表面保持稳定,并且这些细胞可以穿过血脑屏障以在肿瘤部位实现PLX-Lip的富集。研究发现,摄取PLX-Lip的TAMs会被有效地再教育为M1表型,从而增强CAR-T细胞的抗肿瘤功能。
(2)接受PLX-Lip/AZO-T细胞治疗后,60%小鼠的GBM肿瘤会完全消失,总体生存时间可超过50 d。相比之下,其它治疗组小鼠的中位生存时间不超过35 d。综上所述,该研究证明了细胞-药物集成技术可成功实现CAR-T细胞和小分子药物的融合。集成型CAR-T细胞不仅能够为GBM的治疗提供一种性能更优的联合策略,也有望为构建集成型细胞药物提供重要的借鉴和参考。
Nianci Zhu. et al. Enhancing Glioblastoma Immunotherapy with Integrated Chimeric Antigen Receptor T Cells through the Re-Education of Tumor-Associated Microglia and Macrophages. ACS Nano. 2024
DOI: 10.1021/acsnano.4c00050
https://pubs.acs.org/doi/10.1021/acsnano.4c00050



















