铁死亡是一种由过度脂质过氧化物(LPO)驱动的铁依赖性调节性细胞死亡过程,在胰腺癌(PC)治疗领域中表现出了广阔的应用前景。然而,具有乏氧和谷胱甘肽(GSH)表达升高等特征的肿瘤微环境(TME)不仅会抑制LPO的产生,还会诱导谷胱甘肽过氧化物酶4(GPX4)介导的LPO清除,从而极大地影响铁死亡的治疗效果。有鉴于此,同济大学石硕教授和梁淑静教授设计了一种能够三重增强铁死亡的新型铁死亡“放大器”(Zal@HMPTBC)。
本文要点:
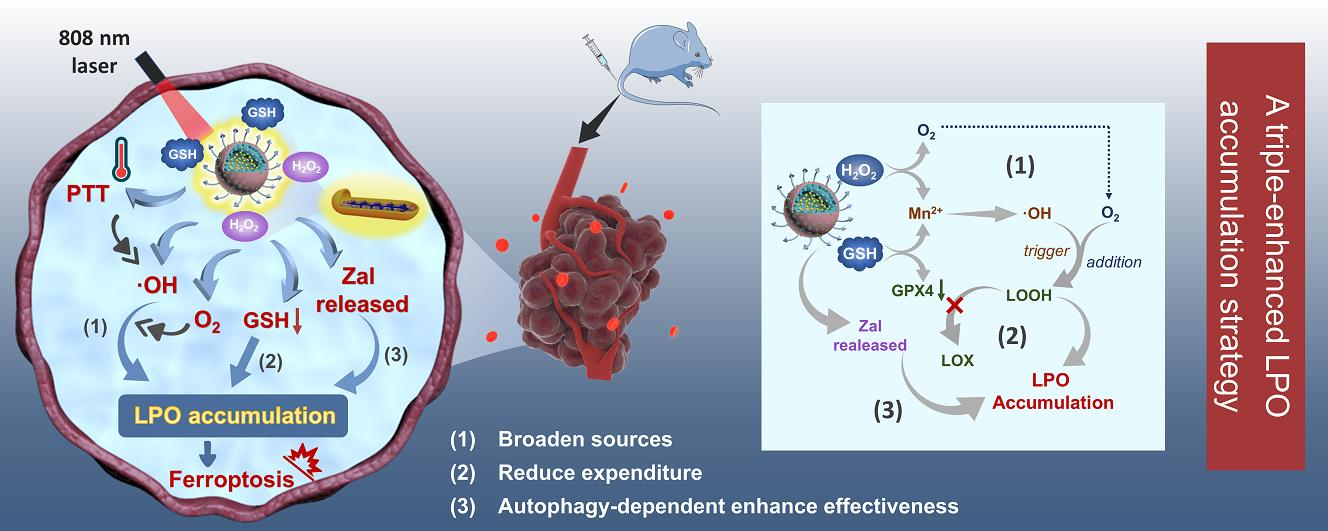
(1)静脉注射后,TME中过表达的H2O2/GSH可诱导Zal@HM-PTBC“崩塌”,以触发产生氧和活性氧(ROS),从而协同增强脂质过氧化程度(开源)。与此同时,中空二氧化锰(HM)的降解会进一步消耗GSH,以显著削弱GPX4的活性,导致LPO清除率下降(节流)。
(2)研究发现,定点释放的扎西他滨可进一步促进对自噬依赖的LPO积累(增强有效性)。体内外实验结果表明,该铁死亡“放大器”具有较好的特异性和良好的治疗效果。综上所述,该研究设计的三重增强LPO积累的策略能够有效地促进铁死亡,有望为PC的治疗提供一条新的途径。
Mengyao Chen. et al. A ferroptosis amplifier based on triple-enhanced lipid peroxides accumulation strategy for effective pancreatic cancer therapy. Biomaterials. 2024
https://www.sciencedirect.com/science/article/pii/S014296122400108X



















