重症急性胰腺炎(AP)是一种危及生命的胰腺炎症性疾病,病死率极高(约40%)。由于存在治疗靶点单一、水溶性差、半衰期短以及胰腺靶向特异性有限等问题,因此处于研发阶段或临床试验阶段的现有药物疗法的疗效仍不够理想。有鉴于此,中国海洋大学何治宇教授和于良民教授开发了一种具有酸响应性、中性粒细胞膜包裹的中空介孔普鲁士蓝纳米颗粒,其表面修饰了N,N-二甲基-1,3-丙二胺,可用于共递送膜通透性钙螯合剂BAPTA-AM(BA)和胰蛋白酶活性抑制剂甲磺酸加贝酯(Ga)。
本文要点:
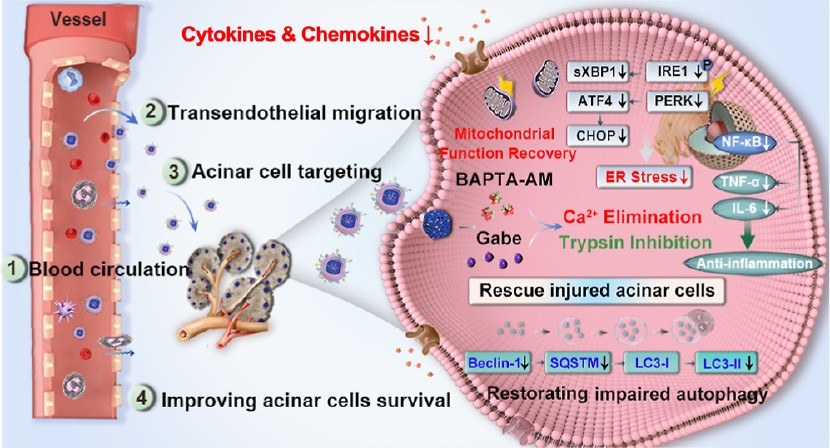
(1)在AP小鼠模型中,该纳米制剂能够表现出有效的炎症内皮募集、跨内皮迁移和精准的腺泡细胞靶向等功能,从而可以实现快速的胰腺定位和更高的富集效果。研究发现,单次低剂量制剂(BA: 200 μg kg−1,Ga: 0.75 mg kg−1)治疗可显著降低胰腺功能指标(接近正常水平),并有效恢复细胞的氧化还原状态,降低凋亡细胞比例,阻断全身炎症放大级联反应,使生存率从58.3%显著提升至100%。
(2)机制研究表明,该药物可抑制内质网应激(IRE1/XBP1和ATF4/CHOP轴),恢复受损的自噬(Beclin-1/p62/LC3轴),从而保护垂死的腺泡细胞,并恢复细胞的“健康状态”。综上所述,该研究构建的纳米药物能够协同调节离子稳态和抑制胰腺自身消化,有望为AP治疗提供一种具有临床转化前景的上游治疗策略。
Yanan Wang. et al. Inflammation and Acinar Cell Dual-Targeting Nanomedicines for Synergistic Treatment of Acute Pancreatitis via Ca2+ Homeostasis Regulation and Pancreas Autodigestion Inhibition. ACS Nano. 2024
DOI: 10.1021/acsnano.4c00218
https://pubs.acs.org/doi/10.1021/acsnano.4c00218



















