肿瘤相关肥大细胞(TAMCs)能够在肿瘤微环境中发挥多方面的作用。因此,对TAMCs进行无创光学成像非常有助于了解它们在肿瘤免疫治疗中的功能。然而,由于缺乏具有肥大细胞特异性的单一酶,因此基于单酶激活的探针设计方法并不适用于构建TAMCs探针。有鉴于此,南洋理工大学浦侃裔教授设计了一种基于光诱导电子转移-分子内电荷转移杂化策略、双酶锁定的分子探针(THCMC),并将其用于TAMCs的体内成像。
本文要点:
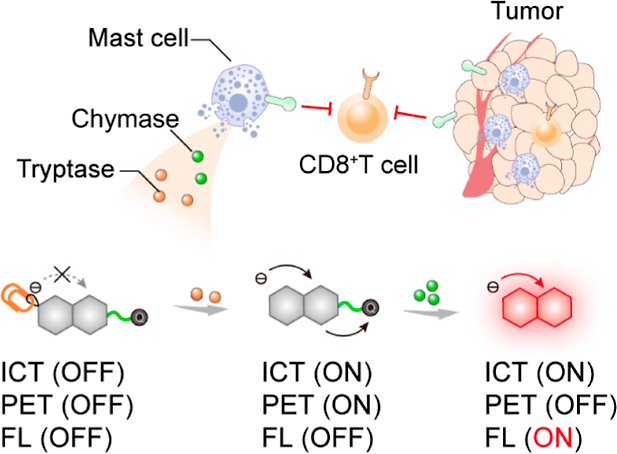
(1)双酶锁定的激活机制确保THCMC只会在肥大细胞特异性共表达的类胰蛋白酶和糜蛋白酶存在的情况下开启近红外(NIR)荧光。因此,THCMC可有效地将肥大细胞与其他白细胞(包括T细胞、中性粒细胞和巨噬细胞)区分开来,而单锁探针则无法实现这一目的。研究发现,具有高特异性的THCMC能够在肿瘤免疫治疗过程中无创地示踪活体小鼠肿瘤中的TAMCs波动情况。
(2)实验结果表明,在联合免疫治疗后,THCMC的瘤内信号下降与TAMCs数量减少之间具有良好的相关性,因此可以准确地预测对肿瘤生长的抑制作用。综上所述,该研究不仅构建了首个靶向TAMCs的近红外荧光探针,而且也提出了一种通用的双酶锁定探针的设计方法,可用于实现体内细胞成像。
Yuxuan Hu. et al. Bienzyme-Locked Activatable Fluorescent Probes for Specific Imaging of Tumor-Associated Mast Cells. Journal of the American Chemical Society. 2024
DOI: 10.1021/jacs.4c02070
https://pubs.acs.org/doi/10.1021/jacs.4c02070



















