靶向端粒维持是一种用于治疗肝细胞癌(HCC)的新兴策略。然而,由于端粒-端粒酶轴在端粒维持中具有双重作用,因此研究者亟需开发一种全面的靶向调控策略。有鉴于此,浙江大学余日胜教授和Hongzhen Bai设计了一种基于聚氨基酸(D-PAAs)的策略,并将其用于时空共递送端粒酶抑制剂BIBR1523和AKT抑制剂补骨脂乙素。
本文要点:
(1)实验通过利用D-PAAs的可修饰性合成了聚合物-抑制剂偶联物(PB和PI)以及叶酸修饰的肿瘤靶向载体(PF)。这些构建模块能够利用D-PAAs的非共价组装实现胶束化,以形成共递送纳米药物(P-BI@P-FA)。研究发现,P-BI@P-FA可改善小分子抑制剂的药代动力学、肿瘤选择性和生物利用度,并且能够通过结合端粒酶失活与端粒破坏以启动双重端粒特异性抑制。
(2)此外,研究者也利用D-PAAs和二氧化锰设计了一种靶向肿瘤、能够用于磁共振成像的磁性纳米杂化系统。综上所述,该研究开发的基于D-PAAs的策略能够实现端粒特异性HCC治疗和诊断,有望为纳米药物的设计提供一个新的方法。
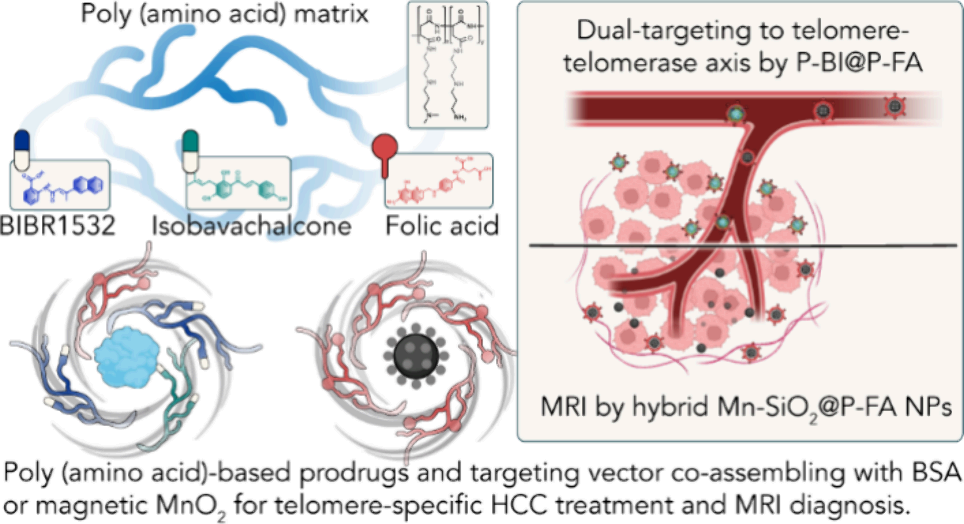
Jinguo Zhang. et al. A Poly(amino acid)-Based Nanomedicine Strategy: Telomere-Telomerase Axis Targeting and Magnetic Resonance Imaging in Hepatocellular Carcinoma Treatment. Nano Letters. 2024
DOI: 10.1021/acs.nanolett.4c01767
https://pubs.acs.org/doi/10.1021/acs.nanolett.4c01767



















