与常规疗法相比,光-免疫疗法能够实现精准的肿瘤靶向治疗,对健康组织的损伤较小,并且不会产生严重的不良反应,但其疗效仍会受到光穿透深度较浅和潜在的肿瘤耐药性等问题的限制。有鉴于此,天津大学姬晓元教授开发了一种具有受体-供体-受体(A-D-A)结构的纳米聚集体,其能够实现单次近红外光触发的双重光学治疗(包括光动力治疗(PDT)和光热治疗(PTT))。
本文要点:
(1)得益于强烈的分子内电荷转移(ICT),该A-D-A结构纳米聚集体具有延伸到近红外区域的广泛吸收和被显著抑制的荧光,可实现深度穿透和高效的光热转换(n= 67.94%)。合适的HOMO-LUMO分布有利于实现充分的系间窜跃(ISC),进而能够将基态氧(3O2)转化为单线态氧(1O2)和超氧阴离子(·O2−),并催化羟基自由基(·OH)的产生。研究发现,增强的ICT和ISC效应使得该A-D-A结构纳米聚集体能够通过高效的PTT和PDT治疗宫颈癌,并诱导产生免疫原性细胞死亡。
(2)结合临床使用的铝佐剂凝胶,研究者开发了一种新型的宫颈癌光-免疫治疗策略,并在原位和腹腔转移的宫颈癌动物模型中证明了该策略能够显著抑制原发肿瘤和转移肿瘤。综上所述,该研究开发的无创治疗策略能够为早期和晚期宫颈癌的临床治疗提供新的思路。
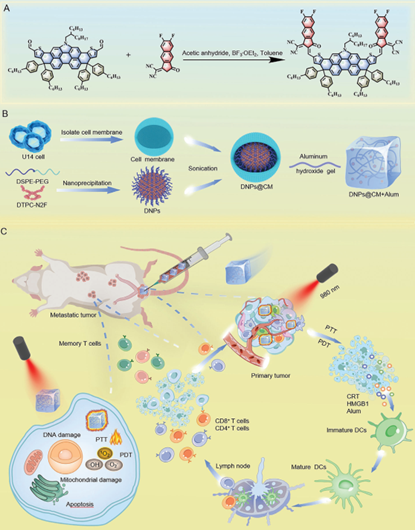
Gaoli Niu. et al. An Acceptor–Donor–Acceptor Structured Nano-Aggregate for NIR-Triggered Interventional Photoimmunotherapy of Cervical Cancer. Advanced Materials. 2024
DOI: 10.1002/adma.202407199
https://onlinelibrary.wiley.com/doi/10.1002/adma.202407199



















