
同时含有强氧化剂(S2O82-)和强还原剂(C2O42-)的溶液由于 S2O82–+C2O42– → 2 SO42–+2CO2 (ΔG0 = −490 kJ/mol)反应,导致这种同时含有强氧化剂和强还原剂的溶液热力学不稳定。但是,在室温下进行反应时,该反应的反应动力学非常缓慢,因此在一天的过程中能够进行的反应非常少。
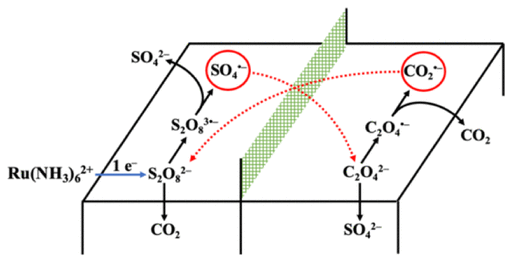
有鉴于此,犹他大学Henry S. White教授、明尼苏达大学Matthew Neurock教授、康奈尔大学Héctor D. Abruña教授等报道通过Ru(NH3)62+引发进行S2O82-的1e-还原生成S2O83·-后,能够快速的切断化学键,生成SO42-和强氧化性的SO4·-。
本文要点
(1)
理论上来看,该反应通过电化学生成单分子S2O83·-,随后引发溶液相发生自催化反应并且消耗S2O82-和C2O42-。在一些实验中人们发现了S2O82-/C2O42-的自催化反应。作者通过微分电化学质谱表征,发现在30 s引发后,在反应进行10 min内溶液中检测形成CO2。当使用BaCO3捕获CO2,进一步验证了自催化反应生成CO2。
(2)
通过第一性原理DFT计算,从头算分子动力学模拟等理论计算,以及循环伏安电化学响应的有限差分法(FDM)理论计算,很好的说明了S2O82–/C2O42–自催化的引发和机理。一些初始研究结果说明自催化反应能够导致反应的前端沿着垂直于电极表面的方向向溶液中传播。
参考文献
Jordyn N. Janusz, Joshua A. Beeler, Seyyedamirhossein Hosseini, Mayank Tanwar, Rui Zeng, Hongsen Wang, Héctor D. Abruña*, Matthew Neurock*, and Henry S. White*, The Electrochemical Peroxydisulfate-Oxalate Autocatalytic Reaction, J. Am. Chem. Soc. 2024
DOI: 10.1021/jacs.4c08080
https://pubs.acs.org/doi/10.1021/jacs.4c08080


















