在肿瘤细胞中,可控的小分子-mRNA共价修饰可以在单线态氧(1O2)的启动下完成修饰过程,这也是一种重要的基因治疗策略。然而,体内产生的1O2往往依赖于外界光的激发,而激光的组织穿透有限等问题仍会极大地干扰深部肿瘤光学治疗的有效性。有鉴于此,华中科技大学赵元弟教授、Jin-Xuan Fan和Kai Cheng构建了一种肿瘤靶向纳米胶束,其可在无需外界光的情况下自发地在细胞内生成1O2,以在肿瘤细胞中实现对mRNA的高水平共价修饰。
本文要点:
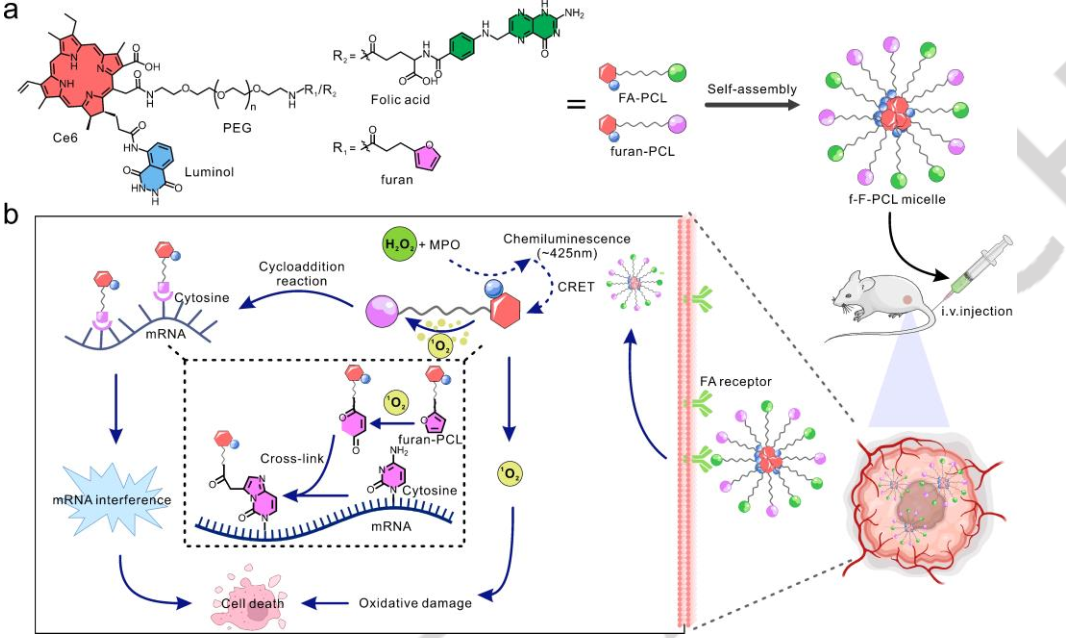
(1)在肿瘤微环境(TME)中的高浓度过氧化氢(H2O2)的触发下,化学键合的鲁米诺和Ce6可通过化学发光共振能量转移(CRET)产生1O2。研究发现,1O2能够将负载的呋喃氧化为高活性的二羰基部分,其可与mRNA上的腺嘌呤(A)、胞嘧啶(C)或鸟嘌呤(G)发生环加成反应,以干扰肿瘤细胞的蛋白表达,从而抑制肿瘤的进展。
(2)体内外实验结果表明,这种自启动的基因治疗纳米胶束可以在没有外界光的情况下诱导1O2对mRNA进行共价修饰,并且研究者能够通过荧光成像技术对该过程进行实时监控。综上所述,该研究工作为基于RNA的肿瘤基因治疗提供了一种新的有效策略。
Yong Li. et al. Self-Initiated Nano-Micelles Mediated Covalent Modification of mRNA for Labeling and Treatment of Tumors. Angewandte Chemie International Edition. 2024
DOI: 10.1002/anie.202411598
https://onlinelibrary.wiley.com/doi/10.1002/anie.202411598



















